
����Ŀ�����ᱵ����Ϊ�������մɹ�ҵ��֧��������ҵ��ȡ������ͼ���Ȼ�ò����Բ������ѱ�����[BaTiO(C2O4)24H2O]�����պ�ɻ�����ᱵ���塣
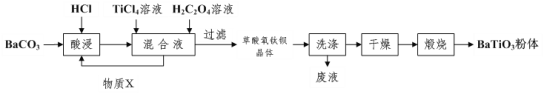
��1�����ʱ�����ķ�Ӧ�����ӷ���ʽΪ___��
��2������TiCl4��Һʱͨ����TiCl4��������Ũ�����ټ�ˮϡ�ͣ���Ŀ����___��
��3������H2C2O4��Һʱ��������Ӧ�Ļ�ѧ����ʽΪ___����ѭ��ʹ�õ�����X��___���ѧʽ�������ʵ�鷽����֤�������ѱ������Ƿ�ϴ�Ӹɾ���___��
��4�����ղ������ѱ�����õ�BaTiO3��ͬʱ�����ɸ����µ���̬������CO��___��
��5����ҵ���ñ���Na2CO3��Һ�����ؾ�ʯ����Ҫ�ɷ���BaSO4�������ﵽƽ��������ϲ���Һ���ظ���β���������ת��Ϊ���������BaCO3������BaCO3�Ʊ��������Ρ���֪�����£�Ksp(BaSO4)��1.0��10��10��Ksp(BaCO3)��2.59��10��9������������Ҫ___molL��1��̼������Һ���ݲ���ʵ������ת��������CO32����ˮ�⣩��
���𰸡�BaCO3+2H+=Ba2++CO2��+H2O ����TiCl4��ˮ�� BaCl2+TiCl4+2H2C2O4+5H2O=BaTiO(C2O4)24H2O��+6HCl HCl ȡ���һ��ϴ��Һ���������������ữ�������������������ɣ���˵�������Ѿ�ϴ�Ӹɾ� CO2��H2O��g�� 2.59��10-4
��������
���Ʊ����̿�֪��̼�ᱵ�����ᷴӦ�����Ȼ�����Ȼ���Ȼ��������Ȼ�̼�����ᷴӦ����BaTiO(C2O4)24H2O�����ˡ�ϴ�ӡ�������յõ�BaTiO3��
(1)̼�ᱵ�����ᷴӦ�����Ȼ�����ˮ��������̼��
(2)TiCl4�ɷ���ˮ�ⷴӦ��
(3)����H2C2O4��Һ���ɲ������ѱ����壬ͬʱ����HCl��ѭ��ʹ�ã�������������������Ƿ�ϴ�Ӹɾ���
(4)BaTiO(C2O4)24H2O���գ������ֽⷴӦ�����ɸ����µ����������CO��CO2��H2O(g)��
(5)����Ksp(BaSO4)���㱥����Һ����������ӵ�Ũ�ȣ��ٸ���ƽ�ⳣ������c(CO32��)��
(1)̼�ᱵ�����ᷴӦ�����Ȼ�����ˮ��������̼�����ӷ�ӦΪBaCO3+2H+��Ba2++CO2��+H2O��
(2)TiCl4�ɷ���ˮ�ⷴӦ����ͨ����TiCl4����Ũ���ᣬĿ��������TiCl4��ˮ�⣻
(3)����H2C2O4��Һ���ɲ������ѱ����壬��ӦΪBaCl2+TiCl4+2H2C2O4+5H2O��BaTiO(C2O4)24H2O��+6HCl��ͬʱ����HCl(������)��ѭ��ʹ�ã���������Ƿ�ϴ�Ӹɾ�����ȡ���һ��ϴ��Һ���������������ữ�������������������ɣ���˵�������Ѿ�ϴ�Ӹɾ���
(4)BaTiO(C2O4)24H2O���գ������ֽⷴӦ����Ԫ���غ��֪�����ɸ����µ����������CO��CO2��H2O(g)��
(5)��֪Ksp(BaSO4)��1.0��10��10�������ᱵ��Һ����������ӵ�Ũ��c(SO42��)��![]() ��1.0��10��5mol/L����c(CO32��)��
��1.0��10��5mol/L����c(CO32��)��![]() mol/L��2.59��10��4mol/L��
mol/L��2.59��10��4mol/L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CH4��������CO2�����ɵõ�����CO�Ļ���ԭ�ϡ��ش��������⣺
��1��CH4��������CO2�Ĵ�ת����ͼ��ʾ��
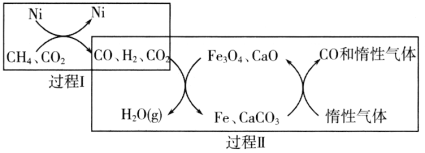
����֪��ط�Ӧ�������仯��ͼ��ʾ��

���̢���Ȼ�ѧ����ʽΪ________��
�ڹ����������̢��˵������ȷ����________������ţ���
a��ʵ���˺�̼�����뺬�����ʵķ���
b���ɱ�ʾΪCO2��H2��H2O��g����CO
c��COδ���뷴Ӧ
d��Fe3O4��CaOΪ�����������˷�Ӧ�Ħ�H
�������������䣬�ڲ�ͬ�������������£���ӦCH4��g����CO2��g����2CO��g����2H2��g��������ͬʱ���CH4��ת�����淴Ӧ�¶ȵı仯��ͼ��ʾ��a����������״̬________����ǡ����ǡ���ƽ��״̬��b��CH4��ת���ʸ���c�㣬ԭ����________��
��2����һ�����ܱ������У�CH4��CO2�ķ�ѹ�ֱ�Ϊ20kPa��25kPa������Ni������Al2O3������������1123Kʹ�䷢����ӦCH4��g����CO2��g����2CO��g����2H2��g����

���о�����CO���������ʦԣ�CO����1.3��10��2��p��CH4����p��CO2��mol��g��1��s��1��ijʱ�̲��p��CO����20kPa����p��CO2����________kPa���ԣ�CO����________mol��g��1��s��1��
�ڴﵽƽ�������ϵѹǿ����ʼʱ��1.8������÷�Ӧ��ƽ�ⳣ���ļ���ʽΪKp��________��kPa��2�����ø����ʵķ�ѹ�������ʵ���Ũ�ȼ��㣩
��3��CH4��������CO2�õ���CO��ż����Ӧ���Ƶò��ᣨH2C2O4���������£���ijŨ�ȵIJ�����Һ�м���һ��Ũ�ȵ�NaOH��Һ��������Һ��![]() �����ʱ��Һ��pH��________������֪������H2C2O4��Ka1��6��10��2��Ka2��6��10��5��lg6��0.8��
�����ʱ��Һ��pH��________������֪������H2C2O4��Ka1��6��10��2��Ka2��6��10��5��lg6��0.8��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����������������������ȷ����( )
A. ��״���£�22.4L H2O���еķ�����Ϊ NA
B. ͨ��״���£�NA ��CO2����ռ�е����Ϊ22.4L
C. ���ʵ���Ũ��Ϊ1mol/L��MgCl2��Һ�У�����Cl������Ϊ2NA
D. ���³�ѹ�£�1.06g Na2CO3���е�Na+������Ϊ0.02 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͼʾ���ó��Ľ�����ȷ����
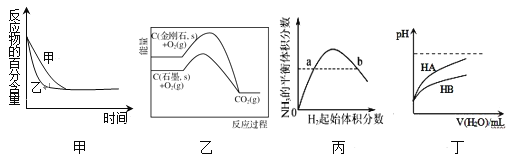
A.ͼ�ױ�ʾѹǿ�Կ��淴Ӧ2A(g)+2B(g)![]() 3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ��
3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ��
B.ͼ���ǽ��ʯ��ʯī�ֱ���������CO2��������ϵ���ߣ�˵��ʯīת��Ϊ���ʯ�ķ�Ӧ����H>0
C.ͼ����ʾһ�������µĺϳɰ���Ӧ�У�NH3��ƽ�����������H2��ʼ�������(N2����ʼ���㶨)�ı仯��ͼ��a��N2��ת���ʴ���b��
D.ͼ����ʾ�����£�ϡ��HA��HB�������ϡ��Һʱ����ҺpH���ˮ���ı仯������ͬ������NaA��Һ��pH����ͬŨ�ȵ�NaB��Һ��pH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2018��11��13�յ�26����ʼ������Թ��ʵ�λ�ƽ����ġ��µ�Ħ���Ķ���涨��1Ħ�����ʰ��������ӵ�����NA��������Ԫ�������йذ����ӵ�����NA��˵����ȷ���ǣ� ��
A.���³�ѹ�£�11gCO2�к���0��75NA��ԭ��
B.2.4gþ���þ����ʱ��ʧȥ�ĵ�����ĿΪ0.1NA
C.��״���£�NA��ˮ���ӵ����ԼΪ22��4L
D.1L 0��3mol��L��NaCl��Һ�к���0��3NA��NaCl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ����Ԫ����Br��ʽ���ڣ���ҵ���ÿ����������Ӻ�ˮ����ȡ��Ĺ���������ͼ��ʾ��
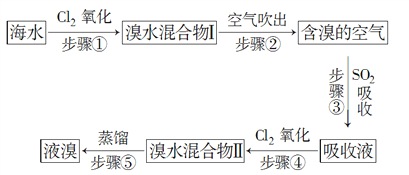
(1)����ٷ�Ӧ�����ӷ���ʽ��____________________������۷�Ӧ�Ļ�ѧ����ʽ��___________________��
(2)�������Ͽ��ǣ���������Ҳ������Br2����___________(����ĸ)��
A��NaOH�������� B��FeCl2
C��Na2SO3 D��H2O
(3)���������������________������Ӧ������2 mol HBr��������________mol SO2��
(4)����������Ӧ�ж�SO2��Cl2��Br2����������������ǿ������˳����________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⼰�仯������������Ӧ�ù㷺�����е����ӵ���Һ����մ�����
��1�������ѭ�������Ƿֽ�ˮ�Ʊ��������о��ȵ㣬�漰����������Ӧ��
��Ӧ��SO2(g)+I2(aq)+2H2O(l)=2HI(aq)+H2SO4(aq) ��H1
��Ӧ��HI(aq)=![]() H2(g)+
H2(g)+![]() I2(aq) ��H2
I2(aq) ��H2
��Ӧ��2H2SO4(aq)=2SO2(g)+O2(g)+2H2O(l)
�ٷ�Ӧ��SO2(g)+2H2O(l)=H2SO4(aq)+H2(g)����H=___������H1����H2��ʾ����
�ڷ���������Ӧ�������ж���ȷ����___
a����Ӧ�����ڳ����½��� b����Ӧ����SO2��ԭ�Ա�HIǿ
c��ѭ���������貹��H2O d��ѭ�������в���1molO2ͬʱ����1molH2
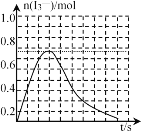
�۷�ӦI����ʱ����Һ�д�������ƽ�⣺I2(aq)+I-(aq)![]() I3-(aq)���䷴Ӧ���ʼ�����ƽ�ⳣ�����ֽ�1molSO2����ͨ�뺬1molI2��ˮ��Һ����ǡ����ȫ��Ӧ����Һ��I3-�����ʵ���n(I3-)�淴Ӧʱ��(t)�ı仯������ͼ��ʾ����ʼ��n(I3-)�������ԭ����___��
I3-(aq)���䷴Ӧ���ʼ�����ƽ�ⳣ�����ֽ�1molSO2����ͨ�뺬1molI2��ˮ��Һ����ǡ����ȫ��Ӧ����Һ��I3-�����ʵ���n(I3-)�淴Ӧʱ��(t)�ı仯������ͼ��ʾ����ʼ��n(I3-)�������ԭ����___��
��2���ú�����ȡ��ʱ�����������������������ɵ��ʡ����������£��������������ܽ��ⵥ�ʽ�һ�������ɵ��������(IO3-)��д��������ⵥ�ʷ�Ӧ�����ӷ���ʽ��___��
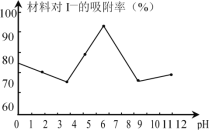
��3������С�������Ͳ���Ag/TiO2����Һ�е����ӽ��������о�����ͼ�Dz�ͬpH�����£�����������Ч���ı仯���ߡ��ݴ��ƶ�Ag/TiO2�������ʺ�����___������ԡ������ԡ����ԡ�����Һ�е�I����
��4���Ȼ�������������Ҳ����Ч���������ӡ��Ȼ��������������Ե����ӵ�������ӦΪI��(aq)+AgCl(s)![]() AgI(s)+Cl��(aq)����Ӧ�ﵽƽ�����Һ��c(I��)=___[��c(Cl��)��Ksp(AgCl)��Ksq(AgI)��ʾ]���÷���ȥ�������ӵ�ԭ����___��
AgI(s)+Cl��(aq)����Ӧ�ﵽƽ�����Һ��c(I��)=___[��c(Cl��)��Ksp(AgCl)��Ksq(AgI)��ʾ]���÷���ȥ�������ӵ�ԭ����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���N(![]() )��һ�ֳ������л��ϳ��м��壬����������;�㷺��
)��һ�ֳ������л��ϳ��м��壬����������;�㷺��
�л���AΪԭ�Ϻϳ�M��N��·��������ʾ��

��֪��I.R-CH=CH2+HBr ![]() R-CH2CH2Br
R-CH2CH2Br
II.R-CH2-CN![]() R-CH2-COOH
R-CH2-COOH ![]()
![]()
��ش��������⣺
(1)A�����й����ԭ�������Ϊ___________������CN�ĵ���ʽΪ___________��
(2)�ڵķ�Ӧ����Ϊ___________��E���������������ŵ�����Ϊ___________��G�Ľṹ��ʽΪ______________________��
(3)д����Ӧ�ݵĻ�ѧ����ʽ__________________________��
(4)д��M������������ˮ��Ļ�ѧ����ʽ______________________��
(5)D��ͬ���칹���У��ܷ���������Ӧ���������Ʒ�Ӧ�ų�H2�Ĺ���___________�֣�д���˴Ź���������4��壬�ҷ������Ϊ1��1��2��6��һ��ͬ���칹��Ľṹ��ʽ��___________��
(6)�����Ϣ��д����E���Ҵ�Ϊԭ���Ʊ�������N�ĺϳ�·�ߣ�(�����Լ���ѡ)___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ���������������ѧ������������мס��Ҿ�Ϊ���ʣ����ǵ�ת����ϵ��ͼ��ʾ(ijЩ�����Ͳ��ֲ�������ȥ)��
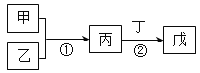
��1�������ɶ�������ԭ�Ӱ뾶���Ľ���Ԫ����ɣ���д������18����˫ԭ�������ӵĵ���ʽ___��
��2�����ҡ�����ϻ��������Ͼ��������̣����������Ļ�ѧ����___��
��3�����ס��������������ᷴӦ����������������Һ��Ӧ�������ˮ��Һ�ڿ����м���ֱ���������õ��Ĺ�������Ϊ___��
��4��������һ���д̼�����ζ�����壬������0.1mol/L����Һ��pH=0.7����д����Ӧ�ڵ����ӷ���ʽ___��
��5������Ӧ���dz����Ŀ��淴Ӧ�����ȷ�Ӧ���÷�Ӧ�����������ǣ�����ý���������¶�700K���ң�ѹǿ30-50Mpa������һ����ʽ�Ρ���д����������ӵ��뷽��ʽ___��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com