
【题目】下列有关常温下0.1 mol/L氨水(pH=11)的说法正确的是
A.该氨水显弱碱性
B.加水稀释过程中,![]() 的值减小
的值减小
C.与同温下pH=11的NaOH溶液相比,NaOH溶液中c(Na+)大于氨水中c(NH4+)
D.加入少量NH4Cl 固体,溶液中水的电离平衡:H2O![]() H+ + OH―向右移动
H+ + OH―向右移动
科目:高中化学 来源: 题型:
【题目】由C、Mg、Ni三种元素组成的一种简单立方结构的化合物具有超导性,其晶胞中C位于体心位置,Mg位于顶角,Ni占据面心位置,该化合物的化学式为________,晶体中Mg原子周围距离最近的Ni原子有________个,该新型超导材料晶胞参数a=0.38nm,计算该晶体的密度________(gcm﹣3)(保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铋酸钠(NaBiO3)是分析化学中的重要试剂,在水中缓慢分解,遇沸水或酸则迅速分解。某兴趣小组设计实验制取铋酸钠并探究其应用。回答下列问题:
Ⅰ.制取铋酸钠
制取装置如图(加热和夹持仪器已略去),部分物质性质如下:
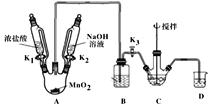
物质 | NaBiO3 | Bi(OH)3 |
性质 | 不溶于冷水,浅黄色 | 难溶于水;白色 |
(1)B装置用于除去HCl,盛放的试剂是___;
(2)C中盛放Bi(OH)3与NaOH混合物,与Cl2反应生成NaBiO3,反应的离子方程式为___;
(3)当观察到___(填现象)时,可以初步判断C中反应已经完成;
(4)拆除装置前必须先除去烧瓶中残留Cl2以免污染空气。除去Cl2的操作是___;
(5)反应结束后,为从装置C中获得尽可能多的产品,需要的操作有___;
Ⅱ.铋酸钠的应用——检验Mn2+
(6)往待测液中加入铋酸钠晶体,加硫酸酸化,溶液变为紫红色,证明待测液中存在Mn2+。
①产生紫红色现象的离子方程式为___;
②某同学在较浓的MnSO4溶液中加入铋酸钠晶体,加硫酸酸化,结果没有紫红色出现,但观察到黑色固体(MnO2)生成。产生此现象的离子反应方程式为___。
Ⅲ.产品纯度的测定
(7)取上述NaBiO3产品wg,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用cmo1·L-1的H2C2O4标准溶液滴定生成的MnO4-(已知:H2C2O4+MnO4-——CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗vmL标准溶液。
该产品的纯度为___(用含w、c、v的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CO2分子晶体可转化为具有类似SiO2结构的原子晶体.从理论上分析,下列说法正确的是( )
A.该转化过程是物理变化
B.1molCO2原子晶体中含2mol C﹣O键
C.CO2原子晶体的熔点高于SiO2
D.CO2的原子晶体和分子晶体互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】饱和食盐水中加入碳酸氢铵可制备小苏打,滤出小苏打后,向母液中通入氨,再冷却、加食盐,过滤,得到氯化铵固体.下列分析错误的是( )
A.该制备小苏打的方程式为:NaCl+NH4HCO3→NaHCO3↓+NH4Cl
B.母液中通入的氨气与HCO3﹣反应:NH3+HCO3﹣→CO32﹣+NH4+
C.加食盐是为增大溶液中Cl﹣的浓度
D.由题可知温度较低时,氯化铵的溶解度比氯化钠的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡有SnCl2、SnCl4两种氯化物.SnCl4是无色液体,极易水解,熔点﹣36℃,沸点114℃,金属锡的熔点为231℃.实验室用熔融的金属锡跟干燥的氯气直接作用制取无水SnCl4(此反应过程放出大量的热).实验室制取无水SnCl4的装置如图所示.
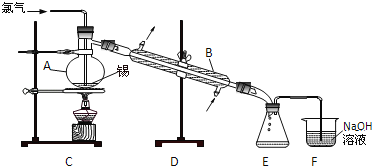
完成下列填空:
(1)仪器A的名称__; 仪器B的名称__.
(2)实验室制得的氯气中含HCl和水蒸气,须净化后再通入液态锡中反应,除去HCl的原因可能是__;除去水的原因是__.
(3)当锡熔化后,通入氯气开始反应,即可停止加热,其原因是__.若反应中用去锡粉11.9g,反应后在锥形瓶中收集到23.8g SnCl4,则SnCl4的产率为__.
(4)SnCl4遇水强烈水解的产物之一是白色的固态二氧化锡.若将SnCl4少许暴露于潮湿空气中,预期可看到的现象是__.
(5)已知还原性Sn2+>I﹣,SnCl2也易水解生成难溶的Sn(OH)Cl.如何检验制得的SnCl4样品中是否混有少量的SnCl2?__.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用含碳化合物合成燃料是解决能源危机的重要方法,已知煤液化过程中有反应CO(g)+2H2(g)=CH3OH(g),其反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )
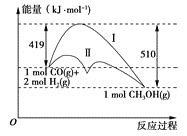
A.该反应的反应热ΔH=+91kJ·mol-1
B.加入催化剂后,该反应的ΔH变小
C.反应物的总能量大于生成物的总能量
D.从图中可以看出,使用催化剂降低了该反应的活化能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)铜是生命必需的元素,也是人类广泛使用的金属。现代工业上,主要采用高温冶炼黄铜矿(CuFeS2,也可表示为Cu2SFe2S3)的方法获得铜。火法炼铜首先要焙烧黄铜矿:2CuFeS2+4O2![]() Cu2S+3SO2+2FeO,反应中被还原的元素有_________,每转移0.6mol电子,有_________mol硫被氧化。
Cu2S+3SO2+2FeO,反应中被还原的元素有_________,每转移0.6mol电子,有_________mol硫被氧化。
(2)产物中的SO2是一种大气污染物,可选用下列试剂中的_________吸收(选填编号)。
a.浓H2SO4b.稀HNO3c.NaOH溶液d.CaCl2
(3)Cu2O投入足量的某浓度的硝酸中,若所得气体产物为NO和NO2的混合物,且体积比为1﹕1,发生反应的化学方程式为:____________________________________。
(4)某同学通过电化学原理实现了如下转化:Cu+2H+→Cu2++H2↑,则H2在_________极获得(填写电极名称)。
(5)向氯化铜和氯化铁的混合溶液中加入氧化铜粉末会产生新的沉淀,写出该沉淀的化学式_________。请用平衡移动的原理,结合必要的离子方程式,对此现象作出解释______。
(6)将SO2气体通入CuCl2溶液中,生成CuCl沉淀的同时,还有产物_________(填写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
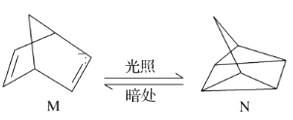
(1)有机物M经过太阳光光照可转化成N,转化过程如下,ΔH=+88.6 kJ·mol-1。则M、N相比,较稳定的是________。
(2)已知CH3OH(l)的燃烧热ΔH=-726.5 kJ·mol-1,CH3OH(l)+![]() O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1则a________726.5(填“>”“<”或“=”)
O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1则a________726.5(填“>”“<”或“=”)
(3)将Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145.0 kJ热量,写出该反应的热化学方程式:________________________________________。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO2(s)+3C(s)===2Al2O3(s)+3TiC(s) ΔH=-1 176.0 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为_______。
(5) 已知:①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH2=-566 kJ·mol-1
③TiO2(s)+2Cl2(g)===TiCl4(s)+O2(g) ΔH3=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)===TiCl4(s)+2CO(g)的 ΔH=__________________。
(6)已知拆开1 mol H—H键,1 mol N—H键,1mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为:________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com