
| A、0.5 mol/L |
| B、1.0 mol/L |
| C、1.5 mol/L |
| D、2.0 mol/L |
| n |
| V |
| 0.75mol |
| 0.5L |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、乙烯水化:CH2=CH2+H2O
| |||
B、葡萄糖发酵:C6H12O6
| |||
C、溴乙烷水解:CH3CH2Br+H2O
| |||
D、丙酸乙酯水解:CH3CH2COOCH2CH3+H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
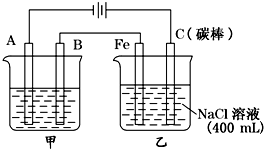 如图为相互串联的甲乙两电解池
如图为相互串联的甲乙两电解池| 物质 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
| KSP | 8.0×10-16 | 4.0×10-38 | 3.0×10-17 | 2.2×10-20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、14.2mg | ||
| B、174g | ||
C、
| ||
| D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应率的影响,在常温下按照如下方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应率的影响,在常温下按照如下方案完成实验. | 实验编号 | 反应物 | 催化剂 |
| ① | 10mL 2% H2O2溶液 | 无 |
| ② | 10mL 5% H2O2溶液 | 无 |
| ③ | 10mL 5% H2O2溶液 | 1mL 0.1mol?L-1 FeCl3溶液 |
| ④ | 10mL 5% H2O2溶液+少量HCl溶液 | 1mL 0.1mol?L-1 FeCl3溶液 |
| ⑤ | 10mL 5% H2O2溶液+少量NaOH溶液 | 1mL 0.1mol?L-1 FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 组别 | 药品1 | 药品2 | 实验现象 |
| Ⅰ | 0.01mol/L NaOH溶液 | 0.01mol/L MgCl2溶液 | 生成白色沉淀 |
| Ⅱ | 0.01mol/L氨水 | 0.01mol/L MgCl2溶液 | 无现象 |
| Ⅲ | 0.1mol/L氨水 | 0.1mol/L MgCl2溶液 | |
| IV | 0.1mol/L氨水 | 0.01mol/L MgCl2溶液 | 生成白色沉淀 |
| V | 0.01mol/L氨水 | 0.1mol/L MgCl2溶液 | 无现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可以利用紫色石蕊试液一次性把NaOH 溶液、稀硫酸、NaCl溶液鉴别出来 |
| B、可以按溶解、过滤、蒸发的操作顺序将硝酸钾和硝酸钠它们分离出来 |
| C、用氢气还原氧化铜实验中,先加热再通入氢气 |
| D、稀释浓硫酸时,先在烧杯里倒入浓硫酸,再小心倒入水并不断搅拌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com