
����Ŀ������������ȷ����
A. ������������������������������ʱ����������ʯī����
B. ��������ĵ���ˮ��Һ�У��ȼ�����������Һ���ټӵ�ˮ����������Ƿ�ˮ����ȫ
C. ��Ӧ3Si(s)+2N2(g)=Si3N4(s)���Է����У���÷�Ӧ����H<0
D. ��֪BaSO4��Ksp= (Ba2+ )��c(SO42-)������BaSO4����������Һ���ܽ�ﵽ����ʱ��c(Ba2+)=c(SO42-)=![]()
���𰸡�C
��������
A.�������������������������û�ԭ�Աȸ���ǿ�Ľ�����Ϊ����������������Ӧ�����ģ���Ӧ��������һ�ֱȸ������õĽ���������Zn����A����
B.��������������Һ��Ӧ�����ܼ�������Ƿ���ȫˮ�⣬ˮ����ֱ�Ӽ���⣬���ܼ���������������ƣ���B����
C.�÷�Ӧ��һ�����������С�ķ�Ӧ������S<0�������Ӧ���Է����У��÷�Ӧ��H-T��S<0������H<0����C��ȷ��
D.�����ᱵ�ĵ�һ������Һ��ʽ�ӳ�������Na2SO4��Һ��c��SO42-�������ܽ�ƽ��BaSO4��s��![]() Ba2+��aq��+SO42-��aq�������ƶ���c��Ba2+����С��Ksp���䣬����Na2SO4��Һ���ܽ�ﵽ����ʱc��Ba2+��<
Ba2+��aq��+SO42-��aq�������ƶ���c��Ba2+����С��Ksp���䣬����Na2SO4��Һ���ܽ�ﵽ����ʱc��Ba2+��<![]() <c��SO42-������D����
<c��SO42-������D����
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮAlCl3���������������л��ϳɵĴ����ȣ���ҵ����������Al2O3��Fe2O3��Ϊԭ���Ʊ���ˮAlCl3�Ĺ����������£�

��1������¯��Al2O3��Cl2��C��Ӧ�Ļ�ѧ����ʽ______��
��2����Na2SO3��Һ�ɳ�ȥ��ȴ���ų���β���е�Cl2���˷�Ӧ�����ӷ���ʽ______��
��3��Ϊ�˲ⶨ�Ƶõ���ˮAlCl3��Ʒ��������FeCl3���Ĵ��ȣ���ȡ16.25g��ˮAlCl3��Ʒ�����ڹ�����NaOH��Һ�У����˳��������ϴ�ӡ����ա���ȴ�����ء���������Ϊ0.32g��
��д�������ⶨ�������漰�����ӷ���ʽ��______��__________��
��AlCl3��Ʒ�Ĵ���Ϊ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2 L�ܱ������ڣ�800 ��ʱ��Ӧ��2NO(g)��O2(g)![]() 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0��020 | 0��010 | 0��008 | 0��007 | 0��007 | 0��007 |
��1��800������Ӧ�ﵽƽ��ʱ��NO�����ʵ���Ũ����________��
��2����ͼ�б�ʾNO2�ı仯��������________����O2��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v��________��

��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����________��
a��v(NO2)��2v(O2) b��������ѹǿ���ֲ���
c��v��(NO)��2v��(O2) d���������ܶȱ��ֲ���
��4����ʹ�÷�Ӧ�ķ�Ӧ�����������________��
a����ʱ�����NO2���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ijͬѧ��Ƶķ��ȷ�Ӧ�Ĺ۲�װ�ã�

��ʵ������������£�
����ͼ��ʾ��ʵ��װ�����Ӻã�
����U�ι��ڼ���������īˮ(��Ʒ����Һ)����T�ιܻ���,ʹU�ι������ߵ�Һ�洦��ͬһˮƽ��,�ٹر�T�ιܻ�����
����ʢ��1.0g�����Ƶ�С�Թ������2 mL���ҵ�����ˮ���۲�����
�Իش�:
��1��ʵ��ǰ������е�һ��ʵ�������_______________��
��2��ʵ���й۲쵽��������______________________________________________________________��
��3��ʵ���з����Ļ�ѧ��Ӧ����ʽ:____________________________��
��4��˵��CaO��H2O��������Ca(OH)2������֮��Ĺ�ϵ:_______________________________________��
��5������ʵ����CaO����NaCl��ʵ�黹�ܷ�۲쵽��ͬ����?____(����������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ҽҩ�ϳ��п����������̺ϳ�һ���������ಡ����Чҩ��(G)��

��֪:��RCH=CH2![]() RCH2CH2CHO��
RCH2CH2CHO��
��
��1��B�ĺ˴Ź�������ͼ����_______�����շ�,C������Ϊ_________��
��2��E�к��������ŵ�����Ϊ_______��д��D��E�Ļ�ѧ����ʽ_______ ��
��3��E-F�ķ�Ӧ����Ϊ________ ��
��4��E��ͬ���칹���У��ṹ�����Ѽ��ұ�����ֻ��һ��ȡ�����ṹ��_____�֣�д�����м���Ŀ����ͬ���칹��Ľṹ��ʽ_______ ��
��5�������йز���G��˵����ȷ����__________
A.G�ķ���ʽΪC15H28O2 B.1molGˮ��������2molNaOH
C.G��������8��Cԭ�ӹ�ƽ�� D.�ϳ�·��������G�ķ�ӦΪȡ����Ӧ
��6��д����1-����Ϊԭ���Ʊ�C��ͬ���칹��������(CH3CH2CH2CH2COOH)���ϳ�·������ͼʾ������:H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH�����Լ���ѡ��___________
CH3CH2OH�����Լ���ѡ��___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��CH2=CHCH3(g)+Cl2(g)![]() CH2=CHCH2Cl(g)+HCl(g)����һ��ѹǿ�£���
CH2=CHCH2Cl(g)+HCl(g)����һ��ѹǿ�£���![]() ���ܱ������г����������ϩ��ͼ�ױ�ʾƽ��ʱ����ϩ���������(
���ܱ������г����������ϩ��ͼ�ױ�ʾƽ��ʱ����ϩ���������(![]() )���¶�(T)��
)���¶�(T)��![]() �Ĺ�ϵ��ͼ�ұ�ʾ��Ӧ��ƽ�ⳣ��K���¶�T�Ĺ�ϵ��������˵����ȷ����
�Ĺ�ϵ��ͼ�ұ�ʾ��Ӧ��ƽ�ⳣ��K���¶�T�Ĺ�ϵ��������˵����ȷ����

A. ͼ����![]()
B. ���ں��ݾ���װ���н���������Ӧ���ﵽƽ��ʱ��װ���ڵ�����ѹǿ������
C. �¶�T1��![]() �� Cl2��ת����ԼΪ33.3%
�� Cl2��ת����ԼΪ33.3%
D. ͼ���У���A��ʾ����Ӧ��ƽ�ⳣ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��H�������ʴ�������ͼ��ʾ��ת����ϵ(��Ӧ���������ֲ���δ���)����֪A�����Σ�B��ʹƷ����Һ��ɫ��G�Ǻ���ɫ���塣�Իش��������⣺
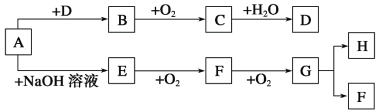
(1)д�����и����ʵĻ�ѧʽ��A________________��B________________��
(2)��Ҫ��д�����з�Ӧ���йط���ʽ
E��F��Ӧ�Ļ�ѧ����ʽ_____________________________________________________��
G��H��Ӧ�����ӷ���ʽ_____________________________________________________��
(3)д��H��Ũ��Һ��ľ̿��Ӧ�Ļ�ѧ����ʽ_______________________________________��
(4)����D�������ӵķ�����___________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A��B�ֱ�Ϊ0.6mol��0.5mol����0.4L�ܱ������з�����Ӧ��3A+B=mC+2D����5min��ﵽƽ�⣬��ʱCΪ0.2mol���ڴ�ʱ����D��ƽ����Ӧ����Ϊ0.1molL��1min��1�����н��۴�����ǣ�������
A.ƽ��ʱ��Ӧ����������ʵ���Ϊ1molB.B��ת����Ϊ20%
C.A��ƽ����Ӧ����Ϊ0.15 molL��1min��1D.mֵΪ2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȼ��Ŀ����ʯ�ij���ͱ仯�յ�����������Ӱ�졣�ؿ���ÿ����1km,ѹǿ����Լ25000-30000kPa���ڵؿ���SiO2��HF����һ��ƽ�⣺SiO2(s) +4HF(g)![]() SiF4(g)+ 2H2O(g) ��H=��148.9kJ/mol��
SiF4(g)+ 2H2O(g) ��H=��148.9kJ/mol��
(1)д��H2O�ĵ���ʽ��___________,SiF4�Ľṹʽ��____________
(2)�ڵؿ��������___________�����ݳ����ڵؿ�dz��������___________�������÷�Ӧ��ƽ�ⳣ������ʽΪ��K=_______________�����������Ӧ��ƽ�ⳣ��Kֵ��÷�Ӧ_______(ѡ����)��
a��һ��������Ӧ�����ƶ� b����ƽ���ƶ�ʱ����Ӧ������������С
c��һ�����淴Ӧ�����ƶ� d����ƽ���ƶ�ʱ�淴Ӧ�����ȼ�С������
(3)����Ӧ�������ݻ�Ϊ2.0L����Ӧʱ��8.0 min��������������ܶ�������0.12 g/L�������ʱ����HF��ƽ����Ӧ����Ϊ______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com