
4.6g铜镁合金完全溶解于100ml密度为1.40g/ml、质量分数为63%的浓硝酸中,得到4480mlNO2和336 ml N2O4的混合气体(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液至离子恰好全部沉淀时,下列说法不正确的是 ( )
| A.该合金中铜与镁的物质的量之比是46:69 |
| B.该浓硝酸中HNO3的物质的量浓度是14.0mol/L |
| C.产生沉淀8.51 g |
| D.离子恰好完全沉淀时,加入NaOH溶液的体积是230mL |
D
解析试题分析: A.4480mL NO2的物质的量=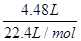 =0.2mol,336mL N2O4的物质的量=
=0.2mol,336mL N2O4的物质的量= =0.015mol,令Cu、Mg的物质的量分别为xmol、ymol,根据二者质量与电子转移守恒,可得:64x+24y=4.6,2x+2y=0.2+0.015×2 ,解得x=0.046、y=0.069,故该合金中铜与镁的物质的量之比=0.046mol:0.069mol=46:69,故A正确;B.密度为1.40g·mL-1、质量分数为63%的浓硝酸.其物质的量浓度=
=0.015mol,令Cu、Mg的物质的量分别为xmol、ymol,根据二者质量与电子转移守恒,可得:64x+24y=4.6,2x+2y=0.2+0.015×2 ,解得x=0.046、y=0.069,故该合金中铜与镁的物质的量之比=0.046mol:0.069mol=46:69,故A正确;B.密度为1.40g·mL-1、质量分数为63%的浓硝酸.其物质的量浓度=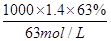 =14mol·L-1,故B正确;C.铜镁合金完全溶解于浓硝酸中,向反应后的溶液中加入NaOH溶液至离子恰好全部沉淀,生成沉淀为Cu(OH)2、Mg(OH)2,由化学式可知n(OH-)=2n(Cu)+2n(Mg)=2×(0.046mol+0.069mol)=0.23mol,故沉淀质量=m(Cu)+m(Mg)+m(OH-)=4.6g+0.23mol×17g·mol-1=8.51g,故C正确;D.离子恰好完全沉淀时,此时溶液中溶质为NaNO3,根据N元素守恒可知n原(HNO3)=n(NaNO3)+n(NO2)+2n(N2O4),故n(NaNO3)=0.1L×14mol·L-1-0.2mol-2×0.015mol=1.17mol,根据钠离子守恒有n(NaOH)=n(NaNO3)=1.17mol,故需要氢氧化钠溶液的体积=
=14mol·L-1,故B正确;C.铜镁合金完全溶解于浓硝酸中,向反应后的溶液中加入NaOH溶液至离子恰好全部沉淀,生成沉淀为Cu(OH)2、Mg(OH)2,由化学式可知n(OH-)=2n(Cu)+2n(Mg)=2×(0.046mol+0.069mol)=0.23mol,故沉淀质量=m(Cu)+m(Mg)+m(OH-)=4.6g+0.23mol×17g·mol-1=8.51g,故C正确;D.离子恰好完全沉淀时,此时溶液中溶质为NaNO3,根据N元素守恒可知n原(HNO3)=n(NaNO3)+n(NO2)+2n(N2O4),故n(NaNO3)=0.1L×14mol·L-1-0.2mol-2×0.015mol=1.17mol,根据钠离子守恒有n(NaOH)=n(NaNO3)=1.17mol,故需要氢氧化钠溶液的体积= =1.17L=1170mL,故D错误,
=1.17L=1170mL,故D错误,
考点:考查混合物计算。


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:单选题
下列叙述正确的是
| A.在氧化还原反应中,金属单质一般只作还原剂 |
| B.氧化还原反应中非金属单质一定是氧化剂 |
| C.金属元素被还原时所得产物一定是金属单质 |
| D.某元素从化合态变为游离态,该元素一定被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某含铬Cr2O72-废水用硫酸亚铁铵[FeSO4·(NH4)2 SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀干燥后得到n molFeO·FeyCrxO3,其中Cr的化合价为+3价。不考虑处理过程中的实际损耗,下列叙述错误的是
| A.消耗硫酸亚铁铵的物质的量为n(2-x)mol |
B.处理废水中Cr2O72- 的物质的量为 mol mol |
| C.反应中转移的电子为3nx mol |
| D.在FeO·FeyCrxO3中3x=y |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中正确的是( )
| A.含有金属元素的离子一定是阳离子,金属阳离子被还原一定得到金属单质 |
| B.pH相等的NaOH、NaHCO3和Na2CO3三种溶液: c(NaOH)<c(NaHCO3)<c(Na2CO3) |
| C.常温下,c(NH4+)相等的4种溶液:①(NH4)2SO4②(NH4)2Fe(SO4)2③NH4Cl ④(NH4)2CO3,溶质物质的量浓度大小关系是:②<①<④<③ |
| D.某温度时水的离子积常数KW=10-13若将此温度下pH=11的NaOH溶液aL与pH=1的稀硫酸bL混合,若所得混合液pH=2,则a:b=2:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以金红石为原料制取Ti的反应为:
aTiO2+bCl2+cC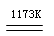 aTiCl4+cCO……反应①
aTiCl4+cCO……反应①
TiCl4+2Mg Ti+2MgCl2……反应②
Ti+2MgCl2……反应②
关于反应①②的分析不正确的是( )
A.TiCl4在反应①中是还原产物,在反应②中是氧化剂
B.C、Mg在反应中均为还原剂,被氧化
C.每生成0.4 mol Ti,反应①②中共转移3.2 mol e-
D.反应①②都是置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
若(NH4)2SO4在强热时分解的产物是SO2、N2、NH3和H2O,则该反应中化合价发生变化和未发生变化的N原子数之比为( )
| A.1:4 | B.1:2 | C.2:1 | D.4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据表中信息,判断下列叙述中正确的是 ( )。
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Fe3+、Br2 | |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知NH4CuSO3与足量的2 mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是( )
| A.反应中硫酸做氧化剂 |
| B.NH4CuSO3中硫元素被氧化 |
| C.1 mol NH4CuSO3完全反应转移0.5 mol电子 |
| D.刺激性气味的气体是氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
工业废水中常含有一定量的Cr2O72—和CrO42—,它们会对生态系统造成很大的损害,其中还原沉淀法是常用的一种处理方法。流程如下:
\其中第①步中存在平衡:2CrO42—(黄色)+2H+ Cr2O72—(橙色)+H2O。下列有关说法正确的是( )
Cr2O72—(橙色)+H2O。下列有关说法正确的是( )
| A.第①步当2v(Cr2O72—)=v(CrO42—)时,达到了平衡状态 |
| B.对于上述平衡,加入适量稀硫酸后,溶液颜色变黄色,则有利于CrO42—的生成 |
| C.第②步中,还原0.1 mol Cr2O72—需要45.6 g FeSO4 |
| D.第③步沉淀剂a可以使用NaOH等碱性物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com