
����˵������ȷ���ǣ� ��
| A�����н���Ԫ�ص�����һ���������ӣ����������ӱ���ԭһ���õ��������� |
| B��pH��ȵ�NaOH��NaHCO3��Na2CO3������Һ�� c(NaOH)��c(NaHCO3)��c(Na2CO3) |
| C�������£�c��NH4+����ȵ�4����Һ���٣�NH4��2SO4�ڣ�NH4��2Fe��SO4��2��NH4Cl �ܣ�NH4��2CO3���������ʵ���Ũ�ȴ�С��ϵ�ǣ���<��<��<�� |
| D��ij�¶�ʱˮ�����ӻ�����KW=10-13�������¶���pH=11��NaOH��ҺaL��pH=1��ϡ����bL��ϣ������û��ҺpH=2����a��b=2��9 |
C
�������������A�����н���Ԫ�ص�Ҳ�������ӣ���AlO2-�����������ӱ���ԭһ���õ��������ʣ���Fe3+����ԭ��Fe2+������B��pH��ȵ�NaOH��NaHCO3��Na2CO3������Һ��������Ũ����ͬ��NaOH��ȫ���룬�������Ũ����С������Խ��Խˮ�⣬̼���Ƶ�ˮ��̶ȴ���̼�����ƣ����̼�����Ƶ�Ũ�������C�������£�c��NH4+����ȵ�4����Һ���٣�NH4��2SO4 �ڣ�NH4��2Fe��SO4��2�ܣ�NH4��2CO3�к��е�NH4+�࣬������ǵ�Ũ����С����Ϊ�ڣ�NH4��2Fe��SO4��2����������ˮ�������ԣ�����NH4+ˮ�⣬�������С���ܣ�NH4��2CO3��̼�������ˮ���Լ��ԣ��ٽ�NH4+ˮ�⣬ˮ��̶ȴ�������������������NH4Cl�к��е�NH4+�٣��������Ũ�������ȷ��D��ij�¶�ʱˮ�����ӻ�����KW=10-13��pH=11��NaOH��Һ����������Ũ��Ϊ0.01mol/L��pH=1��ϡ���ᣬ�����ӵ�Ũ��Ϊ0.1mol/L���������pH=2�������ӵ�Ũ��Ϊ0.1mol/L��˵���������(0.1b-0.01a)/(a+b)=0.01����a��b=9��11������
���㣺����ˮ��ƽ�⡢pH�ļ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����������ˮ��Ӧ������������ԭ��Ӧ����
| A��NO2 | B��CaO | C��Cl2 | D��Na2O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��100 mL�����ʵ�����HBr��H2SO3�Ļ��Һ��ͨ��0��01 mol Cl2����һ��Br����ΪBr2(��֪Br2������H2SO3)��ԭ��Һ��HBr��H2SO3��Ũ�ȶ�����
| A��0��0075 mol��L��1 | B��0��008 mol��L��1 |
| C��0��075 mol��L��1 | D��0��08 mol��L��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
4.6gͭþ�Ͻ���ȫ�ܽ���100ml�ܶ�Ϊ1.40g/ml����������Ϊ63%��Ũ�����У��õ�4480mlNO2��336 ml N2O4�Ļ������(��״��)����Ӧ�����Һ�м���1.0mol/LNaOH��Һ������ǡ��ȫ������ʱ������˵������ȷ���� �� ��
| A���úϽ���ͭ��þ�����ʵ���֮����46:69 |
| B����Ũ������HNO3�����ʵ���Ũ����14.0mol/L |
| C����������8.51 g |
| D������ǡ����ȫ����ʱ������NaOH��Һ�������230mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ�ྻ������ձ��м���44.4gAl����Fe�ۻ���Ȼ�������������ᣬ�������������26.88L�������û�������500mL14 mol��L-1��HNO3�У������Ƿ����ۻ��������������壨��״���²ⶨ����ͼ��ʾ������HNO3�Ļ�ԭ����ΪNO��NO2����ô�����ϴ���һʱ�̿�ʼ����NO����?������Ũ��С��9mol/LΪϡHNO3��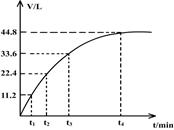
| A��t1 | B��t2 | C��t3 | D��t4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�Ƽ���������������۴������������η�ˮ��˼·�������������η�ˮ����ԣ�ʹ��pH��12��Ȼ��������������ۡ����裬�Ӷ�ʵ��Ԥ���ҵġ������жϴ������
| A����ˮ����ʱ������ת��ΪAl3+ | B����ˮ�����У��������α���ԭ |
| C�����������У�OHһ�����˷�Ӧ | D�����ۿ�����СӰ���ˮ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���б仯�У�������뻹ԭ�����ܷ�������
| A��FeCl2��FeCl3 | B��H2O��H2 | C��Al��NaAlO2 | D��CO2��C |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����·�Ӧ����H2S��H2O2=S����2H2O
��S��O2��SO2����SO2��Br2��H2O=HBr��H2SO4
�������ʵ�������ǿ���ж���ȷ����(����)
| A��H2O2>S��O2>SO2 | B��H2O2>O2��Br2>O2 |
| C��Br2>H2O2��SO2>S | D��Br2>H2O2��Br2>SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ΪԤ����H1N1����������,ͬѧ��ÿ���á�84������Һ(NaClO��Һ)����,����˵������ȷ���ǣ� ��
| A��NaClO��Һ������ԭ����ʹ�����ʱ��� |
| B��1 mol Cl2������NaOH��Һ��Ӧת��2 mol���� |
| C��NaClO��Һ��Ư��ԭ����Na2O2��ͬ,��SO2��ͬ |
| D����84������Һ�롰����顱(����)���ʹ�ÿ��ܻ�����ж������� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com