
【题目】“封管试验”具有简易、方便、节约、绿色等优点。观察下列四个“封管试验”(夹持装置未画出),判断下列说法正确的是( )
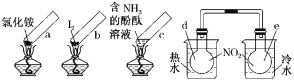
A.加热时,a上部聚集了固体NH4Cl,说明NH4Cl的热稳定性比较好
B.加热时,发现b中I2变为紫色蒸气,在上部又聚集为紫黑色的固体
C.加热时,c中溶液红色变深,冷却后又变浅
D.水浴时,d内气体颜色变浅,e内气体颜色加深
【答案】B
【解析】
A.加热时氯化铵分解生成氨气和氯化氢,在试管的顶部氨气和氯化氢又反应生成氯化铵,NH4Cl的热稳定性较差,故A错误;
B.加热碘升华变为紫色蒸气,在上部冷却聚集为紫黑色的碘固体,故B正确;
C.氨水显碱性使酚酞变红,加热时氨气逸出,溶液红色变浅,冷却后氨气又溶于水和水反应,溶液红色又变深,故C错误;
D.存在平衡:2NO2(g)![]() N2O4(g)△H= - 92.4kJ/ mol,正反应为放热反应,d浸泡在热水中,升高温度平衡向逆反应方向移动,二氧化氮浓度增大,d容器内气体颜色变深;e浸泡在冷水中,温度降低平衡向正反应移动,二氧化氮浓度降低,e容器内气体颜色变浅,故D错误;
N2O4(g)△H= - 92.4kJ/ mol,正反应为放热反应,d浸泡在热水中,升高温度平衡向逆反应方向移动,二氧化氮浓度增大,d容器内气体颜色变深;e浸泡在冷水中,温度降低平衡向正反应移动,二氧化氮浓度降低,e容器内气体颜色变浅,故D错误;
故答案:B。


科目:高中化学 来源: 题型:
【题目】某实验小组拟验证CO2与Na2O2反应的产物,现设计以下实验装置进行实验:
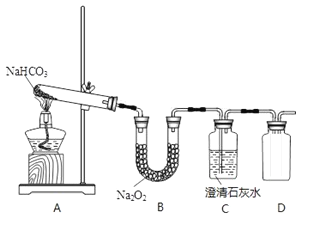
(1)写出装置A中反应的化学方程式________。
(2)写出装置B中反应的化学方程式________。
(3)拟用装置D收集气体产物,请将装置补充完整________。
(4)产物检验:检验气体产物的方法________。
(5)检验固体产物的方法:从B装置中取少量固体,溶于水配成溶液,________。
(6)有同学认为该实验装置存在明显缺陷,你认为该缺陷是什么________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.CO2催化加氢制甲醇是极具前景的资源化研究领域,主要反应有:
i.CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH1=-49.4kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-49.4kJ·mol-1
ii.CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH2=+41.2kJ·mol-1
CO(g)+H2O(g) ΔH2=+41.2kJ·mol-1
iii.CO(g)+2H2(g)![]() CH3OH(g) ΔH3
CH3OH(g) ΔH3
(1)ΔH3=___kJ·mol-1。
(2)已知反应i的速率方程为v正=k正x(CO2)·x3(H2),v逆=k逆·x(CH3OH)·x(H2O),k正、k逆均为速率常数且只与温度有关,x为物质的量分数。其物质的量分数平衡常数Kx=___(以k正、k逆表示)。
(3)5MPa时,往某密闭容器中按投料比n(H2):n(CO2)=3:1充入H2和CO2。反应达平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
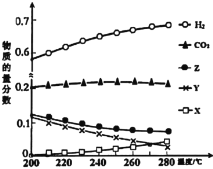
①图中Y代表___(填化学式)。
②250℃时反应ii的Kx___1(填“>”、“<”或“=”)
③下列措施中,一定无法提高甲醇产率的是___。
A.加入适量CO B.使用催化剂
C.循环利用原料气 D.升高温度
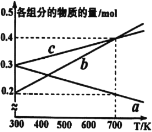
(4)在10MPa下将H2、CO按一定比例投料,平衡状态时各组分的物质的量与温度的关系如图所示。曲线b代表的物质为____(填化学式)。温度为700K时,该反应的平衡常数KP=___(MPa)-2(结果用分数表示)。
Ⅱ.在恒容容器中,使用某种催化剂对反应NO2(g)+SO2(g)![]() SO3(g)+NO(g) ΔH<0
SO3(g)+NO(g) ΔH<0
进行相关实验探究。改变投料比[n(SO2):n(NO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定SO2的平衡转化率[α(SO2)]实验结果如图所示。
已知:KR=16,KZ=![]() 。
。
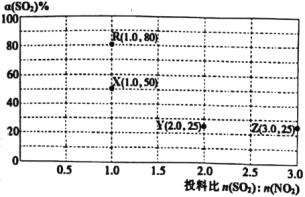
(5)如果要将图中R点的平衡状态改变为X点的平衡状态。应采取的措施是___。
(6)通过计算确定图中R、X、Y、Z四点中温度相等的点是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中所示的装置图能够达到实验目的是( )
A. 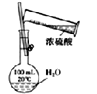 配制一定浓度的稀硫酸
配制一定浓度的稀硫酸
B. 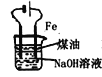 实验室制备Fe(OH)2
实验室制备Fe(OH)2
C. 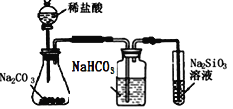 比较氯、碳、硅三种元素的非金属性强弱
比较氯、碳、硅三种元素的非金属性强弱
D.  加热熔融NaOH固体
加热熔融NaOH固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体X通入溶液A(如下图,尾气吸收装置略)中,实验现象能够支持结论的是
选项 | 气体X | 溶液A及反应现象 | 结论 |
A. | 乙醇与浓硫酸共热170℃产生的气体 | Br2的水溶液由橙黄色变为无色 | 乙烯与溴发生反应 |
B. | 电石与饱和食盐水反应产生的气体 | KMnO4酸性溶液紫色逐渐变浅 | 乙炔被高锰酸钾酸性溶液氧化 |
C. | 溴乙烷与氢氧化钠醇溶液共热生成的气体 | Br2的水溶液由橙黄色变为无色 | 乙烯与溴发生反应 |
D. | 碳酸钠固体与醋酸溶液反应产生的气体 | 苯酚钠溶液中出现白色沉淀 | 碳酸的酸性强于苯酚 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮、氧、氟、钙、铜等元素的化合物广泛存在于自然界,回答下列问题:
(1) 将乙炔(C2H2)通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。1个乙炔分子中σ键数目为___________,基态Cl原子的核外电子排布式为__________,[Cu(NH3)4] 2+中Cu 2+的配位数为___________。
(2)NF3是微电子工业中优良的等离子刻蚀气体。元素第一电离能N___________F(填“>”“<”或“=”), NF3中氮原子的杂化轨道类型为____________________,NF3分子的空间构型___________。
(3)氮的氧化物中与CO2互为等电子体的分子为___________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为反应2H2 (g)+O2(g)=2H2O(g)的能量变化示意图。下列说法正确的是( )
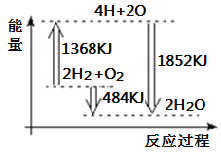
A. 由H、O原子形成2mol H2O(g),共吸收1852 kJ能量
B. 拆开2molH2 (g)和1mol O2 (g)中的化学键成为H、O原子,共放出1368kJ能量
C. 2molH2 (g)和1molO2 (g)反应生成2mol H2O(g),共放出484 kJ能量
D. 2molH2 (g)和1molO2 (g)反应生成2molH2O(l),共吸收484 kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,下列叙述中正确的是( )
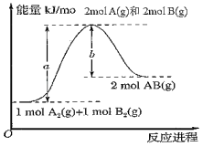
A.每生成2molAB(g)吸收的热量为(a﹣b)kJ
B.该反应是放热反应
C.1molA2(g)和1molB2(g)具有的总能量大于2molAB(g)具有的总能量
D.断裂1molA﹣A键和1molB﹣B键,放出akJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在指定环境中,下列各组离子一定可以大量共存的是
A.某无色溶液:Fe2+、NO![]() 、SO
、SO![]() 、Na+
、Na+
B.使紫色石蕊试液变红的溶液:NH![]() 、Mg2+、Cl-、K+
、Mg2+、Cl-、K+
C.加入铝粉放出氢气的溶液:Na+、Cl-、NH![]() 、NO3-
、NO3-
D.使无色酚酞试液显红色的溶液:S2-、K+、HCO![]() 、Al3+
、Al3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com