
����Ŀ��������ܰ�����������������Ķ�������֮һ���������������Ƹò�����Чҩ�����Ҫ�ϳɹ���·�����£� 
��1��A������Ϊ �� �������µķ���ʽΪ ��
��2���л���B����C�Ļ�ѧ����ʽΪ��ע��������
��3�����з�����������������ĸ����
a���л���D�ɷ���ˮ�ⷴӦ
b�����E�������
c�����F��������
d���л���G������̼ԭ��һ����ͬһƽ����
��4��F����G�������õ���HCOOH���ж��ص����ʣ�д��HCOOH���������Ƶ�������ͭ��Ӧ�Ļ�ѧ����ʽ�� ��
��5���л���B�ж���ͬ���칹�壬д�����������������л���B�Ľṹ��ʽ�� ��
a���ܷ���������Ӧ
b�������ϵ�һȡ���������֣�
���𰸡�
��1��4���������C12H19N3O
��2��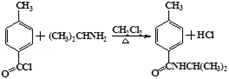
��3��ac
��4��HCHO+4Cu��OH��2 ![]() CO2��+2Cu2O��+5H2O
CO2��+2Cu2O��+5H2O
��5��![]()
���������⣺��1��A���й������Ȼ���Ӧ�����Ȼ�������̼Ϊ���������ϵ�Cԭ��ʼ��ţ���λ��4��C����������Ϊ��4������������ݱ������µĽṹ��ʽ��֪�������ʽΪ��C12H19N3O��
���Դ��ǣ�4���������C12H19N3O����2���ڶ��ȼ��顢���������£��л���B�е���ԭ�ӱ���CH3��2CHNHNH2�еĩ�NHNHCH��CH3��2ȡ�������л���C��HCl����Ӧ����ʽΪ�� 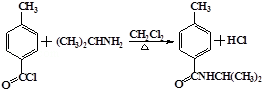 ��
��
���Դ��ǣ� 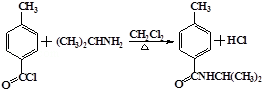 ����3��a���л���D�к�����ԭ�ӡ��ļ����ɷ���ˮ�ⷴӦ����a��ȷ��
����3��a���л���D�к�����ԭ�ӡ��ļ����ɷ���ˮ�ⷴӦ����a��ȷ��
b���л���E���������������ļ�����b����
c���л���FΪ���࣬ˮ������ԣ���c��ȷ��
d���л���G�д��ڰ������������ṹ������̼ԭ�Ӳ�һ����ͬһƽ���ϣ���d����
��ѡ��ac����4��HCOOH���������Ƶ�������ͭ��Ӧ���ɶ�����̼��������ͭ��ˮ����Ӧ����ʽΪ��HCHO+4Cu��OH��2 ![]() CO2��+2Cu2O��+5H2O��
CO2��+2Cu2O��+5H2O��
���Դ��ǣ�HCHO+4Cu��OH��2 ![]() CO2��+2Cu2O��+5H2O����5���л���B�Ľṹ��ʽΪ��
CO2��+2Cu2O��+5H2O����5���л���B�Ľṹ��ʽΪ�� ![]() ����ͬ���칹���ܷ���������Ӧ��˵������ȩ���������ϵ�һȡ����ֻ�����֣�˵����������������ͬȡ������λ�����λ�ã�����ȡ����Ϊ��CHO�ͩ�CH2Cl��CH2CHO�ͩ�Cl���������������л���B��ͬ���칹��Ľṹ��ʽΪ
����ͬ���칹���ܷ���������Ӧ��˵������ȩ���������ϵ�һȡ����ֻ�����֣�˵����������������ͬȡ������λ�����λ�ã�����ȡ����Ϊ��CHO�ͩ�CH2Cl��CH2CHO�ͩ�Cl���������������л���B��ͬ���칹��Ľṹ��ʽΪ ![]() ��
��
���Դ��ǣ� ![]() ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��aXn����bYm��Ϊ������Ԫ�ص����ӣ����ǵĵ��Ӳ�ṹ��ͬ�������жϴ������(����)
A. ԭ�Ӱ뾶X��Y B. ���Ӱ뾶Xn����Ym��
C. a��n��b��m D. X���⻯��Ļ�ѧʽΪHnX
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ƾ��壨Na2S2O35H2O�����������մ��ֳơ�����������֪Na2S2O35H2O����ɫ�����壬������ˮ���������Ҵ��������ȡ������ֽ⣬�ڿ������ױ�������ij��ȤС�����Ʊ���������ƾ��壨Na2S2O35H2O������Ӧԭ��Ϊ2Na2S+Na2CO3+4SO2�T3Na2S2O3+CO2 �� 
��1����ͼ1���Ʊ�Na2S2O3
������b������ �� d��ʢ�ŵ��Լ��� ��
��b���Ʊ�SO2 �� ��Ӧ�Ļ�ѧ����ʽ ��
�۷�Ӧ��ʼ��Ҫ����SO2�������ʣ����Բ�ȡ�Ĵ�ʩ����д��һ�����ɣ���
��2������Na2S2O3���ⶨ������ͼ2��
��I��Ϊ�˼��ٲ�Ʒ��ʧ��������ʱ�� �� �������ǹ��ˡ�ϴ�ӡ��������ϴ�Ӳ���ʱ����ϴ�Ӽ����������ʱ��װ����ͼ3��ʾ����ͨ��H2��Ŀ���� ��
��II���ƵõĴ־��������������������ʣ�Ϊ�˲ⶨ�ֲ�Ʒ��Na2S2O35H2O�ĺ�����������������������KMnO4��Һ�ζ��ķ���������ֲ�Ʒ�е�����������KMnO4��Һ����Ӧ������ȡ1.50g�ֲ�Ʒ����ˮ����0.20molL��1KMnO4��Һ��������ϡ�����ữ���ζ�������Һ��S2O32��ȫ��������ʱ�����ĸ��������Һ���40.00mL����5S2O32��+8MnO4��+14H+�T8Mn2++10SO42��+7H2O��
��KMnO4��Һ���������ʽ����ʽ�����ζ����У�
���� �� ��ﵽ�ζ��յ㣮
�۲�Ʒ��Na2S2O35H2O����������Ϊ������С�����һλ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������
��1�����ݷ��������������ſ�Ԥ���л�����������ʣ� �����л��������ܷ�����ȥ��Ӧ����������ĸ����
a��CH3OH �� b��CH3CH2Cl ��c��CH3CH2OH d�� 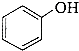
�����л������У��������ױ�������������������ĸ����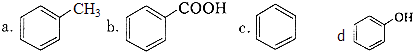
��2���ױ��� ![]() ����һ����Ҫ���л�����ԭ�ϣ� �ټױ�������һ����ƽ���̼ԭ��������
����һ����Ҫ���л�����ԭ�ϣ� �ټױ�������һ����ƽ���̼ԭ��������
�ڼױ������ϵ�һ��������֣���д������һ�ֵĽṹ��ʽ ��
�۳�ȥ���л��е������ױ�����ѡ�õ��Լ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪̼�����ֳ�����ͬλ��12C��13C����Ҳ�г���������ͬλ��16O��17O��18O������5�����ӹ��ɵĶ�����̼�����У�����Է���������������
A. 6��B. 10��C. 11��D. 12��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25�桢101kPa�£�2g����ȼ������Һ̬ˮ���ų�285.8kJ��������ʾ�÷�Ӧ���Ȼ�ѧ����ʽ��ȷ���ǣ� ��
A.2H2��g��+O2��g���T2H2O��1����H=��285.8kJ/mol
B.2H2��g��+O2��g���T2H2O��1����H=+571.6kJ/mol
C.2H2��g��+O2��g���T2H2O��g����H=��571.6kJ/mol
D.H2��g��+ ![]() O2��g���TH2O��1����H=��285.8kJ/mol
O2��g���TH2O��1����H=��285.8kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������
��1����ҵ����ȡ�������Ҫ����ͼ��ͼ1�� 
��I����ҵ�ϳɰ���ԭ����N2��H2 �� װ��A��������������N2�ɴӿ����з���������������Ƚ����� �� Ȼ�����ɵõ���H2����ˮ����Ȼ��Ϊԭ���ڴ��������¸�����ȡ���仯ѧ����ʽΪ ��
��II����ԭ�����Ʊ������л��е�CO�Դ����ж������ã�����ȥԭ�����е�CO����ͨ�����·�Ӧ��CO��g��+H2O��g���TCO2��g��+H2��g����ʵ�֣���֪1100Kʱ�÷�Ӧ��ƽ�ⳣ��K=0.64����ҪʹCO��ת���ʳ���80%������ʼ����c��H2O����c��CO�������� ��
��2������ʯ��������ȥ���Ṥҵ��β������NO��NO2�������ܾ���β�������ܻ��Ӧ�ù㷺��Ca��NO2��2 �� �䲿�ֹ���������ͼ2����֪NO��NO2��1��1ͨ���Һ�������������Σ� 
��I�����������в�������Һ�����Ӵ����գ�β�������������룬ʯ����������������ܣ�����Ŀ������������ѭ��ʹ�ã���������Ҫ�ɷ������ѧʽ����
��II���ù��������NO ��NO2 ���ʵ���֮�Ƚӽ�1��1����n��NO����n��NO2����1��1����ᵼ������n��NO����n��NO2����1��1����ᵼ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ȡ������װ����ͼ�� 
��1��ʵ������ȡ�����Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ��=MnCl2++2H2O��������
��2��ʵ����ͨ���ñ���ʳ��ˮ�������� �� Bƿʢװ���Լ���
��3��Cװ������������ �� ��Ӧ�Ļ�ѧ����ʽΪ
��4�����������Ƿ�й©��ʪ����ֽ����й©��ֽ��ɫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����������Ӧ����
A. ��������ˮ��ӦB. �����ڿ�����ȼ��
C. ����������������Һ��ӦD. ʯ��ʯ���·ֽ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com