
����Ŀ������������
��1����ҵ����ȡ�������Ҫ����ͼ��ͼ1�� 
��I����ҵ�ϳɰ���ԭ����N2��H2 �� װ��A��������������N2�ɴӿ����з���������������Ƚ����� �� Ȼ�����ɵõ���H2����ˮ����Ȼ��Ϊԭ���ڴ��������¸�����ȡ���仯ѧ����ʽΪ ��
��II����ԭ�����Ʊ������л��е�CO�Դ����ж������ã�����ȥԭ�����е�CO����ͨ�����·�Ӧ��CO��g��+H2O��g���TCO2��g��+H2��g����ʵ�֣���֪1100Kʱ�÷�Ӧ��ƽ�ⳣ��K=0.64����ҪʹCO��ת���ʳ���80%������ʼ����c��H2O����c��CO�������� ��
��2������ʯ��������ȥ���Ṥҵ��β������NO��NO2�������ܾ���β�������ܻ��Ӧ�ù㷺��Ca��NO2��2 �� �䲿�ֹ���������ͼ2����֪NO��NO2��1��1ͨ���Һ�������������Σ� 
��I�����������в�������Һ�����Ӵ����գ�β�������������룬ʯ����������������ܣ�����Ŀ������������ѭ��ʹ�ã���������Ҫ�ɷ������ѧʽ����
��II���ù��������NO ��NO2 ���ʵ���֮�Ƚӽ�1��1����n��NO����n��NO2����1��1����ᵼ������n��NO����n��NO2����1��1����ᵼ�� ��
���𰸡�
��1���ϳ�����Һ������������N2�ķе����������CH4+H2O��g�� ![]() CO+3H2��5.8
CO+3H2��5.8
��2��ʹβ���е�NO��NO2 ��������գ�Ca��OH��2���ŷ�������NO �������ߣ���ƷCa��NO2��2 ��Ca��NO3��2 ��������
���������⣺��1����I��N2��H2�ϳɰ����ںϳ����н��еģ�����N2���Ʊ����ǽ�����Һ����Ȼ�����������߿���N2�е���������Ƶã���Ӧ�����������Ѿ�������ֻ��д���������ƽ��Ӧ����ʽΪCH4+H2O��g�� ![]() CO+3H2 �� ���Դ��ǣ��ϳ�����Һ������������N2�ķе����������CH4+H2O��g��
CO+3H2 �� ���Դ��ǣ��ϳ�����Һ������������N2�ķе����������CH4+H2O��g�� ![]() CO+3H2����II����c��H2O����c��CO��ΪX�������ʼc��H2O��ΪX����c��CO��Ϊ����CO��g��+H2O��g���TCO2��g��+H2��g����֪��ҪʹCOת���ʴﵽ0.8����ƽ��ʱ�����ʵ�Ũ��Ϊc��CO��=0.2�� c��H2O��=X��0.8��c��CO2��=0.8��c��H2��=0.8����ƽ�ⳣ��K=
CO+3H2����II����c��H2O����c��CO��ΪX�������ʼc��H2O��ΪX����c��CO��Ϊ����CO��g��+H2O��g���TCO2��g��+H2��g����֪��ҪʹCOת���ʴﵽ0.8����ƽ��ʱ�����ʵ�Ũ��Ϊc��CO��=0.2�� c��H2O��=X��0.8��c��CO2��=0.8��c��H2��=0.8����ƽ�ⳣ��K= ![]() ���ɽ��X=5.8��
���ɽ��X=5.8��
���Դ��ǣ�5.8����2����I��ʹ���������ĺô������ڣ�����β��������Һ֮��Ӵ���������Ӷ����β���������ʣ������пɻ������õ��ǹ�����ʯ���飬Ҳ����Ca��OH��2 ��
���Դ��ǣ�ʹβ���е�NO��NO2 ��������գ�Ca��OH��2����II�����Ṥҵβ��NO��NO2һ���ü�Һ���գ�����ӦΪ��NO+NO2+2OH��=2NO2��+H2O������ӦΪ��2NO2+2OH��=NO2��+NO3��+H2O����n��NO����n��NO2����1��1����һ�������������ŷ�������NO�������ߣ���n��NO����n��NO2����1��1���������������������������ʯ���鷴Ӧ����Ca��NO3��2 ��
���Դ��ǣ��ŷ�������NO�������ߣ���ƷCa��NO2��2��Ca��NO3��2�������ߣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ�����Цġ��á�������ͬ�������壬���־����ڲ�ͬ�¶����ܷ���ת��������˵����ȷ���ǣ� �� 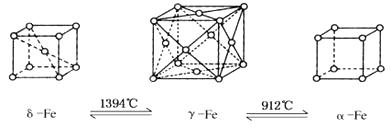
A.��Fe��������ÿ����ԭ�Ӿ���������������ԭ����6��
B.��Fe��������ÿ����ԭ�Ӿ���������������ԭ����6��
C.�������ȵ�1 500��ֱ�����ȴ�ͻ�����ȴ���õ��ľ���������ͬ
D.����ͬ���������������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ǻ�����ѧ��Ӧ���ʿ�������Ҫ���ݣ����ж������������˵��������ȷ���ǣ� ��
A. �����֮�����ײ��һ��������Ч��ײ
B. �����¶ȣ���ʹ��λ����ڻ�������࣬��Ӧ���ʼӿ�
C. ����������μӵķ�Ӧ����ѹǿ����ʹ��λ����ڻ���Ӱٷ������ӣ���Ӧ���ʼӿ�
D. �����ܽ��ͷ�Ӧ�Ļ�ܣ�ʹ��λ����ڻ���Ӱٷ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ܰ�����������������Ķ�������֮һ���������������Ƹò�����Чҩ�����Ҫ�ϳɹ���·�����£� 
��1��A������Ϊ �� �������µķ���ʽΪ ��
��2���л���B����C�Ļ�ѧ����ʽΪ��ע��������
��3�����з�����������������ĸ����
a���л���D�ɷ���ˮ�ⷴӦ
b�����E�������
c�����F��������
d���л���G������̼ԭ��һ����ͬһƽ����
��4��F����G�������õ���HCOOH���ж��ص����ʣ�д��HCOOH���������Ƶ�������ͭ��Ӧ�Ļ�ѧ����ʽ�� ��
��5���л���B�ж���ͬ���칹�壬д�����������������л���B�Ľṹ��ʽ�� ��
a���ܷ���������Ӧ
b�������ϵ�һȡ���������֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڿ���������˷�Ӧ��2H2S��O2��2S����2 H2O�����в���ȷ������ ��
A. ��ԭ����H2O> H2S B. �����û���Ӧ
C. ��������O2> S D. ������H2S> H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ������ĺ���������XΪ��Ҫԭ�������ɽ�������PCL{ ![]() }����ȼ������˫��A���ϳ���·���£�
}����ȼ������˫��A���ϳ���·���£� 
��֪����X�������ܶ�����ͬ������H2��47������FeCl3��Һ����ɫ��CΪ ![]()
�� ![]()
![]()
![]()
��RCOCH2R�� ![]() RCOOCH2R��
RCOOCH2R��
��ش��������⣺
��1��X�ķ���ʽΪ��B�������� ��
��2��B��C����Ҫ�ķ�Ӧ�Լ��������� �� C��D�ķ�Ӧ������ ��
��3��д��X��Y�Ļ�ѧ����ʽ�� ��
��4��0.5mol����˫��A��һ����������������NaOH��Һ��Ӧ���������molNaOH��
��5����������������D��ͬ���칹�����֣������ǿռ��칹����
�ٺ��������������ֹ����� ����ʹ���CCl4��Һ��ɫ ���ܷ���������Ӧ
��6����֪��ϩ��ֱ���Ʊ������������·���Ϊ��
2CH3![]() =CH2+2ROH+2CO+O2
=CH2+2ROH+2CO+O2 ![]() 2CH3
2CH3![]() =CHCOOR+2H2O
=CHCOOR+2H2O
������ϩΪ�л�ԭ�ϣ�����ͷ�Ӧ������ѡ���ϳɾۺ���Ϳ�� ![]() ��д���ϳɸ�Ϳ�ϵķ�Ӧ����ͼ�� ��
��д���ϳɸ�Ϳ�ϵķ�Ӧ����ͼ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ν���Է�����ָ�ڷ����У���һ��̼ԭ�������б˴˻�����ͬ���ĸ�ԭ�ӻ�ԭ����ʱ���ƴ˷���Ϊ���Է��ӣ�����̼ԭ��Ϊ����̼ԭ�ӣ�������һ������̼ԭ�ӵ�����һ�����й�ѧ���ԣ����磬�л������ ![]() ���й�ѧ���ԣ�����л�������ֱ������·�Ӧ�����ɵ��л������й�ѧ���Ե��ǣ� ��
���й�ѧ���ԣ�����л�������ֱ������·�Ӧ�����ɵ��л������й�ѧ���Ե��ǣ� ��
A.�����ᷢ��������Ӧ
B.��NaOHˮ��Һ����
C.��������Һ����
D.�ڴ�������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3.2 gCuͶ�뵽һ��Ũ�ȵ�HNO3��Һ�У�ǡ����ȫ��Ӧ������NO2��NO�Ļ�����干 0.08 mol����ԭ��Һ��HNO3�����ʵ���Ϊ�� ��
A.0.34 molB.0.38 molC.0.28 molD.0.18 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A��![]() �����ɻ����龭������Ӧ�ϳɣ�
�����ɻ����龭������Ӧ�ϳɣ�
������˵��������ǣ�������
A.��Ӧ1�����Լ�������
B.��Ӧ3���õ��Լ���������ͭ
C.��Ӧ1Ϊȡ����Ӧ����Ӧ2Ϊ��ȥ��Ӧ
D.A��ͨ���ӳɷ�Ӧ�ϳ�Y
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com