
����Ŀ����ϩ�IJ����Ǻ���һ������ʯ�ͻ���ˮƽ����Ҫ��־����ҵ�ϳ��ö����ѽ��Ʊ���ϩ��
����Ӧ��C4H10(g��������)![]() C2H4(g)+C2H6(g) ��H1
C2H4(g)+C2H6(g) ��H1
����Ӧ��C4H10(g��������)![]() CH4(g)+C3H6(g) ��H2
CH4(g)+C3H6(g) ��H2
�ش��������⣺
��1����ѧ�ϣ����ȶ����ʵ�������Ϊ0����Ԫ�صĵ��ʻ��ϳɵ�һ������ʱ�ķ�Ӧ�Ƚиû�����������ȣ������ȿɱ�ʾ����������������±�Ϊ25�桢101kPa�¶����л���������ȣ�
���� | ���� | ���� | ��ϩ | ��ϩ | ������ | �춡�� |
������/kJ��mol-1 | -75 | -85 | 52 | 20 | -125 | -132 |
��������Ӧ�У���H1=___kJ��mol-1��
�������Ը���Ӧ����ͬ�����²����춡���ѽ���ȡһ��������ϩ�����ܺıȲ���������__����������������������
��2��һ���¶��£��ں�ѹ�ܱ�������Ͷ��һ���������鷢����Ӧ������ϩ��
��������������÷�Ӧ�ﵽƽ��״̬����___������ţ���
a.�����ܶȱ��ֲ���
b.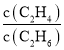 ���ֲ���
���ֲ���
c.��H����
d.������ֽ����ʺ����������������
��Ϊ��ͬʱ��߷�Ӧ���ʺ�ת���ʣ��ɲ��õĴ�ʩ��__��
��3�����ܱ������г��붡�飬��һ��������Ũ�ȡ�������ѹǿ�ȣ��·�����Ӧ�������ϩ�������¶ȹ�ϵ��ͼ��ʾ��
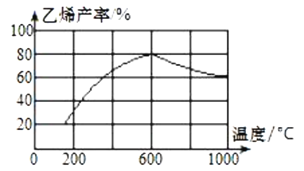
�¶ȸ���600��ʱ�������¶����ߣ���ϩ���ʽ��ͣ����ܵ�ԭ����__��
��4����һ���¶�����1L�����ܱ������г���2mol�����飬������ѹǿΪP0����Ӧ������ϩ�����飬����10min�ﵽƽ��״̬�����¶����ø���ֵķ�ѹ��ʾ��ƽ�ⳣ��K(p)=0.5P0��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������������0��10min����ϩ����������v(C2H4)Ϊ__mol��L-1��
���𰸡�+92 �� ad �����¶� �������Խ��ͻ������� 0.1
��������
(1)�ٷ�Ӧ����ʽ���ʱ�=�������������-��Ӧ��������ȣ����Ը÷�Ӧ���ʱ�=(52-85+125)kJ/mol=+92kJ/mol���������Ȼ�ѧ����ʽΪC4H10(g��������)C2H4(g)+C2H6(g)��H=+92kJmol-1��
�������춡��������Ƚϵͣ����ȶ���������Ӧ������ܺıȸߣ�
(2)��a. ��Ӧǰ���������������䣬��������ѹǿ���䣬�÷�ӦΪ��������ķ�Ӧ�����������������䣬����Ӧ�����������ܶȻ���ƽ���ƶ����仯�����Ը����ܶ��ж�ƽ��״̬����a��ȷ��
b. ��ʼʱֻͨ�������飬����![]() һֱ������ڼ�����֮�ȣ�����
һֱ������ڼ�����֮�ȣ�����![]() ����ʱ����˵���ﵽƽ��״̬����b����
����ʱ����˵���ﵽƽ��״̬����b����
c. �ʱ�������������ȣ����Ƿ�ﵽƽ��״̬�أ���c����
d. ������ֽ���������������������ȣ������淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬����d��ȷ��
��ѡ��ad��
�ڸ÷�Ӧ������Ӧ�����ȷ�Ӧ��Ϊ����߷�Ӧ���ʺͷ�Ӧ���ת���ʣ��ɲ��յĴ�ʩ�������¶ȣ�
(3)�����������¶�Ӱ�죬�л���ѧ��Ӧ�и���Ӧ�϶࣬�����¶����ߣ���ϩ���ʽ��ͣ����ܵ�ԭ���Ǵ������Խ��ͣ����������ࣻ
(4)��ƽ��ʱ���ɵ���ϩΪxmol��������ʽ���£�
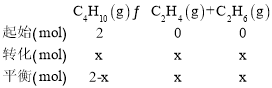
��ƽ��ʱ��ϵ�����干(2-x+x+x)mol=(2+x)mol������ϵ��ѹǿΪ![]() ����P(C4H10)=
����P(C4H10)=![]() ��P(C2H4) =P(C2H6)=
��P(C2H4) =P(C2H6)=![]() ��K(P)=
��K(P)=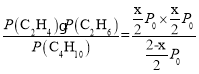 =0.5P0�����x=1mol���������Ϊ1L������v(C2H4)=
=0.5P0�����x=1mol���������Ϊ1L������v(C2H4)=![]() =0.1mol/Lmin-1��
=0.1mol/Lmin-1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.��ͼ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ�ã������װ�ûش����⣺
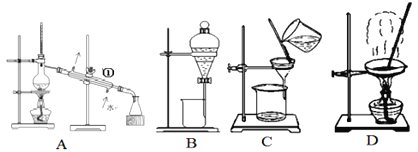
��1���ӵ�ˮ�з����I2��ѡ��װ��_______�������װ��ͼ����ĸ�����÷��뷽��������Ϊ_______��
��2��A��װ�âٵ�������________����װ��ͨ����ѡ�����������ܺ����������ܵ�ԭ���ǣ�_______�����в�������ͼA����ͬһԭ������______����ѡ����ţ�
��3������װ��C�Թ������õĹ���ϴ�ӵľ�����������ǣ�________��
��.�����Լ�ƿ��ǩ�ϵ����ݣ�
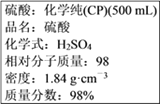
��1��ij��ѧ��ȤС������������ʵ�ʵ��̽��ʱ����Ҫ240 mL 4.6 mol��L��1��ϡ���ᣬ������ϡ����ʱ��Ҫȡ________mL�ĸ��������ʱ��ѡ�õ�������Ҫ����Ͳ���ձ�����������__________��__________���ں�������д��ȱ���������ƣ���
��2�����ƹ����У����в�����ʹ���Ƶ�ϡ������ҺŨ��ƫ�ߵ���_______������ţ���
����ȡŨ�������Ͳ������ˮϴ��2��3�Σ�����ϴ��Һת������ƿ
������ƿʹ��ʱδ����
���ܽ��δ����ȴ����Һ������
�ܶ���ʱ��С������������ˮ�ε�ƿ��
�ݶ��ݺ���ҡ�ȡ����ã�����Һ����ڿ̶��ߣ��ټ�����ˮ�����̶���
��.Ϊ�ⶨij��������Na2O��Na2O2��Ʒ�Ĵ��ȣ�ʵ��С��������·���������Ʒ�������̼��Ӧ��ͨ���ⶨ��Ӧ����������������������Ʒ��Na2O2�ĺ�����
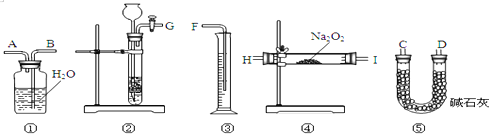
��1����ͼ����ɸ�ʵ������õ���ʵ��װ�ã����ݴ�ʵ�鷽����ʵ����ʹ�����������Ӵ�����______������д������ţ����ظ�ʹ�á���
��2��װ�â٢ݵ����÷ֱ��ǣ���___________��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
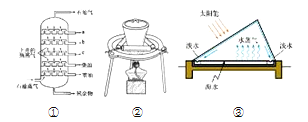
����Ŀ��Ϊ�˼������ˮ��IJ���������ʵ�鷽����
![]()
��ش��������⣺
��1���Լ�1Ϊ20%��H2SO4��Һ����������_________��
��2���Լ�2Ϊ_________����������_________��ʹ����ˮ������ʵ�����˳�����У�������Ӧ�����ӷ���ʽΪ��_________��
��3����Ӧ�ٵĻ�ѧ����ʽΪ_________��
��4��Ϊ�������Һ�Ƿ�����ȫˮ�⣬ȡ����ˮ��Һ���Թ��У������ˮ����֤������δ��ȫˮ���������_________��
��5�����ʵ�������û�м����Լ�2��ֱ�Ӽ����Լ�3���ܷ�ʵ��ʵ��Ŀ��_________���������������������������ܣ���ԭ����_________����ĸ�����ʩ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.1mol/L��Al2��SO4��3��Һ�еμ�1.0mol/L��NaOH��Һ���μӹ�������ҺpH��NaOH��Һ����仯��������ͼ��ʾ�����з�������ȷ����
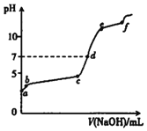
A.a��pH<7��ԭ��Al3++3H2OAl(OH)3+3H+
B.bc�η�������Ҫ��Ӧ��Al3++3OH=Al(OH)3
C.ef�η�������Ҫ��Ӧ��Al(OH)3+OH=AlO2+2H2O
D.d�㣬��Һ�д������ڵ�������Na+��AlO2��SO42
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(H3AsO3)����Һ�д��ڶ�������̬�����������ʵ�����������ҺpH��ϵ����ͼ��ʾ������˵���У�����ȷ����
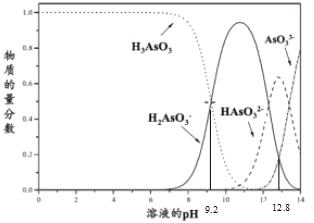
A. K3AsO3��Һ�е�ˮ�ⷽ��ʽ��AsO33-+H2O![]() HAsO32-+OH-
HAsO32-+OH-
B. pH=12.8ʱ��c(HAsO32-) >c(H2AsO3-)=c(AsO33-)
C. pH = 12ʱ����Һ��c(H2AsO3-) + 2c(HAsO32-) + 3c(AsO33-) + c(OH-) = c(H+)
D. pH=9.2ʱ����H2AsO3-��H3AsO3�Ļ����Һ�У�c(H2AsO3-):c(H3AsO3)=1:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϩ��![]() ���������������ϵ���Ҫ���壬��ͨ���ұ��������Ƶã�
���������������ϵ���Ҫ���壬��ͨ���ұ��������Ƶã�
![]() ��g��
��g��![]()
![]() ��g��+H2��g�� ��H
��g��+H2��g�� ��H
(1)��֪��
��ѧ�� | C-H | C-C | C=C | H-H |
����/kJ/mol | 412 | 348 | 612 | 436 |
����������Ӧ�ġ�H��________ kJ��mol��1��
(2)500��ʱ���ں����ܱ������У�����a mol�ұ�����Ӧ�ﵽƽ��������������ѹǿΪP�����ٳ���bmol���ұ������´ﵽƽ��������������ѹǿΪ2P����a_______b������� ��������=�������ұ���ת���ʽ�________������� ����С�����䡱����
(3)��ҵ�ϣ�ͨ�����ұ���EB�������в���N2��ԭ�������ұ���N2�����ʵ���֮��Ϊ1�U10��N2�����뷴Ӧ�������Ʒ�Ӧ�¶�600�棬��������ϵ��ѹΪ0.1Mpa����������½��з�Ӧ���ڲ�ͬ��Ӧ�¶��£��ұ���ƽ��ת���ʺ�ij���������±���ϩ��ѡ���ԣ�ָ����H2����IJ����б���ϩ�����ʵ���������ʾ��ͼ���£�
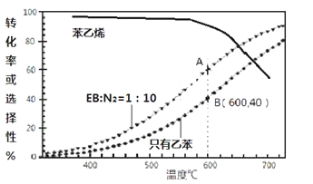
��A��B�����Ӧ������Ӧ���ʽϴ����________��
�ڲ���N2������ұ���ƽ��ת���ʣ�����˵������ʵ___________________________��
����ƽ���ѹ����ƽ��Ũ�ȼ���600��ʱ��ƽ�ⳣ��Kp=________����������λ��Ч���֣���ѹ=��ѹ�����ʵ���������
�ܿ��Ʒ�Ӧ�¶�Ϊ600���������___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CH4 ��һ����ࡢ��Ч�����������Ļ������ܵ�ȼ�ϣ���ȼ����Ϊ890.3kJ��mol-1����������Ϊȼ�ϵ�ص�ȼ�ϡ�
��1��д������ȼ�յ��Ȼ�ѧ����ʽ��____________________________________________��
��2���Լ��顢����������������ҺΪԭ�ϣ����Ե缫Ϊ�缫���Թ���ȼ�ϵ�ء��õ�صĸ�����ӦʽΪ____
��3���ã�2���е�ȼ�ϵ��Ϊ��Դ����ʯīΪ�缫���500mL���з�̪��NaCl��Һ��װ����ͼ��ʾ��
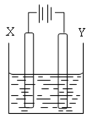
����д�������������������۲쵽������____________________��
����ȼ�ϵ������2.8L O2����״���£�ʱ�������ʱNaCl��Һ��pH=__________ ��������Һ��������䣬����ȫ������Һ���ݳ�������Y��ͨ���ĵ��ӵ����ʵ���Ϊ��_______________________��
�����֮��Ҫʹ��Һ�ָ�ԭ״��Ӧ������Һ�м������� _________�������ƣ�����Һ��Cl�D���� ____________��������X������Y������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ԭ�����͵��ǣ� ��
A.H2��I2(g)��������ѹ����ɫ����B.��������������SO2ת��ΪSO3
C.����ˮ�м�ʯ��ʯ����ߴ������Ũ��D.����������ˮ����ˮ��ɫ��dz
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��װ�ý�����Ӧʵ�飬�ܴﵽʵ��Ŀ�ĵ���
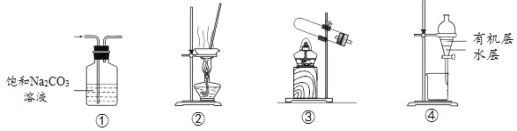
A.�â�װ�ó�ȥCO2�к��е�����SO2
B.�â�װ�����ɱ���AlCl3��Һ�Ʊ�AlCl3����
C.�â�װ�ü���NH4Cl������ȡNH3
D.�â�װ�÷�������������ˮ�Ļ��Һ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com