
����Ŀ��TiO2��TiCl4��Ϊ��Ҫ�Ļ���ԭ�ϣ���֪��
��.TiCl4(g)+O2(g)![]() TiO2(s)+2Cl2(g) ��H=-175.4kJ/mol
TiO2(s)+2Cl2(g) ��H=-175.4kJ/mol
��.2C(s)+O2(g)![]() 2CO(g) ��H=-220.9kJ/mol
2CO(g) ��H=-220.9kJ/mol
��ش��������⣺
��1��TiCl4(g)+2CO(g)![]() TiO2(s)+2C(s)+2Cl2(g)����H=___kJ/mol��
TiO2(s)+2C(s)+2Cl2(g)����H=___kJ/mol��
��2��t��ʱ����10L�����ܱ������г���1molTiCl4��2molO2��������ӦI��4min�ﵽƽ��ʱ���TiO2�����ʵ���Ϊ0.2mol��
�ٷ�Ӧ0~4minĩ��ƽ������v(Cl2)=_�����¶���K=_���÷�����ʾ����O2��ƽ��ת����=__��
�����д�ʩ�����ܼӿ�����Ӧ���ʣ���������O2��ƽ��ת���ʵ���_��
A.�����������
B.�������
C.���������TiO2
D.����O2��Ũ��
E.�����¶�
F.���Ϸ�����������
��t��ʱ����10L�����ܱ������г���3molTiCl4��һ������O2��������ӦI�����������ƽ��ת���ʣ�a%������ʼ�����ʵ���֮�ȣ�TiCl4/O2���Ĺ�ϵ��ͼ1��ʾ���ܱ�ʾO2��ƽ��ת���ʵ�����Ϊ___(����L1������L2��)��M�������Ϊ___(�������������ʾ)��
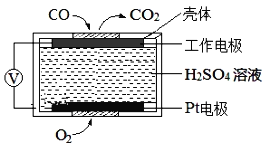
��3��CO���ж����壬�ⶨ������CO�������õķ���֮һ�ǵ绯ѧ������������������CO�������Ĺ���ԭ����ͼ2��ʾ�������缫�ķ�ӦʽΪ___��Ϊ���ٶԻ�����ɵ�Ӱ�죬��CO��H2�����Ʊ��״�(CH3OH)���Լ״�Ϊȼ�ϣ�����Ϊ��������KOH��ҺΪ�������Һ�����Ƴ�ȼ�ϵ�أ��缫����Ϊ���Ե缫�����������Һ��KOH�����ʵ���Ϊ0.8mol������0.5mol�״����뷴Ӧʱ���������Һ�����ʵ���Ҫ�ɷ���___(д��ѧʽ)��
���𰸡�+45.5 0.01mol/(Lmin) ![]() 10% F L1 (1��
10% F L1 (1��![]() ) CO��2e-��H2O=CO2��2H+ K2CO3��KHCO3
) CO��2e-��H2O=CO2��2H+ K2CO3��KHCO3
��������
(1)��֪��. TiCl4(g)+O2(g)![]() TiO2(s)+2Cl2(g) ��H=-175.4kJ/mol����.2C(s)+O2(g)
TiO2(s)+2Cl2(g) ��H=-175.4kJ/mol����.2C(s)+O2(g)![]() 2CO(g) ��H=-220.9kJ/mol������-���ɵ�TiCl4(g)+2CO(g)
2CO(g) ��H=-220.9kJ/mol������-���ɵ�TiCl4(g)+2CO(g)![]() TiO2(s)+2C(s)+2Cl2(g)�����ݸ�˹���ɿɵã���H=-175.4kJ/mol-(-220.9kJ/mol)=+45.5kJ/mol���ʴ�Ϊ��+45.5��
TiO2(s)+2C(s)+2Cl2(g)�����ݸ�˹���ɿɵã���H=-175.4kJ/mol-(-220.9kJ/mol)=+45.5kJ/mol���ʴ�Ϊ��+45.5��
(2)���������Ϣ��֪��
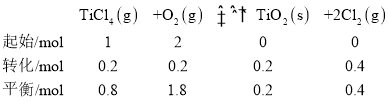
��0~4min�ڣ���Cl2��ʾ�ķ�Ӧ����![]() ��ƽ�ⳣ��
��ƽ�ⳣ��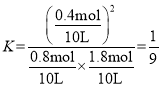 ��
��![]() ���ʴ�Ϊ��0.01mol/(Lmin)��
���ʴ�Ϊ��0.01mol/(Lmin)��![]() ��10%��
��10%��
��A. ��С�������������ѹǿ��������Ӧ���ʼӿ죬��ƽ�ⲻ�ƶ���O2��ƽ��ת���ʲ��䣬Aѡ�����
B���������������Ӧ���ʼӿ죬��ƽ�ⲻ�ƶ���O2��ƽ��ת���ʲ��䣬Bѡ�����
C�����������TiO2������Ӧ���ʼ�����ƽ�������ƶ���O2��ƽ��ת��������Cѡ�����
D������O2��Ũ�ȣ�����Ӧ���ʼӿ죬ƽ�������ƶ�����������������ԭ����ֻ���������ܵ�����O2��ƽ��ת���ʽ��ͣ�Dѡ�����
E�������¶ȣ�����Ӧ���ʼ�����ƽ�������ƶ���O2��ƽ��ת��������Eѡ�����
���ϣ����Ϸ�������������������F��ȷ����Ϊ��F��
������TiCl4��Ũ�����ӣ�O2��ת����Խ��Խ������L1��ʾO2��ƽ��ת���ʵ����ߣ�M���ʾn(TiCl4/O2)=����ʽ������֮��=1ʱ��TiCl4��ת���ʺ�O2��ת������ͬ����a=1��t��ʱ����10L�����ܱ������г���3molTiCl4��3molO2�Ļ������ʱ��ת������ȣ���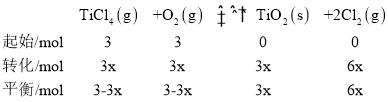
��Ϊ�¶Ȳ��䣬��ƽ�ⳣ�����䣬��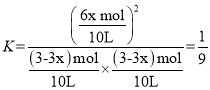 �����x=
�����x=![]() ��M���������
��M�������Ϊ��![]() ���ʴ�Ϊ��L1��
���ʴ�Ϊ��L1��![]() ��
��
(3)��ͼ��֪��H2SO4���������Һ�������缫��COʧȥ����ת��ΪCO2����缫��ӦʽΪCO��2e-��H2O=CO2��2H+���Լ״�Ϊȼ�ϣ�����Ϊ��������KOH��ҺΪ�������Һ�����Ƴ�ȼ�ϵ�أ��缫����Ϊ���Ե缫�����״��ڸ������뷴Ӧ������Ԫ���غ㣬����/span>0.5mol�״����뷴Ӧʱ��������CO2��0.5mol����0.8mol�������ط�Ӧ�����ݷ���ʽ2KOH+CO2===K2CO3+H2O��K2CO3+CO2+H2O===2KHCO3����֪����0.3mol��K2CO3��0.2mol��KHCO3����������Һ�����ʵ���Ҫ�ɷ���K2CO3��KHCO3���ʴ�Ϊ��CO-2e-+H2O===CO2+2H+��K2CO3��KHCO3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SO2��һ�ִ�����Ⱦ������ڻ�����ʳƷ��ҵ��ȴ�й㷺Ӧ�á�ij��ȤС��ͬѧ��SO2��ʵ�����Ʊ�������ʵ������о���
(1)��ͬѧ���ս̲�ʵ��Ҫ�������ͼ��ʾװ����ȡSO2
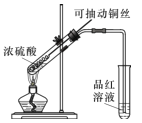
�ٱ�ʵ����ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ�� ______��ͭ˿�ɳ鶯���ŵ���_______��
��ʵ�������ͬѧ�۲쵽�Թܵײ����ֺ�ɫ�ͻҰ�ɫ���壬����Һ��ɫ���ڡ���ͬѧ��Ϊ�Ұ�ɫ����Ӧ�����ɵİ�ɫCuSO4����������ɫ����Ļ�������CuSO4��ɫ������ʽ����������Ũ�����________�ԡ�
����ͬѧ��Ϊ��ʵ����ƴ������⣬���ʵ�鰲ȫ�ͻ����Ƕȷ�������ʵ���п��ܴ��ڵ�������________��
(2)��ȤС�����������ϣ������ۺϷ������ۣ��������ʵ������(����װ����)��
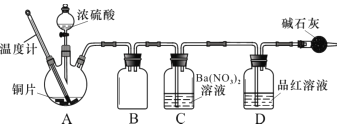
ʵ���¼ A ���������£�
��� | ��Ӧ�¶�/�� | ʵ������ |
1 | 134 | ��ʼ���ֺ�ɫ��״��������³������������ |
2 | 158 | ��ɫ���������ͬʱ������������ |
3 | 180 | ����ų����ٶȸ��죬�Թ�����ҺΪ��ɫ���� |
4 | 260 | �д��������������Һ��Ϊ��ɫ���Թܵײ������Ұ�ɫ���壬Ʒ����Һ��ɫ |
5 | 300 | ͬ�� |
�������ϵ�֪�� �����еĺ�ɫ�ͻҰ�ɫ����������Ҫ�ɷ�Ϊ CuS��Cu2S �� CuSO4������CuS �� Cu2SΪ��ɫ���壬�����¶�������ϡ���ᣬ�ڿ��������վ�ת��ΪCuO��SO2��
��ʵ����ʢװŨ�������������Ϊ ____________��
��ʵ���¼����__________��ʵ������Ӱ�죬Ϊ�˵õ�Ԥ��ʵ�������ڲ�����Ӧ��____________��
��װ��C �з�����Ӧ�����ӷ���ʽ�� ___________________��
�ܽ�ˮϴ������ĺ�ɫ�����ɺⶨ����ǰ��������仯�����Խ�һ��ȷ����ɫ�������Ƿ�һ������ CuS��ԭ��Ϊ__________(��ϻ�ѧ����ʽ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��M ��ij���ϵ���Ч�ɷ֣�������к� 3 ����Ԫ����M ��һ�ֺϳ�·�����£�
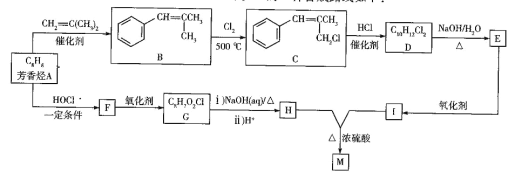
��֪����A ����������ԭ�ӿ��ܹ�ƽ�棻��D �ĺ˴Ź�����������6���壻��H �� I ��Ϊͬϵ� ��ش��������⣺
(1)A ��������____________��E ������������������___________��
(2)B��C �ķ�Ӧ������____________��
(3)д�� H �� I ��Ӧ���� M �Ļ�ѧ����ʽ��___________��
(4)T�� H ��ͬ���칹�壬ͬʱ�߱�����������T��___________��(�����������칹)�����У�������һ�����ֻ�� 2 �ֵĽṹ��ʽΪ____________��
����FeCl3��Һ������ɫ��Ӧ�����ܷ���ˮ�ⷴӦ��������Ӧ��
(5)A ��(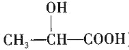 )��ҽҩ����㷺����������������������ܼ��ȡ������������̣��� 2����ϩ����ϩΪԭ�Ϻϳ����ᣬ��ƺϳ�·�ߣ�_____________________(���Լ���ѡ)��
)��ҽҩ����㷺����������������������ܼ��ȡ������������̣��� 2����ϩ����ϩΪԭ�Ϻϳ����ᣬ��ƺϳ�·�ߣ�_____________________(���Լ���ѡ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ⶨ�л���������̼�������ɳ���ȼ�շ���������ͼ�ǵ¹���ѧ�����ϣ�ⶨ�л�����ɵ�װ�ã�����ͭ����������750������ʹ�л�������������ȫ������ΪCO2��H2O���ú��й����������ƺ��Ȼ��Ƶ����չֱܷ�����CO2��H2O��
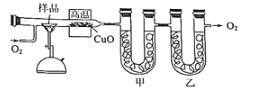
�Իش��������⣺
(1)��װ����ʢ�ŵ�ҩƷ��______��
(2)��4.6g �л���A����ʵ�飬�������5.4gH2O��8.8gCO2����������и�Ԫ�ص�ԭ�Ӹ�������______��
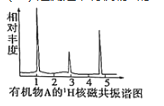
(3)���ⶨ���л���A��1H�˴Ź�������ͼ����A�Ľṹ��ʽΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣�W��X��Y��ZΪ����������Ԫ�أ�W��X������ϼ�֮��Ϊ8������˵����ȷ���ǣ� ��
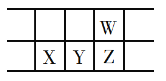
A.ԭ�Ӱ뾶��W>Z
B.�����£�X�ĵ�����Y�ĵ��ʾ�������Ũ����
C.X������������ˮ������ǿ��
D.�����̬�⻯�����ȶ��ԣ�Z<W
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(NaClO2)����ǿ�����ԣ������ֽ⣬����Ư����ʳƷ�������ȡ�
���������Ƶ��Ʊ�
�������Ƶ�Ϊԭ���Ʊ��������ƵĹ����������£�
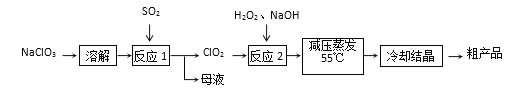
��1���������Ӧ1����Ӧ���ʵĴ�ʩ��__________________�����һ�����ɣ���ĸҺ�����ʵ���Ҫ�ɷ���___________(�ѧʽ)��
��2��ÿ��1mol SO2�μӷ�Ӧ�������Ͽ�����ClO2�����ʵ���Ϊ________mol��
��3�� ����Ӧ2���Ļ�ѧ����ʽΪ_____________________________________��
��4����ȡ����ѹ����������������ѹ��������ԭ����____________________��
��5������Ӧ2����ʹ��H2O2�������������ʵ�ԭ����____________________��
���������Ƶ�Ӧ��
��6��������������ˮ��������ˮ�п��ܲ��������������ƣ����Լ�������������ȥ�������������Σ����������������������Ʒ�Ӧ�⣬��������������____________��
��7��ʵ���ҿ����������ƺ������������������·�Ӧ�Ʊ�ClO2���塣д��������Ӧ�����ӷ���ʽΪ____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������,Ka1(H2CO3)=4.3��10-7,Ka2(H2CO3)=5.6��10-11��ij��Ԫ��H2R�������ε���Һ��,H2R��HR-��R2-���ߵ����ʵ�����������ҺpH�仯��ϵ��ͼ��ʾ����������������ǣ� ��
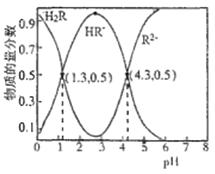
A.��pH=4.3����Һ�У�3c(R2-)=c(Na+)+c(H+)-c(OH-)
B.���������Ũ�ȵ�NaOH��Һ��H2R��Һ��Ϻ���Һ��ˮ�ĵ���̶ȱȴ�ˮС
C.��pH=3����Һ�д���![]() =10-3
=10-3
D.��Na2CO3��Һ�м�������H2R��Һ��������Ӧ��CO32-+H2R=HCO3-+HR-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ά(PET) �ṹ��ʽΪ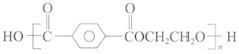 ,������������Ӧ�ù㷺������ռ�ϳ���ά������70%���ϣ��ϳ�ԭ����Ҫ��Դ��ʯ�ͺ�ú�IJ�Ʒ��
,������������Ӧ�ù㷺������ռ�ϳ���ά������70%���ϣ��ϳ�ԭ����Ҫ��Դ��ʯ�ͺ�ú�IJ�Ʒ��
��1����������ϩ�ͶԶ��ױ�Ϊ�л�ԭ�ϣ���Ƹþ�����ά�ϳ���·: ___________(�ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ���������Լ���ѡ)��
��2��д�����������з������۷�Ӧ�Ļ�ѧ����ʽ: ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��������ͼװ����ȡ�ܽϳ�ʱ����ڵ�Fe(OH)2������ʵ��������Һ��������������ˮ�ȼ�����С����з�����ȷ����
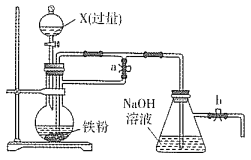
A. X������ϡ�����ϡ�����ϡ����
B. ʵ�鿪ʼʱӦ�ȹر�ֹˮ��a����b��������ƿ�м���X
C. ��Ӧһ��ʱ��������ƿ�й۲쵽��ɫ����
D. ��Ӧ���������ر�b����Һ©����������Fe(OH)2�ɽϳ�ʱ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com