
����Ŀ��Ϊ̽��FeCl3��Һ�е�����ƽ������ӷ�Ӧ��ijС��ͬѧ����������ʵ�顣
��1������50 mL 1.0 mol��L1��FeCl3��Һ������pHԼΪ0.7����c(H+) = 0.2 mol��L1��
���û�ѧ�������FeCl3��Һ�����Ե�ԭ����
������ʵ�鷽���У���ʹFeCl3��ҺpH���ߵ���������ĸ��ţ���
a.��ˮϡ�� b. ����FeCl3����
c.�μ�ŨKSCN��Һ d. ����NaHCO3����
��2��С��ͬѧ��������FeCl3��Һ̽����������п�۵ķ�Ӧ��ʵ��������������£�
���� | ���� |
��Ӧƿ�м���6.5 gп�ۣ�Ȼ�����50 mL 1.0 mol��L1��FeCl3��Һ������ | ��Һ�¶�Ѹ���������Ժ���ֺ��ɫ������ͬʱ�����������ݣ���Ӧһ��ʱ����ã��ϲ���ҺΪdz��ɫ����Ӧƿ�ײ��к�ɫ���� |
�ռ����鷴Ӧ�����в��������� | �����ܿڿ������棬�б����� |
��֪��Zn��������Al���ƣ��ܷ�����Ӧ��Zn + 2NaOH = Na2ZnO2 + H2 ��
�� ���ʵ�������ƽ���ƶ�ԭ�����ͳ��ֺ��ɫ������ԭ����
�� �����ӷ���ʽ���ͷ�Ӧ����ҺΪdz��ɫ��ԭ����
�� �������ɫ���壬������ʵ��֤ʵ�����к��е���Ҫ���ʡ�
i. ��ɫ������Ա�����������
ii. ���ɫ�����м���������NaOH��Һ���������ݣ�
iii. ��ii��ʣ�����������ˮϴ�Ӻ���ϡ���ᣬ�����������ݣ�
iv. ��iii��Ӧ�����Һ�еμ�KSCN��Һ���ޱ仯��
a. ��ɫ������һ�����е���������
b. С��ͬѧ��Ϊ����ʵ����ȷ����ɫ�������Ƿ���Fe3O4 �� ��������
��3��Ϊ��һ��̽������1.0 mol��L1 FeCl3��Һ��Fe3+��H+�����Ե����ǿ��������ʵ�鲢�۲쵽��Ӧ��ʼʱ�������£�
���� | ���� |
��5 mL 1.0 mol��L1��FeCl3��Һ��0.65 gп�ۻ�� | ��Һ�¶�Ѹ����������ʼʱ����û������ |
����0.65 gп�ۻ�� | ��Һ������������������ |
С��ͬѧ�ó����ۣ���1.0 mol��L1 FeCl3��Һ�У�Fe3+�������Ա�H+��ǿ��
���𰸡�
��1����Fe3+ + 3H2O ![]() Fe(OH)3 + 3H+,acd
Fe(OH)3 + 3H+,acd
��2����Һ�¶�����,��Ӧ�����г���H2ʹ��Һ��c(H+)����,����ٽ�Fe3+ + 3H2O ![]() Fe(OH)3 + 3H+�����ƶ�,���ֺ��ɫFe(OH)3����,2Fe3+ + Zn = 2Fe2+ + Zn2+,Fe��Zn,iii��,������Fe3O4,ϡ������Fe3O4��Ӧ������Fe3+����Fe������Ӧ����Fe2+,������iv�м�ⲻ��Fe3+,��û��Fe3O4�õ���iv��������ͬ
Fe(OH)3 + 3H+�����ƶ�,���ֺ��ɫFe(OH)3����,2Fe3+ + Zn = 2Fe2+ + Zn2+,Fe��Zn,iii��,������Fe3O4,ϡ������Fe3O4��Ӧ������Fe3+����Fe������Ӧ����Fe2+,������iv�м�ⲻ��Fe3+,��û��Fe3O4�õ���iv��������ͬ
��3��5 mL 0.2 mol��L-1����pH = 0.7�������� ���ɲ�����Cl-�Է�Ӧ��Ӱ�죩
��������
�⣺��1����FeCl3��Һ����������Ϊ�Ȼ���ˮ��Ľ����
���Դ��ǣ�Fe3+ + 3H2O ![]() Fe(OH)3 + 3H+��
Fe(OH)3 + 3H+��
�� a. ��ˮϡ�ͣ����ܴٽ��Ȼ���ˮ�⣬��������Ũ�ȼ�С��pH������ȷ��b. ����FeCl3���壬�Ȼ�����Һ��Ũ������ˮ��̶ȼ�С����������Ũ������pH��С������c. �μ�ŨKSCN��Һ��ʹ��������Ũ�ȼ�С��Fe3+ + 3H2O ![]() Fe(OH)3 + 3H+�����ƶ������Լ�����pH������ȷ��d. ����NaHCO3���壬ʹ��������Ũ�ȼ�С��pH������ȷ��
Fe(OH)3 + 3H+�����ƶ������Լ�����pH������ȷ��d. ����NaHCO3���壬ʹ��������Ũ�ȼ�С��pH������ȷ��
��ѡacd��
��2������Һ�¶����ߣ���Ӧ�����г���H2ʹ��Һ��c(H+)���ͣ�����ٽ�Fe3+ + 3H2O ![]() Fe(OH)3 + 3H+�����ƶ������ֺ��ɫFe(OH)3������
Fe(OH)3 + 3H+�����ƶ������ֺ��ɫFe(OH)3������
���Դ��ǣ���Һ�¶����ߣ���Ӧ�����г���H2ʹ��Һ��c(H+)���ͣ�����ٽ�Fe3+ + 3H2O ![]() Fe(OH)3 + 3H+�����ƶ������ֺ��ɫFe(OH)3������
Fe(OH)3 + 3H+�����ƶ������ֺ��ɫFe(OH)3������
�� п�������ӷ���������ԭ��Ӧ�����������ӣ�ʹ�÷�Ӧ����ҺΪdz��ɫ��
���Դ��ǣ�2Fe3+ + Zn = 2Fe2+ + Zn2+��
��a. ��ɫ������Ա���������˵�������������ɫ�����м���������NaOH��Һ���������ݣ�˵������п����˺�ɫ������һ������п��
���Դ��ǣ�Fe��Zn��
b. iii�У�������Fe3O4��ϡ������Fe3O4��Ӧ������Fe3+����Fe������Ӧ����Fe2+��������iv�м�ⲻ��Fe3+����û��Fe3O4�õ���iv��������ͬ��
���Դ��ǣ�
iii�У�������Fe3O4��ϡ������Fe3O4��Ӧ������Fe3+����Fe������Ӧ����Fe2+��������iv�м�ⲻ��Fe3+����û��Fe3O4�õ���iv��������ͬ��
��3��Ҫʹ����Һ�����������������ݣ�������5 mL 0.2 mol��L-1��������п��Ӧ������̽��Ŀ�ģ��Ƚ�1.0 mol��L1 FeCl3��Һ��Fe3+��H+�����Ե����ǿ������5 mL 1.0 mol��L1��FeCl3��Һ��0.65 gп�ۻ�ϣ���Һ�¶�Ѹ����������ʼʱ����û�����ݣ�˵��������������п��������ԭ��Ӧ��������ˮ�����ɵ���������п��Ӧ���Ӷ�˵����1.0 mol��L1 FeCl3��Һ�У�Fe3+�������Ա�H+��ǿ��
���Դ��ǣ�5 mL 0.2 mol��L-1�����ᡣ
�����㾫�����������⣬������Ҫ�˽������ԡ���ԭ��ǿ���ıȽ�(���������ӵ����������䵥�ʻ�ԭ�Ե���ǿ���������ǽ��������ӵĻ�ԭ�����䵥�ʵ���������ǿ����������ͬ����������ͬһ��ԭ����Ӧʱ����Ӧ����Խ�ף�����������������Խǿ������ͬ����������ͬһ��ԭ����Ӧʱ����ԭ���������ij̶�Խ���������������Ծ�Խǿ)��


 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ں��й��ۼ������ӻ�������ǣ� ��
A.Na2O2
B.H2O
C.MgCl2
D.N2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ���ܺ���Cl����SO42����CO32-��NH4+��Fe3����Fe2����Al3����Na����ijͬѧΪ��ȷ����ɷ֣�ȡ������Һ����Ʋ����������ʵ�飺
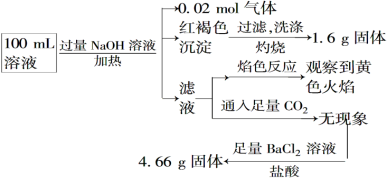
����˵����ȷ����
A��ԭ��Һ��c(Fe3��)��0.2 mol��L��1
B��Ҫȷ��ԭ��Һ���Ƿ���Fe2���������Ϊȡ����ԭ��Һ���Թ��У���KSCN��Һ���ټ���������ˮ����Һ��Ѫ��ɫ������Fe2��
C��SO42����NH4+��Na��һ�����ڣ�CO32-��Al3��һ��������
D����Һ��������4�����Ӵ��ڣ�����Cl��һ�����ڣ���c(Cl��)��0.2 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016���ҹ�������Ա���Ƴ�һ�����¡��ɺ�����NaCO2��ء��ŵ�ʱ�õ�ء����롱CO2 �� ���ʱ��������CO2������CO2ʱ���乤��ԭ������ͼ��ʾ�����յ�ȫ��CO2�У���2/3ת��ΪNa2CO3��������ڶ��̼���ܣ�MWCNT���缫���档����˵����ȷ���ǣ�( )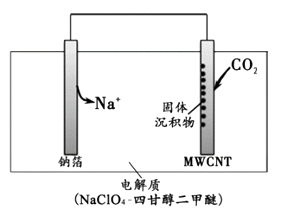
A.�����롱CO2ʱ���Ʋ�Ϊ����
B.��������CO2ʱ��Na+����̼���ܵ缫�ƶ�
C.�����롱CO2ʱ��������Ӧ��4Na+ + 3CO2 + 4e-= 2Na2CO3 + C
D.��״���£�ÿ��������22.4LCO2 �� ת�Ƶ�����Ϊ0.75mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����A������Al2(SO4)3��Al2O3��Fe2O3����һ�������¿�ʵ����ͼ��ʾ�ı仯��

��ش��������⡣
��1��B��C��D��E 4�����ʵĻ�ѧʽΪ��
B____________��C____________��D____________��E____________��
��2������F��NaOH��Һ��Ӧ�����ӷ���ʽΪ________________________________��
����E��ϡ���ᷴӦ�����ӷ���Ϊ____________________________________��
��ҺG�����ϡ��ˮ��Ӧ�Ļ�ѧ����Ϊ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������������(����������������)������������Ʒ�Ĺ�ҵ�������£�
��1������I��������Ӧ�����ӷ���ʽ����
��2������II����һ��Ũ�ȵ�NaHCO3��Һ�����������Һ��������ҺpH��Al(OH)3���ɵ��������NaHCO3��Һ����仯���������£�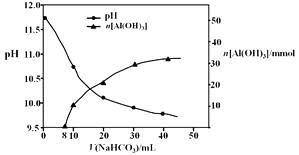
�� ����NaHCO3��Һ���С��8 mLʱ��������Ҫ��Ӧ�����ӷ���ʽ����
�� ����II����Al(OH)3�����ӷ���ʽ����
��3������III�����Na2CO3��Һ��װ������ͼ��ʾ��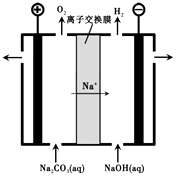
�������ĵ缫��Ӧʽ����
�ڼ�������Һ���ɵ�ԭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������þ�����Ͻ�Ͷ��100mLһ�����ʵ���Ũ�������У��Ͻ�ȫ���ܽ⣬��������Һ�еμ�4mol /LNaOH��Һ�����������ɳ��������������NaOH��Һ�������ϵ��ͼ(�����������λ��mL��������������λ��g)����
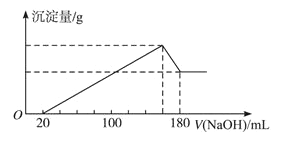
��1��ԭ�Ͻ���Mg��Al���������ٿ�?_________
��2����������ʵ���Ũ��c(HCl)=____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ�òⶨ�к��ȵ�ʵ�鲽�����£� 
������Ͳ��ȡ50mL 0.50molL��1���ᵹ��С�ձ��У���������¶ȣ�������һ��Ͳ��ȡ50mL 0.55molL��1 NaOH��Һ��������һ�¶ȼƲ�����¶ȣ��۽�NaOH��Һ����С�ձ��У��跨ʹ֮��Ͼ��ȣ���û��Һ����¶ȣ��ش��������⣺
��1��Ϊʲô����NaOH��ҺҪ�Թ�����
��2������NaOH��Һ����ȷ������������ţ���
A.�ز�������������
B.��������������
C.һ��Ѹ�ٵ���
��3��ʹ������NaOH��Һ��Ͼ��ȵ���ȷ������������ţ���
A.���¶ȼ�С�Ľ���
B.�ҿ�ӲֽƬ�ò���������
C.��������ձ�
D.�������¶ȼ��ϵĻ��β������������ؽ���
��4���ֽ�һ������ϡ����������Һ��ϡ����������Һ��ϡ��ˮ�ֱ��1L 1molL��1��ϡ����ǡ����ȫ��Ӧ���䷴Ӧ�ȷֱ�Ϊ��H1����H2����H3 �� ���H1����H2����H3�Ĵ�С��ϵΪ ��
��5������ܡ����ܡ�����Ba��OH��2��Һ�������������������Һ�����ᣬ������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������з�����ӦH2��g��+I2��g��2HI��g����0��5min��H2��Ũ�ȼ�����0.1mol/L���������ʱ����
��HI��ʾ��ƽ����Ӧ����Ϊ�� ��
A.0.01molL��1min��1
B.0.04molL��1min��1
C.0.2molL��1min��1
D.0.5molL��1min��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com