
| A、四种元素位于同一周期 |
| B、氢化物的稳定性H2Y>HZ |
| C、离子的氧化性aW3+>bX+ |
| D、原子半径Z>Y |


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
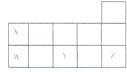
| A、YO2能使紫色石蕊试液先变红后褪色 |
| B、将W的氧化物溶于水可得W的含氧酸 |
| C、X的氢化物沸点比W的氢化物的沸点高 |
| D、Y的阴离子电子层结构与Z原子的相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
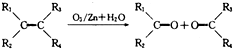 (其中R、R1、R2、R3和R4均表示烃基)今有A~K等11种不同的有机物,它们之间的转化关系如下.其中A为烃,1mol A可得2mol B.
(其中R、R1、R2、R3和R4均表示烃基)今有A~K等11种不同的有机物,它们之间的转化关系如下.其中A为烃,1mol A可得2mol B.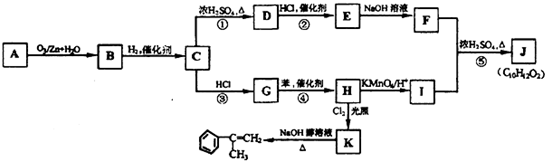
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
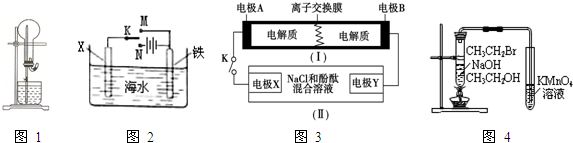
| A、图1的干燥烧瓶中盛有CO2,烧杯和滴管内盛有饱和NaHCO3溶液,挤压胶管的胶头会形成无色喷泉 |
| B、图2中若X为碳棒,开关K置于N处,铁极的反应:Fe-2e-═Fe2+ |
| C、图3中装置(Ⅰ)为一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图.当闭合开关K时,电极X附近溶液先变红,则电极B发生了还原反应 |
| D、用图4验证溴乙烷发生消去反应生成烯烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸氢钙溶液跟稀盐酸反应:Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑ |
| B、碳酸钙溶于醋酸中:CaCO3+2H+═Ca2++H2O+CO2↑ |
| C、饱和石灰水跟稀硝酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| D、氯化铁溶液中加入过量的铁粉:Fe3++Fe=Fe 2+ |
| E、向稀氨水中加入稀盐酸:NH3?H2O+H+=NH4++H2O |
| F、小苏打溶液个烧碱溶液反应:HCO3-+OH-=CO32-+H2O |
| G、氢氧化钡溶液与稀硫酸反应:Ba2++OH-+H++SO42-═H2O+BaSO4↓ |
| H、铁和稀硫酸反应:2Fe+3H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
| B、某溶液与NaOH溶液共热,产生使湿润红色石蕊试纸变蓝的气体,说明原溶液中一定存在NH4+ |
| C、某溶液加入BaCl2溶液,产生了白色沉淀,再加入足量的HNO3溶液,沉淀不溶解,则溶液中一定含有SO42- |
| D、验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加硝酸银的硝酸溶液,有白色沉淀出现,证明含Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com