
����Ŀ���������ȣ�ClO2������������ˮ�������Դ���Ϊԭ������ClO2�Ĺ�����Ҫ�������ٴ��ξ��ƣ��ڵ������NaCl��Һ����ClO2����ȡ��������������ͼ��

�� ��ʳ��ˮ�к���Ca2+��Mg2+��SO42-�����ʡ����Ӳ���ʱ��������ˮ���ȼ���������Լ�X��X��_____(�ѧʽ)�����������ٲ������ټ��������Na2CO3��NaOH����ַ�Ӧ����һ����ȥ������ⷢ����Һ���Ժ���һ������SO42-����ԭ����_______������֪��Ksp(BaSO4)��1.1��10��10��Ksp(BaCO3)��5.1��10��9��
�����������У���ʳ��ˮ���ض������µ��õ��������������ᷴӦ����ClO2�����ʱ���ɵ�����B��__����Ӧ��Ļ�ѧ����ʽΪ________________��
�� ClO2�ܲ��ȶ������������ƣ�������ˮ���յõ�ClO2��Һ��Ϊ�ⶨ������Һ��ClO2�ĺ���������������ʵ�飺
����1��ȷ��ȡClO2��Һ10.00 mL��ϡ�ͳ�100 mL������
����2����ȡV1mL�������뵽��ƿ�У�����������pH��2.0������������KI���壬ҡ�ȣ��ڰ�������30���ӡ�(��֪��ClO2��I����H+��I2��Cl����H2O δ��ƽ)
����3���Ե�����Һ��ָʾ������c mol��L��1Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��ҺV2mL������֪��I2��2S2O32-��2I����S4O62-��
�� ȷ��ȡ10.00 mL ClO2��Һ�IJ���������_________________________��
�� �ζ������У�������ƽ�вⶨ���ε�ԭ����________________________��
�� ������������ɼ����ԭClO2��Һ�����ʵ���Ũ��Ϊ__________mol��L��1���ú���ĸ�Ĵ���ʽ��ʾ����
���𰸡�BaCl2 BaSO4��BaCO3��Ksp������Һ�д��ڴ�����CO32-����ʱ��BaSO4(s)�Ჿ��ת��ΪBaCO3(s) H2 2NaClO3��4HCl==2ClO2����2NaCl��2H2O+Cl2�� ��ʽ�ζ��� ����ʵ����� ![]()
��������
����ˮ�к��е��������ӿ���ͨ���ӳ����Լ���ȥ��BaCl2��Һ�ڼ�Na2CO3��Һ֮ǰ�ӡ����Ƶ�ʳ��ˮ��������Һ�е�⣬�õ�NaClO3��NaCl+3H2O![]() NaClO3+3H2����Ȼ��NaClO3��HCl��Ӧ����ClO2������ʽΪ2NaClO3��4HCl=2ClO2����2NaCl��2H2O+Cl2����
NaClO3+3H2����Ȼ��NaClO3��HCl��Ӧ����ClO2������ʽΪ2NaClO3��4HCl=2ClO2����2NaCl��2H2O+Cl2����
�Ŵ�ʳ��ˮ�к���Ca2+��Mg2+��SO42�������ʡ����Ӳ���ʱ��������ˮ���ȼ��������BaCl2����ȥ��������ӣ����ݳ���ת��ԭ����BaSO4��BaCO3��Ksp������Һ�д��ڴ�����CO32������ʱ��BaSO4(s)�Ჿ��ת��ΪBaCO3(s)�����Ծ���ⷢ����Һ���Ժ���һ������SO42����
�Ƹ��ݵ��ԭ��NaCl�������ƣ�����������Ӧ�����������������ɣ�����B���������ɣ�����B����������Ӧ���������ơ���������ClO2����������Ӧ�Ļ�ѧ����ʽΪ2NaClO3��4HCl=2ClO2����2NaCl��2H2O+Cl2����
��ClO2���������ԣ�ȷ��ȡ10.00 mL ClO2��Һ�IJ�����������ʽ�ζ��ܣ�Ϊ����ʵ����������ƽ�вⶨ���ε�ԭ���ǣ���ԭClO2��Һ�����ʵ���Ũ��Ϊxmol��L��1������ClO2~ I2~2S2O32����ϵʽ��2��V1mL![]() ��x=V2mL
��x=V2mL![]() ��c mol��L��1��x=
��c mol��L��1��x=![]() ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)T ��ʱ,��1 L�ܱ�������A������B���巴Ӧ����C���塣��Ӧ������A��B��C��Ũ����ʱ��t�ı仯��ͼ��ʾ���÷�Ӧ�Ļ�ѧ����ʽΪ______����2��������A��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ____mol��L-1��min-1��

(2)һ��������,������Ӧ�ﵽ��ѧƽ��״̬�ı�־��_____(����ĸ)��
A.v(��)=v(��)=0
B.�����ʵ�Ũ�Ȳ��ٱ仯
C.��λʱ��������1 mol A,ͬʱ����3 mol B
(3)���÷�Ӧ�ų�����,�����¶�ʱ,��ѧ��Ӧ����____(�����С��),ƽ����_____(��������桱)��Ӧ�����ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��HCN��һ�־綾�Ե��ᣬ�����£�0.10molL-1HCN��Һ��pH = 3������˵����ȷ����( )
A.HCN��һ��ǿ��
B.��ͬŨ�ȵ�NaCl��Һ��NaCN��Һ��ǰ�ߵ�pH����
C.��NaCN��Һ�д��ڣ�c(Na+) = c(HCN) + c(CN��)
D.�к���ͬ�����Ũ�ȵ�HCl��Һ��HCN��Һ�������ĵ�NaOH��Һ�������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����AgCl����ˮ�γɱ�����Һ
��1��д�������ܽ�ƽ�ⷽ��ʽ___________________________________�� д��AgCl��Ksp����ʽ________________________________________
��2������ñ�����Һ�м���NaCl���壬��C(Ag+)_____(��������������������
�����������£���Ũ�Ⱦ�Ϊ0.1molL-1������4����Һ��
��NaCN��Һ��NaOH��Һ��CH3COONa��Һ��NaHCO3��Һ
HCN | H2CO3 | CH3COOH |
Ka=4.9��10-10 | Ka1=4��10-7 Ka2=5.6��10-11 | Ka=1.7��10-5 |
��1����4����ҺpH��С����______(�����)��
��2�����и�����Ũ���ɴ�С��˳����_______________________��
��3���ܵ�ˮ�ⷽ��ʽΪ______________________________________������ˮ��ƽ�ⳣ����������Ϊ______��
��4��25��ʱ�����HCN��NaCN�Ļ����Һ��pH=11����c(HCN)��c(CN-)֮��Ϊ____________����NaCN��Һ��ͨ������CO2��������Ӧ�����ӷ���ʽΪ_____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ��������֪���ʵ���Ũ�ȵ��������ⶨδ֪���ʵ���Ũ�ȵ�NaOH��Һʱ��ѡ���̪��ָʾ��������գ�
��1����ͼ�dz��������IJ��ֽṹ��
A.  B.
B. ![]() C.
C.  D.
D. 
�����������:B_____��C______��
��ʹ��ǰ�����Ƿ�©ˮ��������______________��(���������)
��2���ñ�������ζ������NaOH��Һʱ����������ʽ�ζ��ܵĻ���������ҡ����ƿ���۾�ע��_____���ζ��յ�ʱ����ƿ����ɫ�仯Ϊ_______���Ұ��������ɫ����ԭ��
��3�����в����п���ʹ����NaOH��Һ��Ũ����ֵƫ�͵���_______��
A .��ʽ�ζ���δ�ñ�������ϴ��ֱ��ע�������
B .�ζ�ǰʢ��NaOH��Һ����ƿ������ˮϴ����û�и���
C .��ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ
D .��ȡ�������ʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
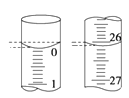
��4�����ζ���ʼ�ͽ���ʱ����ʽ�ζ����е�Һ����ͼ��ʾ������������Һ�����Ϊ_______mL��
��5��ijѧ������3��ʵ��ֱ��¼�й����������
�ζ� ���� | ����NaOH��Һ�����/mL | 0.100 0mol/L��������/mL | ||
�ζ�ǰ�̶� | �ζ���̶� | ��Һ���/mL | ||
��һ�� | 25.00 | 0.00 | 25.11 | 25.11 |
�ڶ��� | 25.00 | 0.56 | 30.56 | 30.00 |
������ | 25.00 | 0.22 | 25.11 | 24.89 |
���ݱ�������ʽ�����NaOH��Һ�����ʵ���Ũ��______����������λ��Ч���֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ��ʾ���з�Ӧ�����ӷ���ʽ���ǣ� ��
A.�ù�����ˮ���չ�ҵβ���е�SO2��2NH3��H2O��SO2=2NH4+��SO32-��H2O
B.Ca(HCO3)2��Һ������NaOH��Һ��Ӧ��Ca2����2HCO3-��2OH��=CaCO3����CO32-��2H2O
C.������������������ϡ��� Fe3O4��8H��=Fe2����2Fe3����4H2O
D.������Һ�е���Ba(OH)2��ҺʹSO42-ǡ����ȫ������2Ba2����3OH����Al3����2SO42-=2BaSO4����Al(OH)3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽΪC6H12O2���л���A������ζ��A������������ˮ�������л���B��C��B�ܺ�̼��������Һ��Ӧ�������壻C���ܷ�����ȥ��Ӧ���ܴ���������ȩ��ͪ����A���ܵĽṹ�м��֣� ��
A.4B.5C.6D.7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪CuSO4��Һ�ֱ���Na2CO3��Һ��Na2S��Һ�ķ�Ӧ������£�
(1)CuSO4��Na2CO3��Ҫ��Cu2����![]() ��H2O=Cu(OH)2����CO2�� ��Ҫ��Cu2����
��H2O=Cu(OH)2����CO2�� ��Ҫ��Cu2����![]() =CuCO3��
=CuCO3��
(2)CuSO4��Na2S��Ҫ��Cu2����S2��=CuS�� ��Ҫ��Cu2����S2����2H2O=Cu(OH)2����H2S��
���м������ʵ��ܽ�ȴ�С�ıȽ��У���ȷ����(����)
A.Cu(OH)2��CuCO3��CuSB.CuS��Cu(OH)2��CuCO3
C.CuS��Cu(OH)2��CuCO3D.Cu(OH)2��CuCO3��CuS
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.2000mol/L��NaOH��Һ��μ��뵽20.00mL0.2000mol/LNH4Cl��Һ�У���Һ��pH������NaOH��Һ������Ĺ�ϵ��ͼ��ʾ(�����ǻӷ�)������˵��������ǣ� ��

A.a����Һ�У�c(NH3H2O)+c(H+)=c(OH-)+c(NH4+)
B.��a�㵽d��ˮ�ĵ���̶Ȳ��ϼ���
C.b����Һ�У�c(Cl-)>c(Na+)>c(H+)=c(OH-)
D.c����Һ�У�c(NH3H2O)+c(NH4+)=2c(Na+)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com