
【题目】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂.请填空.
(1)如图是常见仪器的部分结构。
A.  B.
B. ![]() C.
C.  D.
D. 
①写出仪器名称:B_____,C______。
②使用前需检查是否漏水的仪器有______________。(填仪器标号)
(2)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_____,滴定终点时,锥形瓶中颜色变化为_______,且半分钟内颜色不复原。
(3)下列操作中可能使所测NaOH溶液的浓度数值偏低的是_______。
A .酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B .滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C .酸式滴定管在滴定前有气泡,滴定后气泡消失
D .读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
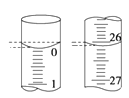
(4)若滴定开始和结束时,酸式滴定管中的液面如图所示,所用盐酸溶液的体积为_______mL。
(5)某学生根据3次实验分别记录有关数据如表:
滴定 次数 | 待测NaOH溶液的体积/mL | 0.100 0mol/L盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 25.11 | 25.11 |
第二次 | 25.00 | 0.56 | 30.56 | 30.00 |
第三次 | 25.00 | 0.22 | 25.11 | 24.89 |
依据表数据列式计算该NaOH溶液的物质的量浓度______。(保留两位有效数字)
【答案】容量瓶 滴定管 BC 锥形瓶溶液颜色的变化 淡红色突变为无色 D 26.10 0.10mol/L
【解析】
(1)①根据仪器结构特点判断;
②凡是带有活塞,旋塞的仪器使用前一般需要检查是否漏水;
(2)滴定过程中眼睛应注视锥形瓶溶液颜色的变化;酚酞在pH<8.2的溶液里为无色,滴定终点溶液显中性,据此判断滴定终点颜色变化;
(3)依据c(待测)=![]() 分析不当操作对V(标准)的影响,以此判断浓度的误差;
分析不当操作对V(标准)的影响,以此判断浓度的误差;
(4)根据滴定管的结构和精确度以及测量的原理;
(5)先根据数据的有效性,舍去第2组数据,然后求出1、3组平均消耗V(盐酸),接着根据盐酸和NaOH反应求出c(NaOH).
(1)①仪器B带有瓶塞,且瓶颈细,有刻度线无刻度为容量瓶;C带有刻度,小数在上,大数在下,为滴定管;
②容量瓶带有活塞,滴定管带有旋塞,为防止漏液,使用前应检查是否漏水;故选:BC;
(2)滴定过程中眼睛应注视锥形瓶溶液颜色的变化;用标准的盐酸滴定待测的NaOH溶液时,用酚酞做指示剂,开始溶液显碱性,所以锥形瓶中溶液颜色为红色,随着盐酸的加入量增多,溶液碱性减弱,颜色逐渐变浅,当由淡红色突变为无色,且半分钟内颜色不复原,即达到终点;
(3)A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸,导致标准液被稀释,所需标准液体积偏大,溶液浓度偏高,故A不选;
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥,对消耗标准液的体积不产生影响,溶液浓度无影响,故B不选;
C.酸式滴定管在滴定前有气泡,滴定后气泡消失,导致消耗的标准液体积偏大,溶液浓度偏高,故C不选;
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数,造成V(标准)偏小,溶液浓度偏低,故D选;
故选:D;
(4)滴定管小刻度在上,大刻度在下,精确值为0.01mL,起始读数为0.00mL,终点读数为26.10mL,盐酸溶液的体积为26.10mL;
(5)根据数据的有效性,第2组数据偏差较大,舍去第2组数据,然后求出1、3组平均消耗V(盐酸)=25.00mL,则:c(待测)=![]()
![]() =0.10mol/L。
=0.10mol/L。


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】常温下,向![]() 溶液中逐滴加入
溶液中逐滴加入![]() 溶液,混合溶液的pH随KOH溶液的加入变化情况如图,下列结论错误的是( )
溶液,混合溶液的pH随KOH溶液的加入变化情况如图,下列结论错误的是( )
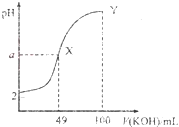
A.当加入![]() mLKOH溶液时,所得溶液中水的电离程度大于X点溶液的水的电离程度
mLKOH溶液时,所得溶液中水的电离程度大于X点溶液的水的电离程度
B.HA为弱酸,常温下,Ka的数量级为![]()
C.Y点对应的溶液中:![]()
D.若用KOH溶液滴定HA溶液,可选用甲基橙作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,CH3COOH和NH3·H2O的电离常数均为1.8×10-5。向20 mL浓度均为0.1 mol/L NaOH和NH3·H2O的混合液中滴加等物质的量浓度的CH3COOH溶液,所得混合液的导电率与加入CH3COOH溶液的体积(V)的关系如图所示。下列说法不正确的是

A. a=20,b=40,且溶液呈中性处于A、B两点之间
B. B点溶液中:c(CH3COO-)>c(Na+)>c(NH![]() )
)
C. 已知lg3≈0.5,则C点的pH≈5
D. A、B、C三点中,B点溶液中水的电离程度最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组探究常温下难溶电解质的溶解平衡,查得如下资料:
难溶电解质 | FeS | CuS | Mg(OH)2 | Fe(OH)3 |
Ksp(溶解平衡常数) | 6.3×10-18 | 6.3×10-36 | 1.8×10-11 | 4.0×10-38 |
依据上述数据进行的预测不合理的是
A.向饱和FeS溶液中加入少量Na2S固体,有浑浊出现
B.除去FeSO4溶液中的CuSO4,可选用FeS做沉淀剂
C.向含等物质的量的MgCl2和FeCl3的混合溶液中逐滴加入NaOH溶液,最先出现的沉淀是Mg(OH)2
D.向1mL 0.1 mol·L—1MgCl2溶液中滴加2mL0.1mol·L—1 NaOH溶液,取澄清溶液滴加2滴0.1mol·L—1 FeCl3溶液,有浑浊出现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,一定条件下进行如下反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g),△H=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+2CO2(g),△H=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A.加催化剂同时升高温度B.加催化剂同时增大压强
C.升高温度同时充入N2D.降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)可用于自来水消毒。以粗盐为原料生产ClO2的工艺主要包括:①粗盐精制;②电解微酸性NaCl溶液;③ClO2的制取。工艺流程如下图:

⑴ 粗食盐水中含有Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中先加入过量的试剂X,X是_____(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO42-,其原因是_______。(已知:Ksp(BaSO4)=1.1×10-10;Ksp(BaCO3)=5.1×10-9)
⑵上述过程中,将食盐水在特定条件下电解得到的氯酸钠与盐酸反应生成ClO2。电解时生成的气体B是__;反应Ⅲ的化学方程式为________________。
⑶ ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了以下实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100 mL试样。
步骤2:量取V1mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30分钟。(已知:ClO2+I-+H+—I2+Cl-+H2O 未配平)
步骤3:以淀粉溶液作指示剂,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。(已知:I2+2S2O32-=2I-+S4O62-)
① 准确量取10.00 mL ClO2溶液的玻璃仪器是_________________________。
② 滴定过程中,至少须平行测定两次的原因是________________________。
③ 根据上述步骤可计算出原ClO2溶液的物质的量浓度为__________mol·L-1(用含字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10 mL0.1 mol/L的HR溶液中逐滴加入0.1 mol/L的氨水,所得溶液pH及导电能力变化如图。下列分析正确的是( )

A. 各点溶液中的离子浓度总和大小关系:d>c > b > a
B. 常温下,R-的水解平衡常数数量级为10 -9
C. a点和b点溶液中,水的电离程度相等
D. d点的溶液中,微粒浓度关系:c(R-)+2c(HR)=c(NH3H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一定温度下CuS的溶度积常数为4.0×10-36,现将0.1 mol CuSO4放入100 mL 1.0 mol·L-1Na2S溶液中,充分搅拌反应(不考虑溶液体积变化),则下列说法不正确的是( )
A.反应后溶液的pH比反应前溶液的pH小
B.反应后溶液中不存在Cu2+、S2-
C.反应后溶液中c(Cu2+)与c(S2-)都约为2.0×10-16mol·L-1
D.若向饱和CuS水溶液中加入Na2S溶液,Ksp(CuS)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈蓝色。下列说法中不正确的是( )
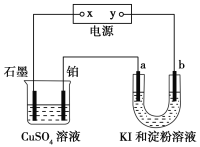
A.x是正极,y是负极 B.a极产生氢气,b极生成I2
C.a极和Pt电极都有气泡产生 D.U形管中溶液的碱性增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com