
【题目】化合物F是一种非天然氨基酸,其合成路线如下:
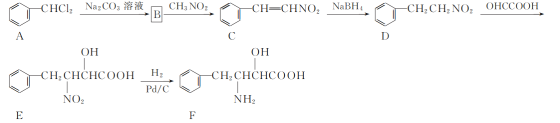
(1) C中官能团的名称为________。
(2) D→E的反应类型为________。
(3) B的分子式为C7H6O,写出B的结构简式:________。
(4) D的一种同分异构体X同时满足下列条件,写出X的结构简式: ________。
①六元环状脂肪族化合物;
②能发生银镜反应,1 mol X反应能生成4 mol Ag;
③分子中只有4种不同化学环境的氢。
(5) 写出以![]() 、CH3NO2为原料制备
、CH3NO2为原料制备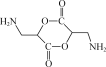 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干) _____ 。
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干) _____ 。
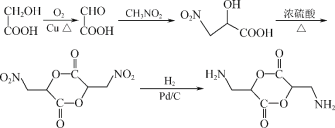
【答案】碳碳双键、硝基 加成反应 ![]()
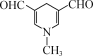 或
或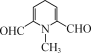 或
或![]()
【解析】
A的结构为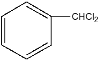 ,分子式为C7H6Cl2,不饱和度为4;B的分子式为C7H6O,不饱和度为5,因此推测B的结构为
,分子式为C7H6Cl2,不饱和度为4;B的分子式为C7H6O,不饱和度为5,因此推测B的结构为 ,即苯甲醛;C的结构为
,即苯甲醛;C的结构为 ,与NaBH4反应后生成的D的结构中不含碳碳双键,因此C发生了加成反应;由D生成E,是D与OHCCOOH反应的结果,那么根据D和E的结构推测,二者发生的是加成反应;由E生成的F结构中不再含有硝基而是代之以氨基,因此E生成F发生的是硝基还原的反应。
,与NaBH4反应后生成的D的结构中不含碳碳双键,因此C发生了加成反应;由D生成E,是D与OHCCOOH反应的结果,那么根据D和E的结构推测,二者发生的是加成反应;由E生成的F结构中不再含有硝基而是代之以氨基,因此E生成F发生的是硝基还原的反应。
(1)由C的结构可知,C中官能团的名称为碳碳双键和硝基;
(2)通过分析可知,D生成E发生的是加成反应;
(3)通过分析可知,B为苯甲醛,结构简式为: ;
;
(4)由D的结构可知,D的分子式为C8H9NO2,不饱和度为5;D的同分异构体X不含苯环,但含有六元环状结构;1mol的X可以发生银镜反应生成4mol的Ag,所以X的结构中有2个醛基;考虑到X的不饱和度也为5,所以X的结构中可能还含有两个双键,同时为了保证其分子内只有4种等效氢原子,X的结构尽可能对称;通过分析,六元环不能全由碳原子构成,这样即使结构对称也至少有5种等效氢原子,不合要求;所以可能的结构有: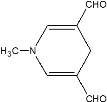 ,
, ,
, 任写一种即可;
任写一种即可;
(5)由产物的结构 可知,其含有两个酯基,并且结构对称,所以可以认为是由两分子的同一物质相互酯化得来的;此外,由于产物结构中的氨基易被氧化,所以考虑其是在合成路线的最后一步通过硝基还原得来,那么获得产物
可知,其含有两个酯基,并且结构对称,所以可以认为是由两分子的同一物质相互酯化得来的;此外,由于产物结构中的氨基易被氧化,所以考虑其是在合成路线的最后一步通过硝基还原得来,那么获得产物 可先由2个
可先由2个![]() 发生分子之间的酯化反应,再发生硝基还原即可;那么为了获得
发生分子之间的酯化反应,再发生硝基还原即可;那么为了获得![]() 则可参照D生成E的反应,利用CH3NO2与OHCCOOH二者的加成反应获得;因此合成路线为:
则可参照D生成E的反应,利用CH3NO2与OHCCOOH二者的加成反应获得;因此合成路线为: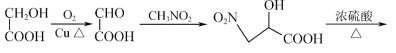
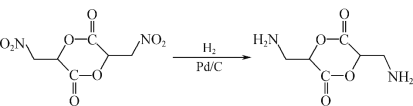 。
。


 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质.下列实验现象和结论一致且正确的是
A. 加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在
B. 溶液呈黄绿色,且有刺激性气味,说明有HClO分子存在
C. 加入AgNO3溶液产生白色沉淀,说明有Cl-分子存在
D. 加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃,101 k Pa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ/mol,辛烷的燃烧热为5518 kJ/mol。下列热化学方程式书写正确的是 ( )
A. 2H+(aq) +![]() (aq)+
(aq)+![]() (aq)+2
(aq)+2![]() (aq)=BaSO4(s)+2H
(aq)=BaSO4(s)+2H![]() O(1)
O(1) ![]() H=
H=![]() 114.6 kJ/mol
114.6 kJ/mol
B. 2KOH(aq)+ H![]() SO4(aq)= K
SO4(aq)= K![]() SO4(aq)+2H
SO4(aq)+2H![]() O(l)
O(l) ![]() H=
H=![]() 114.6kJ/mol
114.6kJ/mol
C. C8H18(l)+ ![]() O
O![]() (g)=8CO
(g)=8CO![]() (g)+ 9H
(g)+ 9H![]() O
O ![]() H=
H=![]() 5518 kJ/mol
5518 kJ/mol
D. 2C8H18(g)+25O![]() (g)=16CO
(g)=16CO![]() (g)+18H
(g)+18H![]() O(1)
O(1) ![]() H=
H=![]() 5518 kJ/mol
5518 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,3.36L氧气与3.2g硫反应,生成SO2分子数为0.1NA
B.1L0.1mol·L-1氨水中NH3·H2O分子数为0.1NA
C.标准状况下,1.12L氯气发生反应转移的电子数一定为0.1NA
D.46gNO2和N2O4混合气体中氧原子总数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一个五圆环,每个环中的物质依次为FeCl3、NaCl、Na2O2、CO2、I2,图中相连的两种物质可归属为同一类,用①、②、③、④表示相交部分,请回答下列问题:
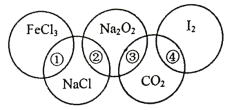
(1)关于上述相交部分的说法不正确的是___(填序号)。
A.①表示盐类 B.②表示钠的化合物
C.③表示氧化物 D.④表示非电解质
(2)关于上述相交部分的说法正确的是___(填序号)。
A.海水晒盐属于物理变化 B.Na2O2属于碱性氧化物
C.I2易溶于CCl4 D.钠着火可用CO2灭火
(3)若NaCl固体中含有少量I2杂质,可采用的除杂方法是___(填序号)
A.过滤 B.加热 C.渗析
(4)上述五种物质中,有两种物质可以发生氧化还原反应,其化学方程式为___;
(5)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1mol·L-1图中某物质M的溶液,继续煮沸得到红褐色透明液体。
①物质M的化学式为____。
②检验该红褐色透明液体是胶体的方法为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A. 1mol Na被完全氧化生成Na2O2,失去2NA个电子
B. 0.5mol锌粒与足量的盐酸反应产生H2为11.2L
C. 电解58.5g熔融的氯化钠,能产生23.0g金属钠、22.4L氯气(标准状况)
D. 标准状况下,22.4L氢气和氧气的混合气体,所含分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当密闭容器中合成氨反应N2+3H2![]() 2NH3达到平衡后,保持温度不变,将容器的容积压缩为原来的1/2。达到新平衡后,与原平衡相比较,下列说法中正确的是
2NH3达到平衡后,保持温度不变,将容器的容积压缩为原来的1/2。达到新平衡后,与原平衡相比较,下列说法中正确的是
A. 容器内的总压强为原来的2倍 B. N2的浓度比原来平衡浓度小
C. H2的转化率为原来的2倍 D. 气体的密度为原来的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍、钴及其化合物在工业上应用广泛。从某含镍废渣(含主要成分为Ni、CoO、Co2O3 及少量杂质Al2O3)提取碳酸钴、硫酸镍的工艺如下:

已知:25℃,Ksp[Co(OH)2]=4.0×10-15, lg2=0.3
(1)酸浸时需将含镍废渣粉碎,目的是_______,酸浸时通入SO2的作用是________。
(2)“除铝”时发生反应的离子方程式是______________________,25℃,若“沉钴”开始时c (Co2+) = 0.010 mo/L,则控制pH≤______时不会产生Co(OH)2沉淀。
(3)一定浓度的NiSO4溶液中加入适量的NaClO和NaOH混合液,可制得NiOOH沉淀,该反应的化学方程式为________。NiOOH可用于制备碱性镍氢电池,该电池工作原理: NiOOH+ MH![]() Ni(OH)2+M(M为储氢合金)电池充电时阳极的电极反应式是___________。
Ni(OH)2+M(M为储氢合金)电池充电时阳极的电极反应式是___________。
(4) NiSO4溶液可经过操作A得到NiSO4·7H2O晶体,俗称“翠矾”,操作A具体是指______________。煅烧该晶体时剩余固体质量与温度变化曲线如图,已知该曲线中D处所得产物均为氧化物,写出C到D的化学方程式______________。
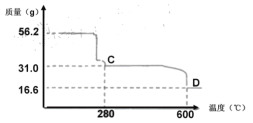
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是:
A. 反应达到平衡时,X的转化率为50% B. 反应可表示为X+3Y![]() 2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com