
����Ŀ������PAA��![]() �����и���ˮ�ԣ���״PAA�ڿ�ѹ�ԡ���ˮ�Եȷ�����������PAA����״PAA���Ʊ������ǣ�����ϩ����NaOH�кͣ���������������a���������ۺϡ��䲿�ֽṹƬ����ͼ������˵������ȷ����
�����и���ˮ�ԣ���״PAA�ڿ�ѹ�ԡ���ˮ�Եȷ�����������PAA����״PAA���Ʊ������ǣ�����ϩ����NaOH�кͣ���������������a���������ۺϡ��䲿�ֽṹƬ����ͼ������˵������ȷ����
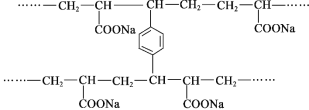
A. ����PAA�ĵ��岻����˳���칹����
B. �γ���״�ṹ�Ĺ��̷����˼Ӿ۷�Ӧ
C. ������a�Ľṹ��ʽ��![]()
D. PAA�ĸ���ˮ���롪COONa�й�
 С��ſ�ʱ��ҵϵ�д�
С��ſ�ʱ��ҵϵ�д� һ������ϵ�д�
һ������ϵ�д� �Ƹ�С״Ԫ���ֳ������ϵ�д�
�Ƹ�С״Ԫ���ֳ������ϵ�д� �¸��̵�ѧϵ�д�
�¸��̵�ѧϵ�д� ����ͬѧһ����ʦȫ�źþ�ϵ�д�
����ͬѧһ����ʦȫ�źþ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������߷ֱ��ʾԪ��ij��������˵�����Ĺ�ϵ(ZΪ�˵������Y ΪԪ�ص��й�����)�����������Ԫ���й���������ϵ����ߵı��������Ӧ�����С�
a  b
b c
c d
d e
e
(1)��A ��Ԫ�ص�����������______
(2)��A ��Ԫ���⻯��ķе�______
(3)O2����F����Na����Mg2����Al3�������Ӱ뾶______
(4)��������Ԫ�ص�����ϼ�______
(5)�ڶ�����Ԫ�� Be��B��C��N��O ��ԭ�Ӱ뾶______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������ҵ��һ��ɲ������·�Ӧ���ϳɼ״���CO(g)+2H2(g) ![]() CH3OH(g) ��H
CH3OH(g) ��H
��1����ѧƽ�ⳣ������ʽΪK=___________________��
��2����ͼ�Ǹ÷�Ӧ�ڲ�ͬ�¶���CO��ת������ʱ��仯�����ߡ�

�� �÷�Ӧ���ʱ䦤H______0(�����������������)��
�� T1��T2�¶��µ�ƽ�ⳣ����С��ϵ��K1____________K2(�����������������)��
�� �������ݻ����䣬���д�ʩ�����Ӽ״����ʵ���_________��
a. �����¶� b. ��CH3OH(g)����ϵ�з���
c. ʹ�ú��ʵĴ��� d. ����He��ʹ��ϵ��ѹǿ����
��3����֪�ڳ��³�ѹ�£��� 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)��H ��-a kJ��mol-1�� 2CO(g)+O2(g)=2CO2(g) ��H ��-b kJ��mol-1�� H2O(g)= H2O(l) ��H��-c kJ��mol-1����CH3OH(l)+O2(g) =CO(g)+2H2O(l)��H��___kJ��mol-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����м��鷽���ͽ�����ȷ����
A.�ȼ���ϡ���ᣬ�ٵμ���������Һ�а�ɫ�������ɣ���ԭ��Һ��һ����Cl��
B.�����Ȼ�����Һ�а�ɫ�������ɣ���ԭ��Һ��һ����SO![]()
C.����ŨNaOH��Һ����ȣ�������ʹʪ��ĺ�ɫʯ����ֽ����ɫ�����壬��ԭ��Һ����NH4+
D.������ɫʯ����Һ����Һ�Ժ�ɫ��֤����Һһ���ʼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯�����ת��������ͼ��ʾ�����з�����������

A. ����a���淢���˼��Թ��ۼ��Ķ��Ѻ��γ�
B. N2��H2��Ӧ����NH3��ԭ��������Ϊ100%
C. �ڴ���b�����γɵ�����ʱ�����漰����ת��
D. ����a��b����߷�Ӧ��ƽ��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���һ�ݻ�Ϊ5 L�ĺ����ܱ������г���0.4 mol SO2��0.2 mol O2��������Ӧ��2SO2(g)+O2(g)![]() 2SO3(g) ��H����196 kJ/mol������Ӧ�ﵽƽ��ʱ��������ѹǿ��Ϊ��ʼʱ��0.7������ش��������⣺
2SO3(g) ��H����196 kJ/mol������Ӧ�ﵽƽ��ʱ��������ѹǿ��Ϊ��ʼʱ��0.7������ش��������⣺
��1 ���жϸ÷�Ӧ�ﵽƽ��״̬�ı�־��___________(����ĸ)��
A��SO2��O2��SO3���ߵ�Ũ��֮��Ϊ2��1��2 B�������������ѹǿ����
C�������ڻ��������ܶȱ��ֲ��� D��SO3�����ʵ������ٱ仯
E��SO2���������ʺ�SO3�������������
��2����SO2��ת���ʣ�_______________���ڴﵽƽ��ʱ��Ӧ�ų�������Ϊ____________kJ���۴��¶��¸÷�Ӧ��ƽ�ⳣ��K��__________��
��3����ͼ��ʾƽ��ʱSO2�����������ѹǿ���¶ȱ仯�����ߣ���

���¶ȹ�ϵ��T1________T2(���������������������ͬ)��
��ƽ�ⳣ����ϵ��KA_________KB��KA_________KD��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ����NO2(g)��CO(g) ![]() CO2(g)��NO(g)��Ӧ�����������仯��ʾ��ͼ��һ�������£��ڹ̶��ݻ����ܱ������и÷�Ӧ�ﵽƽ��״̬�����ı�����һ������X��Y��X�ı仯��ϵ������ͼ����ʾ��
CO2(g)��NO(g)��Ӧ�����������仯��ʾ��ͼ��һ�������£��ڹ̶��ݻ����ܱ������и÷�Ӧ�ﵽƽ��״̬�����ı�����һ������X��Y��X�ı仯��ϵ������ͼ����ʾ��

�����й�˵����ȷ����
A. һ�������£����ܱ������м���1 mol NO2(g)��1 mol CO(g)��Ӧ�ų�234 kJ����
B. ��X��ʾCO����ʼŨ�ȣ���Y��ʾ�Ŀ�����NO2��ת����
C. ��X��ʾ�¶ȣ���Y��ʾ�Ŀ�����CO2�����ʵ���Ũ��
D. ��X��ʾ��Ӧʱ�䣬��Y��ʾ�Ŀ����ǻ��������ܶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Anammox����һ�����͵İ���ȥ������������˵��������ȷ����

A. 1mol NH4+ ��������������Ϊ10NA
B. ������N2H4���к��м��Լ��ͷǼ��Լ�
C. ����II����������Ӧ������IV���ڻ�ԭ��Ӧ
D. ����I�У����뷴Ӧ��NH4+��NH2OH�����ʵ���֮��Ϊ1:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�������ܶ�Ϊ1.25g/mL��������Ϊ36.5%��Ũ��������480 mL0.1mol/L�����ᡣ��ش��������⣺
��1��Ũ��������ʵ���Ũ��Ϊ _________��
��2������480 mL0.1 molL��1��������Ҫ�������У��ձ�������������ͷ�ιܡ�_____��_______��
��3������Ͳ��ȡŨ���� ___mL
��4��ʹ������ƿ������Һʱ�����������ʹ������ҺŨ��ƫ�͵���___��
����������ƽ��ʹ�����룩����ʱ�����������������λ�÷ŵߵ���
����Щ�����ܽ����ȣ���δ����ȴ��ת��������ƿ��
����Һת�Ƶ�����ƿ���ձ���������δ������ˮϴ�ӡ�
��ת����Һʱ��������������ƿ�ڽӴ�
�����ݺ�ҡ�ȣ�����Һ�潵�ͣ��ֲ�������ˮ�����´ﵽ�̶���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com