
关于平衡常数,下列说法不正确的是( )
A.平衡常数不随反应物或生成物的浓度的改变而改变
B.平衡常数随温度的改变而改变
C.平衡常数不随压强的改变而改变
D.使用催化剂能使平衡常数增大
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
H-是负一价的阴离子,它可与NH3发生以下反应:H-+NH3= H2+NH2-,下列有关这个反应的说法中不正确的是
A. 该反应中NH3被还原 B.该反应中H-是还原剂
C.该反应中NH2-是还原产物 D.反应中被氧化和被还原的元素都是H元素
查看答案和解析>>
科目:高中化学 来源: 题型:
氢氟酸(HF)是一种弱酸。25℃时,向20mLO.1mol•L-1氢氟酸中加入VmL0.1mol•L-1NaOH溶液充分反应。已知: HF(aq)+OH-(aq)═F-(aq)+H2O(1) △H= - 67.7kJ•mol-1,
H+(aq)+OH-(aq)═H2O (1) △H═ - 57.3kJ•mol- 根据题意,下列判断或结论正确的是
A.氢氟酸的电离过程是吸热的
B.当V=20时,溶液中:c(F-)<c(Na+)=0.1mol•L-1
C.当V<20时,溶液中离子浓度关系可能为:c(Na+)=c(F-)
D.当V>20时,溶液中离子浓度关系一定为:c(Na+)>c(F-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列解释物质用途或现象的反应方程式不准确的是
A.硫酸型酸雨的形成会涉及反应:2H2SO3+O2 2H2SO4
2H2SO4
B.热的纯碱溶液可以清洗油污的原因:CO32— +2H2O
 H2CO3+2OH¯
H2CO3+2OH¯
C.盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH¯=SiO32—+H2O
D.成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ ClO-+2H+= Cl2↑+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
银氨溶液可用于检测CO气体,实验室研究的装置如图:
|
| 已知:银氨溶液制备反应为 Ag++2NH3·H2O=[Ag(NH3)2]++2H2O。 反应结束后试管C底部有黑色沉淀生成,分离出上层清液和底部黑色固体备用。 |
(1)甲酸(HCOOH)遇浓硫酸分解生成CO和H2O,该反应体现浓硫酸的 (填“强氧化性”或“脱水性”)。
(2)装置A中软管的作用是 。
(3)为验证上层清液中产物的成分,进行如下实验:
a.测得上层清液pH为10。
b.向上层清液中滴加几滴Ba(OH)2溶液,发现有白色浑浊出现,同时产生能使湿润
红色石蕊试纸变蓝的气体。
c.取新制的银氨溶液滴加几滴Ba(OH)2溶液,无明显现象。
①实验c的目的是 。
②根据上述实验现象判断,上层清液中产物成分为 (填化学符号)。
(4)设计实验证明黑色固体的成分是Ag:
可供选择的试剂有:浓硫酸、浓硝酸、NaOH溶液、NaCl溶液。
取少量上述黑色固体,用蒸馏水洗净, ,说明黑色固体是Ag单质。(补充必要的实验内容及实验现象)
(5)从银氨溶液中回收银的方法是:向银氨溶液中加入过量盐酸,过滤,向沉淀AgCl
中加入羟氨(NH2OH),充分反应后可得银,羟氨被氧化为N2。
①写出生成AgCl沉淀的离子反应 。
②若该反应中消耗6.6 g羟氨,理论上可得银的质量为 g。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
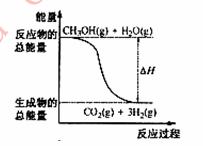
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH= + 49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
下列说法正确的是( )
A.CH3OH的燃烧热为192.9 kJ/mol
B.反应①中的能量变化如右图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知:CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g) ΔH > -192.9kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,反应2SO2 + O2  2SO3达到平衡时,n(SO2)∶n(O2)∶n(SO3) =
2SO3达到平衡时,n(SO2)∶n(O2)∶n(SO3) =
2∶3∶4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,
此时SO2的物质的量应是( )
A.0.4mol B.0.6mol C.0.8mol D.1.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
选择萃取剂将碘水中的碘萃取出,这种萃取剂应具备的性质是 ( )
A.不溶于水,且必须易与碘发生化学反应 B.不溶于水,且比水更容易使碘溶解
C.不溶于水,且必须比水密度大 D.不溶于水,且必须比水密度小
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)⇌2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表,下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
|
| A. | 反应前2min的平均速率v(Z)=2.0×10﹣3mol/(L•min) |
|
| B. | 其他条件不变,降低温度,反应达到新平衡前v(逆)<v(正) |
|
| C. | 该温度下此反应的平衡常数K=144 |
|
| D. | 其他条件不变,再充入0.2mol Z,平衡时X的体积分数增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com