
在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)⇌2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表,下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
|
| A. | 反应前2min的平均速率v(Z)=2.0×10﹣3mol/(L•min) |
|
| B. | 其他条件不变,降低温度,反应达到新平衡前v(逆)<v(正) |
|
| C. | 该温度下此反应的平衡常数K=144 |
|
| D. | 其他条件不变,再充入0.2mol Z,平衡时X的体积分数增大 |
| 化学平衡建立的过程;化学平衡的影响因素.. | |
| 专题: | 化学平衡专题. |
| 分析: | A、根据v= B、根据温度对化学平衡的影响判断; C、利用三段式,根据平衡常数的定义进行计算; D、利用等效平衡的思想作判断. |
| 解答: | 解:A、根据v=计算出Y的速率为mol/(L•min)=0.002mol/(L•min),根据速率之比等于化学计量数之比可得Z的速率为2×0.002mol/(L•min)=0.004mol/(L•min),故A错误; B、由于该反应为放热反应,降低温度时,平衡正向移动,v(逆)<v(正),故B正确; C、利用三段式, X(g)+Y(g)⇌2Z(g) 起始(mol/L) 0.016 0.016 0 转化(mol/L) 0.006 0.006 0.012 平衡(mol/L)0.01 0.01 0.012 所以平衡常数K==1.44,故C错误; D、假设将0.2mol Z在另一容器中建立与原平衡成等效平衡的体系,再将该体系加入到原容器中,由于该反应前后气体体积不变,所以压强对平衡的移动没有影响,所以加入后,X的体积分数不变,故D错误; 故选B. |
| 点评: | 本题主要考查了化学反应速率的计算、影响平衡移动的因素、化学平衡常数的计算、等效平衡的思想等知识,中等难度,解时注意基本原理的应用. |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
关于平衡常数,下列说法不正确的是( )
A.平衡常数不随反应物或生成物的浓度的改变而改变
B.平衡常数随温度的改变而改变
C.平衡常数不随压强的改变而改变
D.使用催化剂能使平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为4种常见溶液中溶质的质量分数和物质的量浓度:
| 溶 质 | HCl | NaOH | CH3COOH | HNO3 |
| 溶质的质量分数/% | 36.5 | 40 | 60 | 63 |
| 物质的量浓度/mol L-1 | 11.8 | 14.3 | 10.6 | 13.8 |
这4种溶液中密度最小的是( )
A HCl B NaOH C CH3COOH D HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各表述与示意图一致的是( )

|
| A. | 图①表示N2O4(g)⇌2NO2(g)△H>0,N2O4转化率随温度、时间的变化 |
|
| B. | 图②中曲线表示反应2SO2(g)+O2(g)⇌2SO3(g)△H<0,正、逆反应的平衡常数K随温度的变化 |
|
| C. | 图③表示10 mL0.01 mol/LKMnO4酸性溶液与过量0.1mol/LH2C2O4溶液混合时,n(Mn2+)随时间的变化 |
|
| D. | 图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0,使用和未使用催化剂时,反应过程中的能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
溶液中由水电离产生的c(OH﹣)=1×10﹣14mol•L﹣1,满足此条件的溶液中一定能大量共存的离子组是( )
|
| A. | Al3+ Na+ NO3﹣ Cl﹣ | B. | K+ Ba2+ Cl﹣ NO3﹣ |
|
| C. | K+Na+ Cl﹣CO32﹣ | D. | K+ NH4+ SO42﹣ NO3﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
有两只密闭容器A和B,A容器有一个可移动活塞使容器内保持恒压,B容器保持恒容,起始时向两只容器中分别充入等量的体积比为2:1的SO2和O2的混合气体,并使A和B容积相等.在保持400℃条件下使之发生反应:2SO2+O2⇌2SO3 填写下列空白:
(1)达到平衡所需时间A比B 短 ,A中SO2的转化率比B 大 .
(2)达到(1)所述平衡后,若向两容器通入数量不多的等量氩气,A容器的化学平衡移动,B容器的化学平衡 不 移动.
(3)达到(1)所述平衡后,向两容器中通入等量的原反应气体,达到平衡后,A中SO3的体积分数 不变 (增大、减小、不变),B容器中SO3的体积分数 增大 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的使用不涉及化学变化的是
A. 用活性炭去除冰箱中的异味
B. 用热碱水清除炊具上残留的油污
C. 用浸泡过高锰酸钾溶液的硅藻土保鲜水果
D. 用含硅胶、铁粉的透气小袋与食品一起密封包装
查看答案和解析>>
科目:高中化学 来源: 题型:
一定体积的KMnO4溶液恰好能氧化一定质量的KHC2O4·H2C2O4·2H2O。若用0.100 0
mol·L-1的NaOH溶液中和相同质量的KHC2O4·H2C2O4·2H2O,所需NaOH溶液的体积
恰好为KMnO4溶液的3倍,则KMnO4溶液的浓度(mol·L-1)为
A.0.008 889 B.0.080 0 C.0.120 0 D.0.240 0
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式书写正确的是 ( )
A.NaHSO4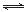 Na++ HSO4- B.NaHCO3
Na++ HSO4- B.NaHCO3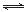 Na++H++CO32-
Na++H++CO32-
C.H3PO4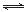 3H++PO43- D.HF
3H++PO43- D.HF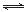 H++F-
H++F-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com