
选择萃取剂将碘水中的碘萃取出,这种萃取剂应具备的性质是 ( )
A.不溶于水,且必须易与碘发生化学反应 B.不溶于水,且比水更容易使碘溶解
C.不溶于水,且必须比水密度大 D.不溶于水,且必须比水密度小
 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应X(g)+Y(g) 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2 min的平均速率v(Z)=2.0×10-3 mol·(L·min)-1
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
关于平衡常数,下列说法不正确的是( )
A.平衡常数不随反应物或生成物的浓度的改变而改变
B.平衡常数随温度的改变而改变
C.平衡常数不随压强的改变而改变
D.使用催化剂能使平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
水的电离过程为H2O
 H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14, K(35℃)=2.1×10-14。则下列叙述正确的是( )
H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14, K(35℃)=2.1×10-14。则下列叙述正确的是( )
A.c(H+)随着温度升高而降低 B.35℃时,c(H+)>c(OH-)
C.水的电离度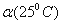 >
>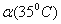 D.水的电离是吸热的
D.水的电离是吸热的
查看答案和解析>>
科目:高中化学 来源: 题型:
根据反应4FeS2+11O2 ═ 2Fe2O3+8SO2,试回答下列问题:
(1)常选用哪些物质来表示该反应的化学反应速率 、 ;
(2)当生成SO2的速率为0.64 mol/(L·s)时,则氧气减少的速率为 ;
(3)如测得4 s后O2的浓度为2.8 mol/L,此时间内SO2的速率为0.4 mol/(L·s),
则开始时氧气的浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
两个体积相同的容器,一个盛有CO,另一个盛有N2和C2H4,在同温同压下两容器内的气体一定具有相同的:①原子总数 ②质子总数 ③分子总数 ④质量( )
A.①② B.②③ C.①③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为4种常见溶液中溶质的质量分数和物质的量浓度:
| 溶 质 | HCl | NaOH | CH3COOH | HNO3 |
| 溶质的质量分数/% | 36.5 | 40 | 60 | 63 |
| 物质的量浓度/mol L-1 | 11.8 | 14.3 | 10.6 | 13.8 |
这4种溶液中密度最小的是( )
A HCl B NaOH C CH3COOH D HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各表述与示意图一致的是( )

|
| A. | 图①表示N2O4(g)⇌2NO2(g)△H>0,N2O4转化率随温度、时间的变化 |
|
| B. | 图②中曲线表示反应2SO2(g)+O2(g)⇌2SO3(g)△H<0,正、逆反应的平衡常数K随温度的变化 |
|
| C. | 图③表示10 mL0.01 mol/LKMnO4酸性溶液与过量0.1mol/LH2C2O4溶液混合时,n(Mn2+)随时间的变化 |
|
| D. | 图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0,使用和未使用催化剂时,反应过程中的能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定体积的KMnO4溶液恰好能氧化一定质量的KHC2O4·H2C2O4·2H2O。若用0.100 0
mol·L-1的NaOH溶液中和相同质量的KHC2O4·H2C2O4·2H2O,所需NaOH溶液的体积
恰好为KMnO4溶液的3倍,则KMnO4溶液的浓度(mol·L-1)为
A.0.008 889 B.0.080 0 C.0.120 0 D.0.240 0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com