
����Ŀ��һ������Һ̬������XY2����һ������O2��ǡ����ȫȼ������Ӧ����ʽΪXY2(l)��3O2(g)��XO2(g)��2YO2(g)����ȴ���ڱ�״���²��������������672 mL���ܶ���2.56 g��L��1��
��1����ӦǰO2�������________mL(��״����)��
��2��������XY2��Ħ��������________��
��3����XY2������X��Y��Ԫ����������3��16����X��Y��Ԫ�طֱ���________��________(��Ԫ�ط���)��
���𰸡� 672mL 76g/mol C S
��������(1)����ʾ��ѧ����ʽ��XY2(l)��3O2(g)![]() XO2(g)��2YO2(g)����֪���÷�Ӧ��һ��Ӧǰ���������������ķ�Ӧ������Ӧǰ�����������ͬ����Ӧ���е�XY2ΪҺ̬���ʷ�ӦǰO2�����Ϊ672 mL��
XO2(g)��2YO2(g)����֪���÷�Ӧ��һ��Ӧǰ���������������ķ�Ӧ������Ӧǰ�����������ͬ����Ӧ���е�XY2ΪҺ̬���ʷ�ӦǰO2�����Ϊ672 mL��
(2)n(O2)��672��10��3L/22.4 L��mol��1��0.03 mol����XY2��O2ǡ����ȫ��Ӧ�������ǵ����ʵ���֮��Ϊ1��3(�ɻ�ѧ����ʽ֪)����XY2�����ʵ���Ϊ0.01 mol������Ӧ�������Ϊ
672 mL���ܶ�Ϊ2.56 g��L��1����Ӧ������������Ϊm����V��2.56 g��L��1��672��10��3L��1.72 g��
���������غ㶨��
m(XY2)��1.72 g��m(O2)
��1.72 g��0.03 mol��32 g��mol��1
��������0.76 g
M(XY2)��![]() ��76 g��mol��1
��76 g��mol��1
(3)������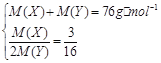
���![]()
��XΪ̼��YΪ��


 �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.1 mol��þ�������������100 mL 2mol/L H2SO4��Һ�У�Ȼ���ٵμ�
1 mol/L NaOH��Һ����ش�
�� ���ڵμ�NaOH��Һ�Ĺ����У���������m�����NaOH��Һ�����V�仯����ͼ��ʾ��

��V1��160mLʱ���������ĩ��n(Mg)�� mol��V2�� mL��
�� �μ�NaOH��Һ����ʹMg2����Al3���պó�����ȫ����V(NaOH)�� mL��
�� ���������Ϊ0.1 mol������Mg�۵����ʵ�������Ϊa����100 mL 2 mol/L�������ܽ���ټ���450 mL 1mol/L��NaOH��Һ�����ó�������Al(OH)3������������a��ȡֵ��Χ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������й�ͼ��˵����ȷ���ǣ� �� 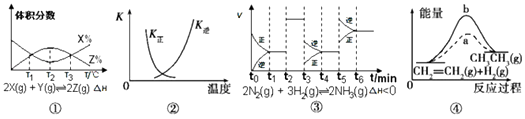
A.��ͼ��֪����Ӧ��T1��T3���ﵽƽ�⣬�Ҹ÷�Ӧ�ġ�H��0
B.ͼ�������߱�ʾ��Ӧ2SO2��g��+O2��g��2SO3��g������H��0�����淴Ӧ��ƽ�ⳣ��K���¶ȵı仯
C.��ͼ��֪����Ӧ��t6ʱ��NH3����������t3ʱ��ȡ���ͷ�Ӧ�¶ȵĴ�ʩ
D.ͼ����a��b���߷ֱ��ʾ��ӦCH2=CH2��g��+H2��g����CH3CH3��g����H��0ʹ�ú�δʹ�ô���ʱ����Ӧ�����е������仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�Na2CO3��NaHCO3��˵������ȷ���ǣ� ��
A.��������Na2CO3��NaHCO3�ֱ����������ᷴӦ��NaHCO3������CO2��
B.�����ʵ���������ֱ���������Na2CO3��NaHCO3��Ӧ��Na2CO3������CO2��
C.��ͬ�¶���ˮ�е��ܽ�ȣ�Na2CO3����NaHCO3
D.�����ʵ�����Na2CO3��NaHCO3�ֱ������������ᷴӦ�������������һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж���Ħ������������ȷ����
A. Ħ���ǹ��ʿ�ѧ�罨����õ�һ��������
B. Ħ�������ʵ����ĵ�λ,���Ħ,����mol
C. Ħ���������ʵĺ�������������ӵ�������ϵ����
D. �����Ϲ涨,0.012kg Cԭ��������̼ԭ����Ϊ1mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1 mol/L FeCl2��1 mol/L KCl��Һ�У�Cl- ���ʵ���Ũ��֮����(����)
A. 1��1 B. 2��1 C. 3��1 D. 1��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ڵ�������ܵ�����ǣ�������
A.��ˮB.����C.����D.���ڵ��Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڻ�ѧ�仯���ǣ�������
A.ú��Һ��B.ʯ�͵ķ���C.��ɫ��ӦD.�ɱ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������β����Ⱦ�����������������Ҫԭ��֮һ����������������������������⣬����Ҫ�����з�������β����ת���������ü����д����������ѡ������ǹؼ���ijϡ��������ת������β��ʾ��ͼ��ͼ�� 
��1�������й�˵����ȷ���� �� a��C3H8��CH3CH=CH3һ����������̼ԭ�Ӷ����õ���SP3�ӻ�
b��N2��CO2��H2O���ǷǼ��Է���
c��ÿ��CO2�����У�����2���м���2���Ҽ�+
d��CO��һ�ֵȵ�����ΪNO+ �� ���ĵ���ʽΪ ![]()
��2��CO��Fe�������ʻ���[Fe��CO��5]����֪������Ϊ0�ۣ���ԭ�ӵĻ�̬��������Ų�ʽΪ �� [Fe��CO��5]������λԭ���� �� ������ ��
��3��C��N��O����Ԫ�صĵ�һ�������ɴ�С��˳���� �� Al2O3�����۵�����ͻ���ϣ�AlCl3�������������۵�ͣ���ҵ�ϵ�ұ��ȡ����ǰ�߶����ú��ߵ�ԭ���� ��
��4�����ѿ��ͷ���������Ҳ����Ϊ����β��ת���Ĵ�����һ�ָ��������ᄃ���ṹ��ͼ����ʾ������ÿ��Sr2+����O2�����ڣ���Sr2+�����O2���ĺ˼��Ϊapm�������ӵ�����ΪNA �� ��������ᄃ���ܶȵļ������ʽΪ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com