
【题目】如图是某有机物分子中C、H、O、N四种原子的成键方式示意图(短线表示单键或者双键)。下列关于该有机物的说法正确的是
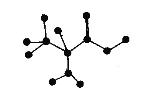
A.在一定条件下,可以通过聚合反应生成高分子化合物
B.分子式为C3H6NO2
C.能和NaOH溶液反应,但不能和盐酸溶液反应
D.不能和NaHCO3溶液反应生成CO2
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】请阅读下列材料,完成下面小题。
随着社会经济的发展,汽车已进入千家万户,它给人们出行带来方便的同时汽车尾气污染问题也日益突显,汽车尾气中含NO、NO2、CO2、SO2和固体悬浮颗粒等。用活性炭还原处理氮氧化物是一种实用的氮氧化物转化方法:C(s)+2NO(g) ![]() N2(g)+CO2(g),可实现氮氧化物无害转化。
N2(g)+CO2(g),可实现氮氧化物无害转化。
【1】下列环境问题与汽车尾气的大量排放无关的是
A.酸雨B.温室效应C.PM2.5超标D.白色污染
【2】该反应属于化学基本反应类型中的
A.化合反应B.分解反应C.置换反应D.复分解反应
【3】该反应属于氧化还原反应,下列说法正确是
A.C元素被还原B.NO得到电子C.NO发生氧化反应D.CO2是氧化剂
【4】关于该反应下列说法不正确的是
A.升高温度能够加快反应速率
B.降低NO浓度能够减慢反应速率
C.使用合适的催化剂可以加快反应速率
D.加入足量的炭粉可以使NO 100%转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=a的某电解质溶液中,插入两支惰性电极,通直流电一段时间后,溶液的pH>a,则该电解质可能是
A. Na2SO4 B. H2SO4 C. AgNO3 D. NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度范围内用氯化钠熔浸钾长石(主要成份为KAlSi3O8)可制得氯化钾,主要反应是:NaCl(l)+KAlSi3O8(s)![]() KCl(l)+NaAlSi3O8(s) △H=-Q kJ/mol。
KCl(l)+NaAlSi3O8(s) △H=-Q kJ/mol。
(1)写出Cl原子的核外电子排布式_______, NaCl的熔点比KCl______ (选填“高”或“低”)。
(2)指出钾长石中存在的化学键类型__________________。
(3)上述反应涉及的位于同一周期的几种元素中,有一种元素的最高价氧化物的水化物和其余元素的最高价氧化物的水化物均能发生反应,该元素是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是制取和收集某气体的实验装置,该装置可用于
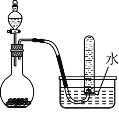
A.用浓盐酸和二氧化锰反应制取Cl2
B.用浓氨水和生石灰反应制取NH3
C.用浓硝酸与铜反应制取NO2
D.用过氧化钠固体和水反应制取O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示

下列说法正确的悬
A. △H1<0,△H2>0
B. 反应①②③的反应热满足关系:△H2-△H1=△H3
C. 反应①②③的平衡常数满足关系;K1·K2=K3
D. 要使反应③在一定条件下建立的平衡向正反应方向移动,可采取升温措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向13.6g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.25 L,固体物质完全反应,生成NO和Cu(NO3)2。在所得溶液中加入0.5 mol/L的NaOH溶液1 L,反应后溶液恰好呈中性,金属离子已完全沉淀,沉淀质量为19.6 g,下列说法不正确的是
A.Cu与Cu2O的物质的量之比为2∶1
B.硝酸的物质的量浓度为2 mol/L
C.Cu、Cu2O与硝酸反应后剩余HNO3的物质的量为0.5 mol
D.产生的NO在标准状况下的体积为2.24 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】布噁布洛芬是一种消炎镇痛的药物。它的工业合成路线如下:
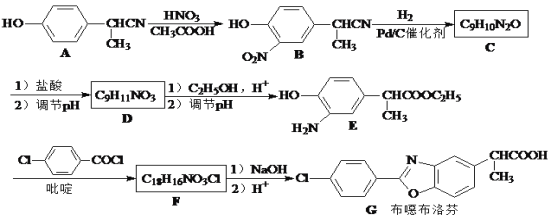
请回答下列问题:
(1)A长期暴露在空气中会变质,其原因是____。
(2)B→C反应类型为___________,E→F反应中生成的无机产物为_________。
(3)由A到B的反应通常在低温时进行。温度升高时,多硝基取代副产物会增多,最可能生成的二硝基取代物是下列物质中的__________(填字母)。
a  b
b 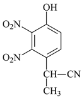 c
c 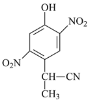 d
d 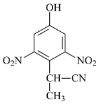
(4)D的结构简式__________;D的同分异构体H是一种α-氨基酸,能使FeCl3溶液显紫色,而且苯环上只有两个取代基,它在苯环上的一卤代物只有两种,则H的结构简式是 _________。
(5)写出以![]() 为原料制备
为原料制备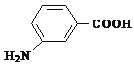 的合成路线流程图(无机试剂任选)_______________。合成路线流程图示例如下:CH2=CH2
的合成路线流程图(无机试剂任选)_______________。合成路线流程图示例如下:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3是一种常见的氧化剂,常用于医药工业、印染工业和制造烟火。实验室用KClO3和MnO2混合加热制氧气,现取KClO3和MnO2的混合物16.60g加热至恒重,将反应后的固体加15g水充分溶解,剩余固体6.55g(25℃),再加5g水充分溶解,仍剩余固体4.80g(25℃)。
(1)若剩余的4.80g固体全是MnO2,则原混合物中KClO3的质量为___g;
(2)若剩余的4.80g固体是MnO2和KCl的混合物
①求25℃时KCl的溶解度___;
②求原混合物中KClO3的质量___;
③所得KCl溶液的密度为1.72g/cm3,则溶液的物质的量浓度为多少___?(保留2位小数)
(3)工业常利用3Cl2+6KOH(热)→KClO3+5KCl+3H2O,制取KClO3(混有KClO)。实验室模拟KClO3制备,在热的KOH溶液中通入一定量氯气充分反应后,测定溶液中n(K+):n(Cl-)=14:11,将所得溶液低温蒸干,那么在得到的固体中KClO3的质量分数的取值范围为多少?___
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com