
【题目】研究NO2、NO、SO2 、CO等大气污染气体的处理具有重要意义。NO2可用下列反应来处理:
6NO2(g)+8NH3(g) ![]() 7N2(g)+12H2O(g)+Q(Q>0)。
7N2(g)+12H2O(g)+Q(Q>0)。
(1)120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡。10min时氧化产物比还原产物多了1.4g,则0~10min时,平均反应速率υ(NO2) = ____________________ ,电子转移了 ___________ 个。
(2)一定条件下上述反应在某体积固定的密闭容器中进行,能说明该反应已经达到平衡状态的是____________。
a.c(NO2):c(NH3) = 3:4 b.6v(NO2)正 = 7v(N2)逆
c.容器内气体总压强不再变化 d.容器内气体密度不再变化
(3)若保持其它条件不变,缩小反应容器的体积后达到新的平衡,此时NO2和N2的浓度之比_________ (填增大、不变、减小),NO2的转化率 ______________。
(4)一定条件下NO2与SO2可发生反应,方程式:NO2(g)+SO2(g)![]() SO3(g)+NO(g) Q。若反应的平衡常数K值变大,该反应___________(选填编号)。
SO3(g)+NO(g) Q。若反应的平衡常数K值变大,该反应___________(选填编号)。
a.一定向正反应方向移动 b. 平衡移动时,逆反应速率先减小后增大
c.一定向逆反应方向移动 d. 平衡移动时,正反应速率先增大后减小
(5)请写出用NaOH溶液完全吸收含等物质的量的NO、NO2混合气体的离子方程式___________。
【答案】0.015mol/(L·min) 1.2NA c 增大 减小 ad NO + NO2+2OH- =2NO2-+ H2O
【解析】
(1)利用化合价变化判断氧化产物、还原产物,然后根据“氧化产物比还原产物多了1.4g”计算出消耗二氧化氮的物质的量及转移电子的物质的量;
(2)可逆反应达到平衡状态时,正逆反应速率相等,各组分的浓度不再变化,据此进行判断;
(3)缩小反应容器体积,增大了压强,平衡向着逆向移动,据此判断二氧化氮与氮气的浓度之比变化及二氧化氮的转化率变化;
(4)反应的平衡常数K值变大,只有改变温度使得平衡正向移动;
(5)用NaOH溶液完全吸收含等物质的量的NO、NO2混合气体,恰好反应生成亚硝酸钠和水。
(1)对于6NO2(g)+8NH3(g) ![]() 7N2(g)+12H2O(g),当有6molNO2反应共转移了24mol电子,该反应的氧化产物和还原产物都是氮气,根据N原子守恒,6mol二氧化氮反应生成4mol氧化产物、3mol还原产物,氧化产物比还原产物多1mol,质量多:28g/mol×1mol=28g,则氧化产物比还原产物多了1.4g时转移电子的物质的量为:24mol×
7N2(g)+12H2O(g),当有6molNO2反应共转移了24mol电子,该反应的氧化产物和还原产物都是氮气,根据N原子守恒,6mol二氧化氮反应生成4mol氧化产物、3mol还原产物,氧化产物比还原产物多1mol,质量多:28g/mol×1mol=28g,则氧化产物比还原产物多了1.4g时转移电子的物质的量为:24mol×![]() =1.2mol,转移电子数为1.2NA;参加反应的NO2为:6mol×
=1.2mol,转移电子数为1.2NA;参加反应的NO2为:6mol×![]() =0.3mol,则0~10min时,平均反应速率υ(NO2)=
=0.3mol,则0~10min时,平均反应速率υ(NO2)=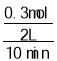 =0.015mol/(Lmin),故答案为:0.015mol/(Lmin);1.2NA ;
=0.015mol/(Lmin),故答案为:0.015mol/(Lmin);1.2NA ;
(2)a.c(NO2):c(NH3)=3:4,无法判断各组分的浓度是否变化,则无法判断是否达到平衡状态,故a错误;
b.6v(NO2)正=7v(N2)逆,表示的是正逆反应速率,但是不满足计量数关系,所以没有达到平衡状态,故b错误;
c.容器内气体总压强不再变化:该反应前后气体体积不相等,则反应过程中压强会发生变化,当压强不变时,表明正逆反应速率相等,达到平衡状态,故c正确;
d.容器内气体密度不再变化:该反应过程中气体的密度始终不变,无法根据密度变化判断平衡状态,故d错误;
故答案为:c;
(3)若保持其它条件不变,缩小反应容器的体积后达到新的平衡,由于增大了压强,平衡向着逆向移动,导致二氧化氮的含量增大、氮气的含量减小,所以此时NO2和N2的浓度之比增大,NO2的转化率减小,故答案为:增大;减小;
(4)化学平衡常数只随温度的变化而变化,该反应为吸热反应,平衡常数K值变大说明温度升高平衡右移,正反应速率先增大后减小,逆反应速率先增大再继续增大,故ad正确,故答案为:ad;
(5)用NaOH溶液完全吸收含等物质的量的NO、NO2混合气体,反应的离子方程式为:NO+NO2+2OH-=2NO2-+H2O,故答案为:NO+NO2+2OH-=2NO2-+H2O。


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
【题目】氯的氧化物是氯与氧的二元化合物的总称,也称为氧化氯。目前Cl2O、ClO2、Cl2O7已能制取。
有关数据见下表:
化学式 | Cl2O | ClO2 | Cl2O7 |
相对分子质量 | 87 | 67.5 | 183 |
沸点/℃ | 2 | 9.7 | 81 |
完成下列填空:
(1)Cl2O是____ 酸的酸酐,Cl2O电子式为____________。
(2)下列能判断Cl和O两种元素非金属性强弱的是______(选填编号)。
a.氧化氯的分子式 b.与金属反应得电子的数目
c.气态氢化物的稳定性 d.最高价氧化物对应水化物的酸性
(3)根据分子间作用力对沸点影响的变化规律:组成和结构相似的分子,其沸点随着相对分子质量的增大而升高,但上表中相对分子质量是Cl2O7>Cl2O>ClO2,其沸点的变化不是Cl2O7>Cl2O>ClO2的原因是___________________________。
(4)ClO2和碱溶液反应生成亚氯酸盐(阴离子是ClO2-)和氯酸盐,其离子方程式是________,氧化产物________。(填离子符号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化汞(HgCl2)可用于木材和解剖标本的保存、皮革鞣制和钢铁镂蚀,是分析化学的重要试剂,还可做消毒剂和防腐剂。HgCl2在水中稍有水解:HgCl2+H2O![]() Hg(OH)Cl+HCl
Hg(OH)Cl+HCl
(1)为了抑制上述反应中HgCl2的水解,可以采取的措施是_________。(选填编号)
a.加水稀释 b. 增加HCl的浓度 c.及时移走产物 d.降温
(2)HgCl2与稀氨水反应则生成难溶解的氨基氯化汞,化学方程式为HgCl2+2NH3→Hg(NH2)Cl↓+NH4Cl,上述反应的短周期元素中,非金属性最强元素原子的最外层轨道排布式为__________,该原子核外电子云有_________种不同的伸展方向。
(3)已知PCl3与NH3分子结构相似,PCl3的电子式是_______________;PCl3与NH3的沸点比较,______高,其原因是_______________________。
(4)氮的一种氢化物HN3可用于有机合成,其酸性与醋酸相似,若HN3与氨水混合,此反应的化学方程式是_______________________。
(5)若将0.4mol/LNH4Cl与0.2mol/LNaOH溶液等体积混合后,PH=10,下列关系正确的是(______)
A.c(NH4+)>c(OH-)>c(Na+)>c(NH3H2O) >c(H+)
B.c(NH4+)>c(Na+)>c(OH-)>c(NH3H2O) >c(H+)
C.c(NH4+)>c(Na+)>c(OH-)>c(H+)>c(NH3H2O)
D.c(NH4+)>c(Na+)>c(NH3H2O) >c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究电化学腐蚀及防护的装置如图所示。下列有关说法错误的是( )

A.d为石墨,电流从d流入导线进入铁片
B.d为铜片,铜片上电极反应为:O2 + 2H2O + 4e → 4OH–
C.d为锌块,铁片不易被腐蚀
D.d为镁片,铁片上电极反应为:2H+ + 2e → H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含铬Cr2O72- 废水用硫酸亚铁铵[FeSO4·(NH4)2 SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀干燥后得到n molFeO·FeyCrxO3(Cr化合价+3价) 。不考虑处理过程中的实际损耗,下列叙述错误的是( )
A.消耗硫酸亚铁铵的物质的量为n(2-x)molB.处理废水中Cr2O72- 的物质的量为![]() mol
mol
C.反应中发生转移的电子为3nx molD.在FeO·FeyCrxO3中3x=y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2 (g)![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到平衡后,若扩大容器体积,则平衡逆向移动
B.若单位时间内生成x mol NO,同时消耗x mol NH3,则达到平衡状态
C.达到化学平衡时,4υ正(O2)= 5υ逆(NO )
D.化学反应速率关系是:2υ正(NH3)= 3υ正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是反应CO(g)+2H2(g) → CH3OH(g)进行过程中的能量变化曲线。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。下列相关说法正确的是
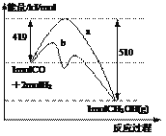
A.该反应是吸热反应
B.使用催化剂后反应热减小
C.热化学方程式为CO(g)+2H2(g) → CH3OH(g) + 510 kJ
D.热化学方程式为CO(g)+2H2(g) → CH3OH(g) + 91 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质Na2S2,其溶液显黄色并有强碱性。
(1)写出该反应的化学方程式:___________________________________。并写出Na2S2的电子式___________该物质中所具有的化学键的类型_______________;该反应中的Na2S表现了_____________性,当生成1mol Na2S2时,转移电子数目为___________。
(2)在碱性溶液中,多硫化钠Na2Sx(x≥2),可被NaClO氧化为硫酸钠,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1:16,则X的值为________。
A.5 B.4 C.3 D.2
(3)常温下Na2S溶液显______(填酸性、中性或碱性),理由是(用离子方程式表示)__________________________。
(4)常温pH=10的0.1mol/LNaHS溶液中各离子浓度由大到小的顺序是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
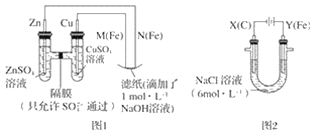
请回答:
Ⅰ.用图 1 所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是__(填字母序号)。
A 铝 B 石墨 C 银 D 铂
(2)N 极发生反应的电极反应式为__。
Ⅱ.用图 2 所示装置进行第二组实验。实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。 查阅资料得知,高铁酸根离子(FeO42-)在溶液中呈紫红色。
(3)电解过程中,X 极区溶液的 pH__(填“增大”“减小”或“不变”)。
(4)电解过程中,Y 极发生的电极反应之一为 Fe﹣6e﹣+8OH﹣= FeO42-+4H2O 若在 X 极收集到672 mL 气体,在 Y 极收集到 168 mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁电极)质量减少____g。
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2K2FeO4+3Z=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com