
����Ŀ��Na2S��Һ�ڿ����г��ڷ���,��������Ӧ��������������ƵĽṹ�ͻ�ѧ�������Ƶ�����Na2S2������Һ�Ի�ɫ����ǿ���ԡ�
(1)д���÷�Ӧ�Ļ�ѧ����ʽ��___________________________________����д��Na2S2�ĵ���ʽ___________�������������еĻ�ѧ��������_______________���÷�Ӧ�е�Na2S������_____________�ԣ�������1mol Na2S2ʱ��ת�Ƶ�����ĿΪ___________��
(2)�ڼ�����Һ�У�������Na2Sx(x��2)���ɱ�NaClO����Ϊ�����ƣ���NaClO����ԭΪNaCl,����Ӧ��Na2Sx��NaClO�����ʵ���֮��Ϊ1��16����X��ֵΪ________��
A.5 B.4 C.3 D.2
(3)������Na2S��Һ��______(�����ԡ����Ի����)��������(�����ӷ���ʽ��ʾ)__________________________��
(4)����pH=10��0.1mol/LNaHS��Һ�и�����Ũ���ɴ�С��˳����_____________________________��
���𰸡�4Na2S + O2 + 2H2O �� 4NaOH + 2Na2S2(��2Na2S + O2+2H2O��4NaOH+2S Na2S+S ��Na2S2) ![]() ���Ӽ����ۼ� ��ԭ 2NA�� A ���� S2-+H2OHS-+OH- c(Na+)>c(HS -)>c(OH-)>c(H+)> c(S2-)
���Ӽ����ۼ� ��ԭ 2NA�� A ���� S2-+H2OHS-+OH- c(Na+)>c(HS -)>c(OH-)>c(H+)> c(S2-)
��������
Na2S2�����ڹ������ƣ�����Ԫ�ػ��ϼ۵ı仯�����������ֵ����ʣ���Һ���������������ˮ������ģ�ͨ��������ǰ���������ں��ԭ�������Һ�е�����Ũ�ȹ�ϵ���Ұ�����ˮ��ƽ�⡢����ƽ�⡢ˮ�ĵ�����о��������
(1) �ڿ����г��ڷ��û�Ӵ�������������ˮ�������ʷ�Ӧ����ʽΪ��4Na2S + O2 + 2H2O �� 4NaOH + 2Na2S2�������ӻ��������ʽΪ��![]() ���к����ۼ������Ӽ�����Ԫ�ػ��ϼ��ɸ����۱���˸�һ�ۣ������˻�ԭ�ԣ�����1mol Na2S2ʱ����ʧȥ2�����ӣ���ת�Ƶ�����ĿΪ2NA��
���к����ۼ������Ӽ�����Ԫ�ػ��ϼ��ɸ����۱���˸�һ�ۣ������˻�ԭ�ԣ�����1mol Na2S2ʱ����ʧȥ2�����ӣ���ת�Ƶ�����ĿΪ2NA��
(2)������Na2Sx��NaClO����Ϊ�����ƣ���NaClO����ԭΪNaCl����Ӧ��Na2Sx��NaClO�����ʵ���֮��Ϊ1��16���ɵ����غ��֪![]() ����x=5���ʴ�Ϊ��A��
����x=5���ʴ�Ϊ��A��
(3)������Na2S��Һ�������ӷ���ˮ�⣺![]() ������Һ�Լ��ԣ�
������Һ�Լ��ԣ�
(4)����pH=10��0.1mol/LNaHS��Һ�Լ��ԣ���������Ӽ�ˮ���ֵ��룬���̶Ȳ�ͬ��ˮ�⣺![]() �����룺
�����룺![]() ������ˮ����ڵ��룬��ˮ�����Ũ�ȴ��ڵ������Ũ�ȣ�����Һ�д���ˮ�ĵ���ƽ�⣬�����ӹ�ϵ��
������ˮ����ڵ��룬��ˮ�����Ũ�ȴ��ڵ������Ũ�ȣ�����Һ�д���ˮ�ĵ���ƽ�⣬�����ӹ�ϵ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ϩ��![]() ������Ҫ���л�����ԭ�ϣ��㷺����ũҩ�������ϵ������������ϩ�������ۺ����ɶ����壬�÷�ӦΪ���淴Ӧ����ͬ�¶��£���Һ�л����ϩŨ���뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
������Ҫ���л�����ԭ�ϣ��㷺����ũҩ�������ϵ������������ϩ�������ۺ����ɶ����壬�÷�ӦΪ���淴Ӧ����ͬ�¶��£���Һ�л����ϩŨ���뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
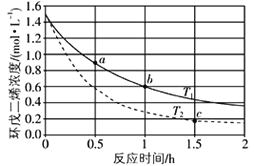
A.T1��T2
B.a��ķ�Ӧ����С��c��ķ�Ӧ����
C.a�������Ӧ����С��b����淴Ӧ����
D.b��ʱ�������Ũ��Ϊ0.45 mol��L1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�NO2��NO��SO2 ��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣NO2�������з�Ӧ��������
6NO2(g)+8NH3(g) ![]() 7N2(g)+12H2O(g)+Q(Q��0)��
7N2(g)+12H2O(g)+Q(Q��0)��
(1)120��ʱ���÷�Ӧ��һ�ݻ�Ϊ2L�������ڷ�Ӧ��20minʱ�ﵽƽ�⡣10minʱ��������Ȼ�ԭ�������1.4g����0��10minʱ��ƽ����Ӧ������(NO2) = ____________________ ������ת���� ___________ ����
(2)һ��������������Ӧ��ij����̶����ܱ������н��У���˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����____________��
a��c(NO2)��c(NH3) = 3��4 b��6v(NO2)�� = 7v(N2)��
c��������������ѹǿ���ٱ仯 d�������������ܶȲ��ٱ仯
(3)�����������������䣬��С��Ӧ�����������ﵽ�µ�ƽ�⣬��ʱNO2��N2��Ũ��֮��_________ (�������䡢��С)��NO2��ת���� ______________��
(4)һ��������NO2��SO2�ɷ�����Ӧ������ʽ��NO2(g)+SO2(g)![]() SO3(g)+NO(g) Q������Ӧ��ƽ�ⳣ��Kֵ��÷�Ӧ___________(ѡ����)��
SO3(g)+NO(g) Q������Ӧ��ƽ�ⳣ��Kֵ��÷�Ӧ___________(ѡ����)��
a.һ��������Ӧ�����ƶ� b. ƽ���ƶ�ʱ���淴Ӧ�����ȼ�С������
c.һ�����淴Ӧ�����ƶ� d. ƽ���ƶ�ʱ������Ӧ������������С
(5)��д����NaOH��Һ��ȫ���պ������ʵ�����NO��NO2�����������ӷ���ʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ���������������к����������Ź㷺Ӧ�á������й��ж��д������(����)

A. װ�â��о����ǽ�����������ʴ��Fe�ϵķ�ӦΪFe��2e��===Fe2��
B. װ�â��о����ǵ��CuCl2��Һ����������ת��Ϊ��ѧ��
C. װ�â��о����ǵ�ⱥ��ʳ��ˮ���������У�B���Ϸ���������Ӧ
D. ����װ�����漰����Ҫ��Ӧ����������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ������У���ӦaA(g)![]() bB(g)��ƽ������¶Ȳ��䣬�������������һ�������ﵽ�µ�ƽ��ʱ��A��Ũ����ԭ����60������( )
bB(g)��ƽ������¶Ȳ��䣬�������������һ�������ﵽ�µ�ƽ��ʱ��A��Ũ����ԭ����60������( )
A.ƽ�����淴Ӧ�����ƶ���B.����A��ת����������
C.����B����������������D.a<b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ķ����в��ϣ������Ӧ���
ijͬѧ���������װ��������ȡSO2����֤SO2�����ʡ���֪��1.0mol/L��Fe(NO3)3��Һ��![]() ���Իش��������⣺
���Իش��������⣺
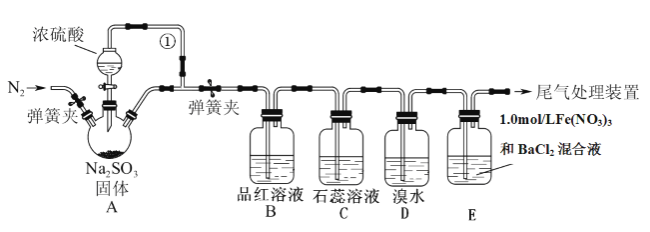
(1)װ��A����������Ũ�������������Ϊ________________________�����ܢٵ�������______________________��
(2)B��C��D����װ�÷ֱ��Ⱥ���֤��SO2����Щ����_______��
A�������ԡ����ԡ���ԭ�� B����ԭ�ԡ����ԡ���ԭ��
C��Ư���ԡ����ԡ���ԭ�� D��Ư���ԡ����ԡ�������
(3)SO2��Ʒ�췴Ӧ��ԭ����_______________________________��
(4)ʵ��ǰ����N2��Ŀ����____________________________�������˲����Ƿ��б�Ҫ_______________________________
(5)װ��E�в����˰�ɫ��������ɷ���______________(������)������E�в�����ɫ�����Ŀ���ԭ�۲쵽������(д����)���ܢ٣�_____________________������___________�����ܢڣ�_____________________������___________��
(6)����2.0mol/L ��NaOH��Һ����SO2β�����뻭����β������װ��_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ʵ������ȡ���ᶡ������ԭ��Ϊ��7.4 mL1-������6.0 mL�����ᣬ1.0mLŨ���ᡣ
1-���� | ������ | |
�ܶȣ�g/cm3�� | 0.81 | 1.05 |
Ħ������(g/mol) | 74 | 60 |
���Ƶ����ᶡ����ʽ��116��������Ϊ5.12 g����������ȷ����
A.���ʣ�Լ54.49%B.���ʣ�Լ42.04%
C.ת���ʣ�������С��1-����D.ת���ʣ����������1-����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��չ̶�������ܱ������У�����10mol N2��30mol H2��Ϻ�����Ӧ��N2��3H2![]() 2NH3����һ���¶��´ﵽƽ�⣬H2��ת����Ϊ20%������ͬһ�����г���NH3�� ��ʹ��Ӧ�ﵽƽ��ʱ���ɷֵİٷֺ���������ƽ��ʱ��ͬ������ʼʱ����NH3�����ʵ����ʹﵽƽ��ʱNH3��ת������
2NH3����һ���¶��´ﵽƽ�⣬H2��ת����Ϊ20%������ͬһ�����г���NH3�� ��ʹ��Ӧ�ﵽƽ��ʱ���ɷֵİٷֺ���������ƽ��ʱ��ͬ������ʼʱ����NH3�����ʵ����ʹﵽƽ��ʱNH3��ת������
A��15mol 20% B��20mol 20% C��20mol 80% D��40mol 80%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�����ࡢ��֬�������ʺ�ά���ض�������Ļ���Ӫ�����ʣ��±�ΪijƷ������Ƭ��ǩ�е�һ���֡�
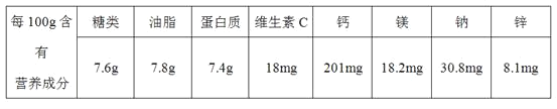
������Ƭ��Ӫ���ɷ��У�����ˮ��Ӧ���ɰ������Ӫ��������_________��ÿ��Ӫ����������ʱ�ų�����������_________��һ��Ӫ������������־���ᵽ�ġ�̼ˮ�������ָ_________������������Ԫ����_________��
��2��ά����C������ˮ������ˮ��Һ�е�����ɫʯ����Һ��ʯ����ɫ�����ȸ���Һ�����ڣ���ɫ��ʧ����ˣ��������ά����C��ʳ��ʱ��Ӧ��ע��_________���ڼ��������£�ά����C�ױ���������������ʱ��ü�һ��_________��
��3�����Ǵ����·�ͨ��������ά֯�ɵģ���������ά��������ë�����ڵȣ������շ��ɳ�������������ά����������ά��źֱ����ղ�������ζ���£�

����ë�ı��Ϊ_________�����ı��Ϊ_________�����ڵı��Ϊ_________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com