
【题目】右图是反应CO(g)+2H2(g) → CH3OH(g)进行过程中的能量变化曲线。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。下列相关说法正确的是
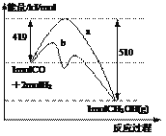
A.该反应是吸热反应
B.使用催化剂后反应热减小
C.热化学方程式为CO(g)+2H2(g) → CH3OH(g) + 510 kJ
D.热化学方程式为CO(g)+2H2(g) → CH3OH(g) + 91 kJ
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
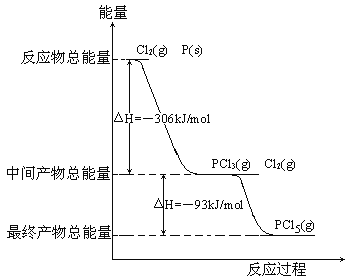
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式_________________________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式_________________________________,上述分解反应是一个可逆反应,温度T1时,在密闭容器中加入0.80molPCl5,反应达到平衡时PCl5还剩0.60mol,其分解率α1等于_________;若反应温度由T1升高到T2,平衡时PCl5的分解率为α2,α2_______α1(填“大于”、“小于”或“等于”)。
(3)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5。原因是________________________________________。
(4)P和Cl2分两步反应生成1molPCl5的△H3=_________,P和Cl2一步反应生成1molPCl5的△H4______△H3(填“大于”、“小于”或“等于”)。
(5)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁是一种新型高效的无机高分子絮凝剂。用硫酸亚铁晶体及硫酸为原料催化氧化法生成硫酸铁,再水解、聚合成产品。实验室模拟生产过程如下:
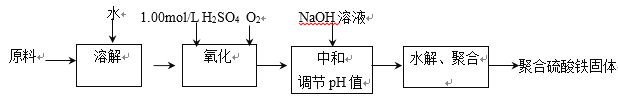
(1)①用原料配制2.50 mol/L的FeSO4溶液时用到的定量仪器有:____________________
②写出氧化过程中的离子方程式:_________________________________________
(2)综合考虑实际投料硫酸亚铁与硫酸的物质的量之比为![]() 左右最佳。 加入的硫酸比理论值稍多,但不能过多的原因是____________________________________________________________________。
左右最佳。 加入的硫酸比理论值稍多,但不能过多的原因是____________________________________________________________________。
(3)硫酸铁溶液水解可以得到一系列具有净水作用的碱式硫酸铁(x Fe2O3·y SO3·z H2O),现采用重量法测定x、y、z的值。
①测定时所需的试剂____________。
(a) NaOH (b) Ba(OH)2 (c) BaCl2 (d) FeSO4
②需要测定____________和____________的质量(填写化合物的化学式)。
(4)选出测定过程中所需的基本操作____________(按操作先后顺序列出)。
a.过滤、洗涤
b.蒸发、结晶
c.萃取、分液
d.冷却、称量
e.烘干或灼烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、NO、SO2 、CO等大气污染气体的处理具有重要意义。NO2可用下列反应来处理:
6NO2(g)+8NH3(g) ![]() 7N2(g)+12H2O(g)+Q(Q>0)。
7N2(g)+12H2O(g)+Q(Q>0)。
(1)120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡。10min时氧化产物比还原产物多了1.4g,则0~10min时,平均反应速率υ(NO2) = ____________________ ,电子转移了 ___________ 个。
(2)一定条件下上述反应在某体积固定的密闭容器中进行,能说明该反应已经达到平衡状态的是____________。
a.c(NO2):c(NH3) = 3:4 b.6v(NO2)正 = 7v(N2)逆
c.容器内气体总压强不再变化 d.容器内气体密度不再变化
(3)若保持其它条件不变,缩小反应容器的体积后达到新的平衡,此时NO2和N2的浓度之比_________ (填增大、不变、减小),NO2的转化率 ______________。
(4)一定条件下NO2与SO2可发生反应,方程式:NO2(g)+SO2(g)![]() SO3(g)+NO(g) Q。若反应的平衡常数K值变大,该反应___________(选填编号)。
SO3(g)+NO(g) Q。若反应的平衡常数K值变大,该反应___________(选填编号)。
a.一定向正反应方向移动 b. 平衡移动时,逆反应速率先减小后增大
c.一定向逆反应方向移动 d. 平衡移动时,正反应速率先增大后减小
(5)请写出用NaOH溶液完全吸收含等物质的量的NO、NO2混合气体的离子方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,密闭容器中进行反应CH4(g) + H2O(g) ![]() CO(g) + 3H2(g),测得CH4的体积百分含量随温度和压强的变化如图所示。下列说法正确的是
CO(g) + 3H2(g),测得CH4的体积百分含量随温度和压强的变化如图所示。下列说法正确的是

A. p1>p2
B. ΔH<0
C. 加入催化剂可以提高甲烷的转化率
D. 恒温下,缩小容器体积,平衡后CH4浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池与电解池在生活中和生产中有着广泛应用。下列有关判断中错误的是( )

A. 装置①研究的是金属的吸氧腐蚀,Fe上的反应为Fe-2e-===Fe2+
B. 装置②研究的是电解CuCl2溶液,它将电能转化为化学能
C. 装置③研究的是电解饱和食盐水,电解过程中,B极上发生氧化反应
D. 三个装置中涉及的主要反应都是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,反应aA(g)![]() bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度是原来的60%,则( )
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度是原来的60%,则( )
A.平衡向逆反应方向移动了B.物质A的转化率增加了
C.物质B的质量分数增加了D.a<b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某次实验室制取乙酸丁酯所用原料为:7.4 mL1-丁醇、6.0 mL冰醋酸,1.0mL浓硫酸。
1-丁醇 | 冰醋酸 | |
密度(g/cm3) | 0.81 | 1.05 |
摩尔质量(g/mol) | 74 | 60 |
若制得乙酸丁酯(式量116)的质量为5.12 g,则以下正确的是
A.产率:约54.49%B.产率:约42.04%
C.转化率:冰醋酸小于1-丁醇D.转化率:冰醋酸大于1-丁醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Heck反应是偶联反应的一种,例如:反应①如下:
![]() +CH3OOCCH=CH2(Ⅰ)
+CH3OOCCH=CH2(Ⅰ)![]()
![]() (Ⅱ)
(Ⅱ)
化合物I可以由以下途径合成:
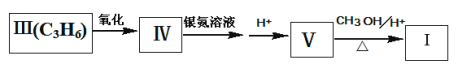
回答以下问题:
(1)化合物Ⅱ的分子式为_____,1mol该物质最多可与________molH2发生加成反应。
(2)卤代烃CH3CHBrCH3发生消去反应可以生成化合物Ⅲ,相应的化学方程式为: ________(注明条件)。
(3)分子式为C4H6O的化合物Ⅵ,满足以下条件:①与化合物IV互为同系物;②含有甲基且无支链,写出其结构简式________。
(4)一定条件下,![]() 与
与 ![]() 也可以发生类似反应①的反应,其有机产物的结构简式为__________。
也可以发生类似反应①的反应,其有机产物的结构简式为__________。
(5)设计一条以CH3CHClCHClCH3和![]() 为原料合成
为原料合成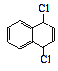 的路线_______。
的路线_______。
提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:(用合成路线流程图表示为:A![]() B……
B……![]() 目标产物)。
目标产物)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com