
【题目】三氯氧磷(POCl3)广泛用于农药、医药等生产。工业制备三氯氧磷的过程中会产生副产品亚磷酸(H3PO3)。请回答下列问题:
(1)三氯氧磷可由三氯化磷、水、氯气加热反应生成,反应的化学方程式为__________。
(2)已知亚磷酸(H3PO3)为二元弱酸,则Na2HPO3溶液中,各离子浓度的大小关系为_______。
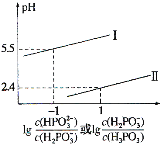
(3)常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。则表示lg![]() 的是曲线______(填“I”或“II”),亚磷酸(H3PO3)的Kal=________,反应HPO32-+H2O
的是曲线______(填“I”或“II”),亚磷酸(H3PO3)的Kal=________,反应HPO32-+H2O![]() H2PO3-+OH-的平衡常数值是____________。
H2PO3-+OH-的平衡常数值是____________。
(4)工业上生产三氯氧磷的同时会产生含磷废水(主要成分为H3PO4、H3PO3)。向废水中先加入适量漂白粉,再加入生石灰调节pH,将磷元素转化为磷酸的钙盐沉淀并回收。若处理后的废水中c(Ca2+)=5×10-6 mol·L-1,则溶液中c(PO43-)=________mol·L-1。(已知Ksp[Ca3(PO4)2]=2×10-29)
【答案】PCl3+Cl2+H2O![]() POCl3+2HCl c(Na+)>c(HPO32-)>c(OH-)>c(H2PO3-)>c(H+) I 10-1.4 10-7.5 4×10-7
POCl3+2HCl c(Na+)>c(HPO32-)>c(OH-)>c(H2PO3-)>c(H+) I 10-1.4 10-7.5 4×10-7
【解析】
(1)三氯氧磷可由三氯化磷、水、氯气加热反应生成,三氯氧磷为POCl3,实际上为PCl3与Cl2反应生成PCl5,PCl5水解生成POCl3;
(2)亚磷酸(H3PO3)为二元弱酸,则HPO32-不能再发生电离,只能水解,使溶液呈碱性,据此分析;
(3)根据H3PO3的电离平衡常数,![]() ,
,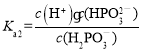 ,则lg
,则lg![]() =lg
=lg![]() ,lg
,lg![]() =lg
=lg![]() ,第一步电离平衡常数远远大于第二步电离平衡常数;
,第一步电离平衡常数远远大于第二步电离平衡常数;
(4)根据CaSO4的溶度积常数计算。
(1)三氯氧磷可由三氯化磷、水、氯气加热反应生成,三氯氧磷为POCl3,实际上为PCl3与Cl2反应生成PCl5,PCl5水解生成POCl3,发生的化学反应为:PCl3+Cl2+H2O![]() POCl3+2HCl;
POCl3+2HCl;
(2)亚磷酸(H3PO3)为二元弱酸,则HPO32-不能再发生电离,只能水解,使溶液呈碱性,同时考虑到水也存在电离平衡,所以溶液中c(H2PO3-)<c(OH-),因此溶液中离子浓度大小顺序为:c(Na+)>c(HPO32-)>c(OH-)>c(H2PO3-)>c(H+),故答案为:c(Na+)>c(HPO32-)>c(OH-)>c(H2PO3-)>c(H+);
(3)根据H3PO3的电离平衡常数,![]() ,
,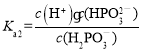 ,则lg
,则lg![]() =lg
=lg![]() ,lg
,lg![]() =lg
=lg![]() ,Ka1>>Ka2,则pH值相同时,即纵坐标相同时,lg
,Ka1>>Ka2,则pH值相同时,即纵坐标相同时,lg![]() > lg
> lg![]() ,即lg
,即lg![]() 横坐标大,则曲线I表示的是lg
横坐标大,则曲线I表示的是lg![]() 曲线II表示的是 lg
曲线II表示的是 lg![]() ;
;![]() ,根据图像可知当pH=2.4时,lg
,根据图像可知当pH=2.4时,lg![]() =1,即当溶液中c(H+)=10-2.4mol/L时,
=1,即当溶液中c(H+)=10-2.4mol/L时,![]() =10,则
=10,则![]() =10-2.4×10=10-1.4;反应HPO32-+H2O
=10-2.4×10=10-1.4;反应HPO32-+H2O![]() H2PO3-+OH-的平衡常数值
H2PO3-+OH-的平衡常数值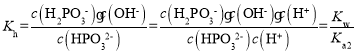 ,根据图像可知当pH=5.5时,lg
,根据图像可知当pH=5.5时,lg![]() =-1,即当溶液中c(H+)=10-5.5mol/L时,
=-1,即当溶液中c(H+)=10-5.5mol/L时,![]() =0.1,所以
=0.1,所以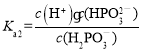 =10-5.5×0.1=10-6.5,Kh=
=10-5.5×0.1=10-6.5,Kh=![]() ,故答案为:I;10-1.4;10-7.5;
,故答案为:I;10-1.4;10-7.5;
(4)Ksp[Ca3(PO4)2]= c3(Ca2+)·c(PO43-),处理后的废水中c(Ca2+)=5×10-6mol/L,则溶液中c(PO43-)= 。
。


科目:高中化学 来源: 题型:
【题目】已知草酸是二元弱酸,0.2 mol·L-1NaHC2O4溶液显酸性,关于NaHC2O4溶液中离子浓度关系的叙述不正确的是( )
A.c(Na+)>c(HC2O4—)>c(C2O42—)>c(H2C2O4)
B.c(Na+)=c(HC2O4—)+c(C2O42—)+c(H2C2O4)
C.c(Na+)+c(H+)=c(HC2O4—)+c(C2O42—)+c(OH-)
D.c(H+)+c(H2C2O4)=c(C2O42—)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三甲胺N(CH3)3是重要的化工原料。最近我国科学家实现了使用铜催化剂将N,N—二甲基甲酰胺(N(CH3)2NCHO,简称DMF)转化为三甲胺的合成路线。回答下列问题:
(1)结合实验与计算机模拟结果,研究单一DMF分子在铜催化剂表面的反应历程,如图所示:
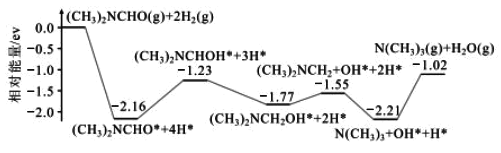
该历程中最大能垒(活化能)=__eV,该步骤的化学方程式为__。
(2)该反应变化的ΔH__0(填“<”、“>”或“=”),制备三甲胺的热化学方程式为__。
(3)160℃时,将DMF(g)和H2(g)以物质的量之比为1:2充入盛有催化剂的刚性容器中,容器内起始压强为p0,达到平衡时DMF的转化率为25%,则该反应的平衡常数Kp=__(Kp为以分压表示的平衡常数);能够增大DMF平衡转化率同时加快反应速率的操作是__。
(4)三甲胺是鱼腥臭的主要来源,是判断海水鱼类鲜度的化学指标之一。通过传感器产生的电流强度可以监测水产品中三甲胺的含量,一种燃料电池型三甲胺气体传感器的原理如图所示。外电路的电流方向为__(填“a→b”或“b→a”),负极的电极反应式为__。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰的用途非常广泛,以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴的碳酸盐及SiO2杂质)为原料生产金属锰的工艺流程如下:
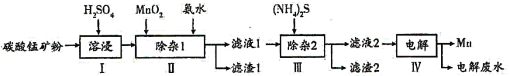
已知25℃时,部分物质的溶度积常数如下:
物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | Fe(OH)3 | MnS | CoS | NiS |
Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.1×10-36 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(1)步骤I中,为加快溶浸速率,可采取的措施是__________(至少答两条)。
(2)步骤II中,加氨水调节溶液的pH为5.0~6.0,则滤渣1的成分主要为________(填化学式);已知MnO2的作用为氧化剂,“除杂1”中涉及的离子方程式为NH3·H2O+H+=NH4++H2O、_____________、___________。
(3)步骤中,所加(NH4)2S的浓度不宜过大的原因是______________。
(4)滤液2中,c(Co2+):c(Ni2+)=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物。该电池放电过程产生MnOOH。回收处理该废电池可得到多种化工原料。有关数据如表所示:
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-17 | 10-17 | 10-39 |
用废电池的锌皮制备ZnSO4·7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是加稀H2SO4和H2O2溶解,铁变为________,加碱调节pH为________时,铁刚好沉淀完全(离子浓度小于1×10-5 mol·L-1时,即可认为该离子沉淀完全);继续加碱至pH为________时,锌开始沉淀(假定Zn2+浓度为0.1 mol·L-1)。若上述过程不加H2O2后果是______________,原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水FeCl2易吸湿、易被氧化,常作为超高压润滑油的成分。某实验小组利用无水FeCl3和氯苯(无色液体,沸点132.2℃)制备少量无水FeCl2,并测定无水FeCl2的产率。
实验原理:2FeCl3+C6H5Cl![]() 2FeCl2+C6H4Cl2+HCl↑
2FeCl2+C6H4Cl2+HCl↑
实验装置:按如图所示组装好的装置,检查气密性后,向三颈烧瓶A中加入16.76g无水FeCl3和22.5g氯苯。
回答下列问题:
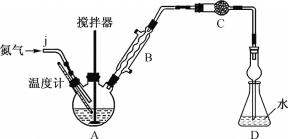
(1)利用工业氮气(含有H2O、O2、CO2)制取纯净干燥的氮气。
①请从下列装置中选择必要的装置,确定其合理的连接顺序:a→________→上图中的j口(按气流方向,用小写字母表示)。
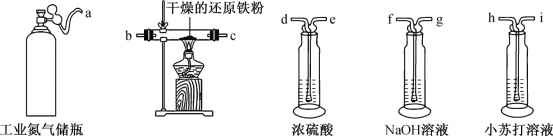
②实验完成后通入氮气的主要目的是________。
(2)装置C中的试剂是________(填试剂名称),其作用是________。
(3)启动搅拌器,在约126℃条件下剧烈搅拌30min,物料变成黑色泥状。加热装置A最好选用__(填字母)。
a.酒精灯 b.水浴锅 c.电磁炉 d.油浴锅
(4)继续升温,在128~139℃条件下加热2h,混合物颜色逐渐变浅,黏度降低。该步骤中加热温度已经接近或超过氯苯沸点,但氯苯实际损失量却非常小,其原因是________。
(5)继续加热1h后放置冷却,在隔绝空气条件下过滤出固体,用洗涤剂多次洗涤所得固体,置于真空中干燥,得到成品。若D中所得溶液恰好与25mL2.0mol·L-1NaOH溶液完全反应,则该实验中FeCl2的产率约为________(保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家研发出一种新型水溶液锂电池,采用复合膜包裹的金属锂作负极,锰酸锂(LiMn2O4)作正极,以0.5 mol/Li2SO4 水溶液作电解质溶液。电池充、放电时,LiMn2O4与Li2Mn2O4可以相互转化。下列有关该电池的说法正确的是
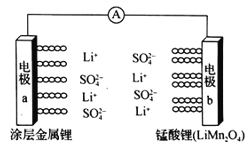
A. 该电池放电时,溶液中的SO42-向电极b移动
B. 该电池负极的电极反应式为:2Li+2H2O==2LiOH+H2↑
C. 电池充电时,外加直流电源的正极与电极a相连
D. 电池充电时,阳极的电极反应式为:Li2Mn2O4-e-==LiMn2O4 +Li+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯磺酸(HSO3Cl)是无色液体,密度为1.79gcm-3,其沸点约152℃:氯磺酸有强腐蚀性,遇潮湿空气生成浓烈的白雾,它属于危险品。制取氯碘酸是在常温下将干燥的氯化氢气体通入溶有三氧化硫的硫酸(发烟硫酸)中,氯化氢与三氧化硫化合即得氯磺酸。在实验室里制取氯磺酸可用如图所示的装置(图中衬垫、夹持和固定仪器均已略去)。
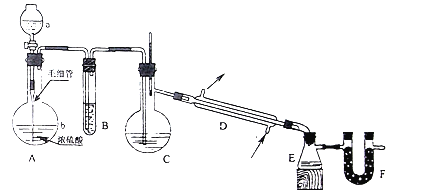
所用到的试剂有:①密度为1.19gcm-3的浓盐酸;②密度为1.84gcm-3质量分数为98.3%的浓硫酸(98.3%的浓硫酸沸点是338℃;③发烟硫酸;④无水氯化钙:⑤水;⑥碱石灰。试填空:
(1)对应仪器中应盛入的试剂或药品(填名称):
a中为______,B中为______,C中为______,F中为______;
(2)A中的分液漏斗下端接有的毛细管的作用是:______,若不用毛细管直接用分液漏斗注入a中液体,可能发生的现象是______,利用生活用品改进实验装置,若将分液漏斗换为______,还能更好的控制反应发生;
(3)写出实验室制备氯磺酸的化学方程式______,一定程度时需用酒精灯在C装置下加热的作用是:______;
(4)如果C中的温度计换成温度传感器,作用是:______;
(5)如果不加F装置可能产生大量烟雾,用化学用语解释原因______;
(6)若F中加无水氯化钙,F后______(填有或没有)必要加装HCl的吸收装置。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四溴化钛(TiBr4)可用作橡胶工业中烯烃聚合反应的催化剂。已知TiBr4常温下为橙黄色固体,熔点为38.3℃,沸点为233.5℃,具有潮解性且易发生水解。实验室利用反应TiO2+C+2Br2![]() TiBr4+CO2制备TiBr4的装置如图所示。回答下列问题:
TiBr4+CO2制备TiBr4的装置如图所示。回答下列问题:
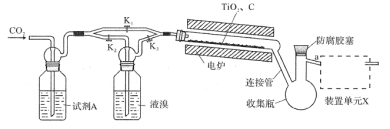
(1)检查装置气密性并加入药品后,加热前应进行的操作是__,其目的是__,此时活塞K1,K2,K3的状态为__;一段时间后,打开电炉并加热反应管,此时活塞K1,K2,K3的状态为____。
(2)试剂A为__,装置单元X的作用是__;反应过程中需用热源间歇性微热连接管,其目的是___。
(3)反应结束后应继续通入一段时间CO2,主要目的是___。
(4)将连接管切断并熔封,采用蒸馏法提纯。此时应将a端的仪器改装为__、承接管和接收瓶,在防腐胶塞上加装的仪器是___(填仪器名称)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com