
【题目】化学与社会、生活密切相关,下列说法正确的是
A. 通过浸渍水玻璃的方法防止木材腐朽
B. 宣纸的主要成分为蛋白质,酸性条件下易水解
C. 地沟油的主要成分与柴油的主要成分相同,所以地沟油可用于制生物柴油
D. SO2有毒,不能用作食品漂白剂和食品防腐剂添加在粉条、红酒等食品饮料中
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究NH3的性质具有重要意义。请回答下列问题:
(1)已知:①NH3 (g)+3O2(g)=2N2(g)+6H2O(g) △H=-1266.5kJ·mol-1
②N2(g)+O2(g)=2NO(g) △H=+180.5 kJ·mol-1
写出氨高温催化氧化生成NO的热化学方程式___________。
(2)氨气、空气可以构成燃料电池,其电池反应原理为:4NH3+302=2N2+6H2O。已知电解质溶液为KOH溶液,则负极的电极反应式为________。
(3)合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的化学平衡常数K值和温度的关系如下:

由上表数据可知该反应的△H_______ 0 填“> ”、“< ”或“=”) ;
理论上,为了增大平衡时H2的转化率,可采取的措施是_______(选填字母);
A.增大压强 B.使用合适的催化剂 C.升高温度 D.及时分离出产物中的NH3
③400℃时,测得某时刻氨气、氮气、氢气的物质的量浓度分别为3mol·L-1、2 mol·L-1、l mol·L-1,此时刻该反应的V正(N2)=______ V逆(N2)。(填“>”、“<”或“=”)。
(4)已知25℃时,Ksp[Fe(OH)3]=1.0×l0-38, Ksp[Al(OH)3]=3.0×l0-34,当溶液中的金属离子浓度小于1.0×10-5mol·L-1时,可以认为沉淀完全。在含Fe3+、A13+的浓度均为1. 05mol·L-1的溶液中加入氨水,当Fe3+完全沉淀时,A13+沉淀的百分数____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种黑色粉末氧化铜、氧化亚铁、二氧化锰、石墨粉,只需加入一种试剂即可将它们区别开来, 这种试剂是( )
A. 氢氧化钠溶液 B. 稀硫酸
C. 浓盐酸 D. 蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.1 mol·L-1NaOH溶液分别滴定体积均为20mL、浓度均为0.1 mol·L-1HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积关系如图(P为曲线I上的点,M、N为曲线II上的点),下列说法不正确的是
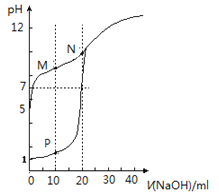
A. HX为弱酸
B. 将P点和N点的溶液混合,所得溶液呈酸性
C. M 点 c(HX)-c(X-)>c(OH-)-c(H+)
D. 向 N点溶液中通入HCl至 PH = 7:c(Na+)>c(HX)=c(Cl-)>c(X-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】⑴下列有机实验操作或叙述,正确的是________________(填写代号)
A、用新制氢氧化铜悬浊液检验糖尿病患者现象是有黑色沉淀生成。
B、乙酸乙酯中少量乙酸可用饱和Na2CO3溶液除去
C、蔗糖水解时应用浓H2SO4作催化剂
D、在鸡蛋白溶液中滴入浓HNO3,加热会产生黄色物质
E、在植物油中滴入溴水,溴水褪色
F、用盐析法分离油脂皂化反应的产物
⑵实验室制乙烯:
①反应的方程式:_____________________________________
②浓H2SO4的作用:___________________________________
③发生装置中的温度计应插在:_________________________________
④实验中要使温度迅速升到170℃的原因是:__________________________
⑤反应时混合液逐渐变黑,是乙醇发生变化产生的气体有明显的刺激性气味,
所以,制备的乙烯中混有______________气体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质间的转化,能通过一步反应实现的是
A. S→SO3 B. Fe→FeCl2 C. CuO→Cu(OH)2 D. SiO2→H2SiO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅酸的说法正确的是( )
A. 硅酸是一种不溶于水的含氧酸 B. 硅酸不溶于水,是一种非电解质
C. 硅酸的酸性比碳酸强 D. 硅酸可由二氧化硅与水反应制得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO、NO2 和CO均为大气污染物,对其治理备受关注。请回答下列问题:
I.碱液吸收法
(1)NaOH溶液可将NO和NO2的混合气体转化为NaNO2,该反应的离子方程式为_________________________________________。
(2)25℃时,HNO2的电离常数Ka=4.6×10-4。常温下,向NaNO2溶液中滴加盐酸至溶液的pH=3时,溶液中![]() =_________(保留两位有效数字)
=_________(保留两位有效数字)
Ⅱ.已知综合治理NO和CO的原理为
i. 2NO(g)+2CO(g)![]() N2(g)+2CO2 (g) △H=-746.5kJmol-1
N2(g)+2CO2 (g) △H=-746.5kJmol-1
ii. C(s)+ 2NO(g)![]() N2(g)+ CO2 (g) △H= +172.5 kJmol-1
N2(g)+ CO2 (g) △H= +172.5 kJmol-1
(3)高温下,1mol C(s)与CO2 完全反应生成CO的热化学方程式为________________________。
(4)一定条件下,某密闭容器中发生反应i和反应ii。达到平衡后,其他条件不变,升高温度,CO的体积分数_______(填“增大”“ 减小”或“无影响”)。
(5)一定条件下,恒容密闭容器中发生反应i。若起始充入的![]() =y,NO的平衡转化率(a)与y和温度(T)的关系如图所示。
=y,NO的平衡转化率(a)与y和温度(T)的关系如图所示。

①y1_____y2(填“>”“<”或“=”)
②M点和N点对应的该反应速率:M_________N(填“>”“<”或“=”)
(6)t℃时,向容积为10L的恒压密闭容器中加入1mol C(s)和2molNO(g),发生反应ii。5min达到平衡时,测得0~5min内,用CO2表示的该反应速率v(CO2)=0.016 molL-1·min-1;N2的体积分数为a。则:
①t℃时,该反应的平衡常数K=_____________。
②若保持条件不变,起始向该容器中按下列配比加入物质,达到平衡时,N2的体积分数仍为a的是____________________(填选项字母)
A.0.5molC和2mol NO B.2mol N2和2mol CO2
C.1 mol C、1 mol N2和1mol CO2 D.1 mol C、1 mol NO和1mol N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有以下物质相互转化
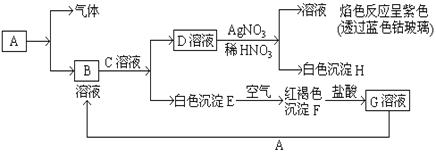
(1)A转化为B及气体这步反应中应加入的试剂是_______(填名称)。
(2)写出B的化学式_______ D的化学式_______
(3)写出由E转变成F的化学方程式_____________________________
(4)写出向G溶液中加入A的有关离子反应方程式是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com