
����Ŀ��ij�о�С�鰴����·�ߺϳ���ʹҩ�����M��

��֪����.R��NH2+![]()
![]() RNHCH2CH2OH
RNHCH2CH2OH
��.![]()
��1��A��B�Ļ�ѧ����ʽ��__��
��2��B��C�ķ�Ӧ������__��
��3��D�ĺ˴Ź�������ֻ��һ�����շ壬��ṹ��ʽ��__��
��4��D��E�Ļ�ѧ����ʽ��__��
��5��G�к���������Ԫ������ṹ��ʽ��__��
��6��I��H��Ӧ������ʹҩ�����M�Ļ�ѧ����ʽ��__��
��7��д��ͬʱ��������������C��ͬ���칹��Ľṹ��ʽ__��д��һ�ּ��ɣ���
�ٷ������б������DZ�����λ��ȡ���
�ں˴Ź������ױ�����������6����ԭ�ӣ����������ʾ����̼��˫����C��N����
��8����CΪԭ�Ͽ��Ժϳ���Ҫ��ҽҩ�м�����������ᣬ�ϳ�·�����£�
![]()
��д��Y�Ľṹ��ʽ__��
�ںϳ�·���з�Ӧ����Fe/HCl��������__��
���𰸡�![]() +Cl2
+Cl2![]() +HCl ȡ����Ӧ
+HCl ȡ����Ӧ ![]() 2
2![]() +CH3NH2
+CH3NH2![]()
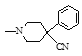
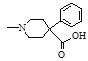 +CH3CH2OH
+CH3CH2OH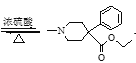 +H2O
+H2O ![]() ��
��![]() ��
��![]() ������һ�֣�
������һ�֣� ![]() ��������-NO2����ԭΪ������-NH2��
��������-NO2����ԭΪ������-NH2��
��������
C��F������Ϣ�еķ�Ӧ����G��G�к���-CN��G����ˮ�ⷴӦ����H��H�к���-COOH�����H��I������������������Ľṹ��ʽ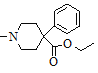 ����֪H��I����������Ӧ�����C��F����̼ԭ����Ŀ����֪IΪCH3CH2OH��HΪ
����֪H��I����������Ӧ�����C��F����̼ԭ����Ŀ����֪IΪCH3CH2OH��HΪ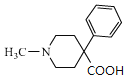 ������л������ʽ���ƿ�֪GΪ
������л������ʽ���ƿ�֪GΪ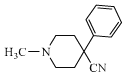 ��CΪ
��CΪ![]() ��FΪ
��FΪ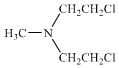 ��EΪ
��EΪ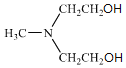 ����C�Ľṹ�����A���ӽṹ�к��б�������AΪ
����C�Ľṹ�����A���ӽṹ�к��б�������AΪ![]() ��A��Cl2�ڹ��������·���ȡ����Ӧ���ɵ�BΪ
��A��Cl2�ڹ��������·���ȡ����Ӧ���ɵ�BΪ![]() ����ϩ��O2�ڴ����������·���������Ӧ���ɵ�D�˴Ź�������ֻ��һ�����շ壬��DӦΪ
����ϩ��O2�ڴ����������·���������Ӧ���ɵ�D�˴Ź�������ֻ��һ�����շ壬��DӦΪ![]() ��D�ٺ�CH3NH2������Ϣ���ķ�Ӧ����E���ݴ˷������⣻
��D�ٺ�CH3NH2������Ϣ���ķ�Ӧ����E���ݴ˷������⣻
(8)��![]() Ϊԭ�Ϻϳɵ����ղ���Ϊ���������ᣬ��C��ŨHNO3��Ũ�����ϼ������ɵ�XӦΪ
Ϊԭ�Ϻϳɵ����ղ���Ϊ���������ᣬ��C��ŨHNO3��Ũ�����ϼ������ɵ�XӦΪ![]() ��X��������Һ��ˮ�����ɵ�YΪ
��X��������Һ��ˮ�����ɵ�YΪ![]() ��Y����Fe/HCl�������·�����ԭ��Ӧ����
��Y����Fe/HCl�������·�����ԭ��Ӧ����![]() ��
��
(1)A��Cl2�ڹ��������·���ȡ����Ӧ���ɵ�BΪ![]() ��������Ӧ�Ļ�ѧ����ʽ��
��������Ӧ�Ļ�ѧ����ʽ��![]() +Cl2
+Cl2![]() +HCl��
+HCl��
(2)![]() ��NaCN����ȡ����Ӧ����
��NaCN����ȡ����Ӧ����![]() ��
��
(3)�ɷ���֪����ϩ��O2�ڴ����������·���������Ӧ���ɵ�D�ṹ��ʽΪ![]() ��
��
(4)D��EΪ![]() ��CH3NH2�����ӳɷ�Ӧ����
��CH3NH2�����ӳɷ�Ӧ���� ����Ӧ����ʽ��2
����Ӧ����ʽ��2![]() +CH3NH2
+CH3NH2![]() ��
��
(5)�ɷ�����֪��G�Ľṹ��ʽ�� ��
��
(6)CH3CH2OH�� ����������Ӧ������ʹҩ����वĻ�ѧ����ʽ��
����������Ӧ������ʹҩ����वĻ�ѧ����ʽ��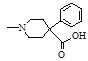 +CH3CH2OH
+CH3CH2OH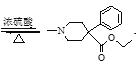 +H2O��
+H2O��
(7)C(![]() )��ͬ���칹����ϣ��ٷ������б��������DZ�������λ��ȡ�����1H-NMR�ױ�����������6����ԭ�ӣ�IR����ʾ����̼��˫��(C=N)�����ܵ�ͬ���칹���У�
)��ͬ���칹����ϣ��ٷ������б��������DZ�������λ��ȡ�����1H-NMR�ױ�����������6����ԭ�ӣ�IR����ʾ����̼��˫��(C=N)�����ܵ�ͬ���칹���У�![]() ��
��
(8)���ɷ���֪Y�Ľṹ��ʽΪ![]() ��
��
��![]() �ڷ�Ӧ����Fe/HCl�������£�������(-NO2)��ԭΪ����(-NH2)��
�ڷ�Ӧ����Fe/HCl�������£�������(-NO2)��ԭΪ����(-NH2)��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ��(��Ҫ�ɷ�CuFeS2)����ȡCu����Ҫԭ�ϡ�
��֪��2CuFeS2+4O2![]() Cu2S+3SO2+2FeO����
Cu2S+3SO2+2FeO����
����Cu2S��1200 ������¼�����Ӧ��2Cu2S+3O2==2Cu2O+2SO2 ����
2Cu2O+Cu2S==6Cu +SO2�� ������
�ٶ�������Ӧ����ȫ��������˵����ȷ����
A. ��Ӧ����CuFeS2������ԭ��
B. ȡ12.5g��ͭ����Ʒ�����ⶨ��3.60g���������CuFeS2��������һ��Ϊ82.8%
C. ��6molCuFeS2����6molCu����O2�����ʵ���Ϊ14.25mol
D. 6molCuFeS2��15.75molO2��Ӧ�������Ͽɵõ�ͭ�����ʵ���Ϊ3mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��ZΪ������Ԫ�أ�X��������������Yԭ��������������2����Y��ԭ��������X��ԭ��������5��Zԭ�ӵ�������������Y��3������������ȷ���ǣ� ��
A.ԭ�Ӱ뾶�Ĵ�С˳��Y��Z��X
B.Z������X����ֱ�ӷ�Ӧ���������ֻ�����
C.��ҵ�ϣ����X��Y�γɵĻ�������ȡY����
D.Y��ZԪ�ص�����������ˮ���ﲻ�ܻ��෴Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����Ȼ�ѧ����ʽ��
�� H2(g)��1/2O2(g)=H2O(l) ��H����285 kJ/mol
�� H2(g)��1/2O2(g)=H2O(g) ��H����241.8 kJ/mol
�� C(s)��1/2O2(g)=CO(g) ��H����241.8 kJ/mol
�� C(s)��O2(g)=CO2(g) ��H����393.5 kJ/mol
�ش����и�������
��1��������Ӧ�����ڷ��ȷ�Ӧ����_______________��
��2��H2��ȼ����Ϊ____________________��C��ȼ����Ϊ__________________��
��3��ȼ��10 g H2����Һ̬ˮ���ų�������Ϊ___________________��
��4��CO��ȼ����Ϊ_________________�����Ȼ�ѧ����ʽΪ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(��)��֪��448 ��ʱ����ӦH2(g)��I2(g)![]() 2HI(g)��ƽ�ⳣ��K1Ϊ49������¶��·�Ӧ2HI(g)
2HI(g)��ƽ�ⳣ��K1Ϊ49������¶��·�Ӧ2HI(g)![]() H2(g)��I2(g)��ƽ�ⳣ��K2Ϊ________����Ӧ1/2H2(g)��1/2I2(g)
H2(g)��I2(g)��ƽ�ⳣ��K2Ϊ________����Ӧ1/2H2(g)��1/2I2(g)![]() HI(g)��ƽ�ⳣ��K3Ϊ______________________________________��
HI(g)��ƽ�ⳣ��K3Ϊ______________________________________��
(��)��һ��������ܱ������н������»�ѧ��Ӧ��CO2(g)��H2(g)![]() CO(g)��H2O(g)���仯ѧƽ�ⳣ��(K)���¶�(t)�Ĺ�ϵ���±���ʾ��
CO(g)��H2O(g)���仯ѧƽ�ⳣ��(K)���¶�(t)�Ĺ�ϵ���±���ʾ��
t/�� | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
(1)�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��________��
(2)�÷�ӦΪ________(��������������������)��Ӧ��
(3)���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������________��
A��������ѹǿ����
B�����������c(CO)����
C��v��(H2)��v��(H2O)
D��c(CO2)��c(CO)
(4)ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c(CO2)��c(H2)��c(CO)��c(H2O)�����жϴ�ʱ���¶�Ϊ________ ����
(5)��800 ��ʱ������������Ӧ��ijһʱ�̲�������ڸ����ʵ�Ũ�ȷֱ�Ϊc(CO2)Ϊ2 mol��L��1��c(H2)Ϊ1.5 mol��L��1��c(CO)Ϊ1 mol��L��1��c(H2O)Ϊ3 mol��L��1������һʱ�̣���Ӧ��________(��������������������)���С�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����( )
A.��֪�����ۻ���Ϊ![]()
![]() �������������Ϊ20
�������������Ϊ20![]() ������1mol������2mol��������ۻ�����ȫ�����ƻ���������������ֻ���ƻ�����
������1mol������2mol��������ۻ�����ȫ�����ƻ���������������ֻ���ƻ�����![]() �����
�����
B.��֪��![]() ʯī
ʯī![]() ��
��![]()
![]() ��
��![]() ��
��![]()
![]() ��
��![]() ʯī
ʯī![]() ��
��![]()
![]() ����
����![]() ��
��![]()
![]()
C.ʵ���û�����![]() ������ϩ
������ϩ![]() �ͱ�
�ͱ�![]() �ı�ȼ���ȷֱ�Ϊ
�ı�ȼ���ȷֱ�Ϊ![]()
![]() ��
��![]()
![]() ��
��![]()
![]() ������֤���ڱ������в����ڶ�����̼̼˫��
������֤���ڱ������в����ڶ�����̼̼˫��
D.��֪һ���¶��£�������Һ�����ʵ���Ũ��Ϊc�������Ϊ![]() ��
��![]() ���������������ƹ��壬��
���������������ƹ��壬��![]() �����ƶ���
�����ƶ���![]() ��С��Ka��С
��С��Ka��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������,��10mL pH=11��NH3��H2O��Һ�м�����������,��������Һ�ķ�����ȷ����( )
��������� | ��������Һ�ķ��� | |
A. | 90mL H2O | ��ˮ�������c(H+)=10-10mol��L-1 |
B. | 0.1mol NH4Cl���� | c(H+)��ԭNH3��H2O��Һ�еĴ� |
C. | 10mL pH=13��NaOH��Һ | NH3��H2O�ĵ���̶Ȳ��� |
D. | 10mL pH=3������ | ��Һ������ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A�Ļ�ѧʽΪNH5,������ԭ�ӵ�������Ӳ�ṹ��������Ӧϡ������Ԫ��ԭ�ӵ�������Ӳ�ṹ,�������й�˵������ȷ���ǣ�������
A.1 mol NH5�к���5NA��N��H������NA��ʾ�����ӵ�������ֵ��
B.NH5�м��й��ۼ��������Ӽ�
C.NH5�ĵ���ʽΪ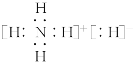
D.NH5��ˮ��Ӧ�����ӷ���ʽΪNH4++H-+H2O=NH3��H2O+H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֡�
̼ | �� | Y | |
X | �� | Z |
���������գ�
��1����ԭ�ӵĺ�������Ų�ʽΪ__����ԭ�ӵĺ������ռ��__�������ZԪ����Ԫ�����ڱ��е�λ��Ϊ__��Yԭ�Ӻ�����______��������ͬ�ĵ��ӡ�
��2��H2S������H-S������Ϊ92�㣬˵��H2S������__������������Ǽ����������ӡ�
��3��������ʵ��˵��YԪ�صķǽ����Ա���Ԫ�صķǽ�����ǿ����__��
a��Y������H2S��Һ��Ӧ����Һ�����
b����������ԭ��Ӧ�У�1molY���ʱ�1mol���ʵõ��Ӷ�
c��Y������Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
��4��X��Z��Ԫ�صĵ��ʷ�Ӧ����0.1molX����ۻ�����ָ������£�����68.7kJ����֪�û�������ۡ��е�ֱ�Ϊ-69���58�棬д���÷�Ӧ���Ȼ�ѧ����ʽ___��
��5��̼������Һ�е����̪����Һ�Ժ�ɫ���������ӷ���ʽ���Ͳ����������ԭ��___����������ɫ����Һ�м��������Ȼ��ƹ��壬��Һ��ɫ��dz������ƽ�����۽��Ͳ����������ԭ��___��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com