
【题目】叠氮化钠(NaN3)是一种应用广泛的化工产品,可用于合成抗生素头孢菌素药物的中间体,汽车安全气囊等。
Ⅰ.实验室制备NaN3
(1)实验原理:
①把氨气通入熔融金属钠反应制得氨基钠(NaNH2),该反应的化学方程式为____________。
②将生成的NaNH2与N2O在210℃-220℃下反应可生成NaN3、NaOH和气体X,该反应的化学方程式为2NaNH2+N2O═NaN3+NaOH+X,实验室检验X气体使用的试纸是湿润的______。
(2)实验装置(图1)、步骤如下,回答下列问题:
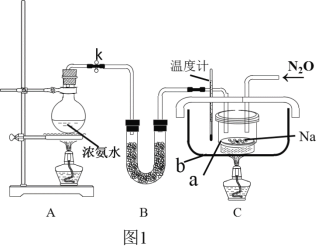
已知:i)NaN3是一种易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
ii)NaNH2的熔点为210℃,沸点为400℃,在水溶液中易水解。
①组装仪器检查装置气密性后,装入药品。装置B中盛放的药品是_______________。
②实验过程应先点燃___(填“A”或“C”)处的酒精灯,理由是_______________________。
③让氨气和熔化的钠充分反应后,停止加热A并关闭止水夹k。向装置C中b容器内充入加热介质植物油并加热到210℃-220℃,然后按图通入N2O;
④装置C反应完全结束后,冷却,取出a中的混合物进行以下操作,得到NaN3固体:

操作II的目的是____________;
操作IV中选用的洗涤试剂最好的是_____。
A.水 B.乙醇 C.乙醇水溶液 D.乙醚
(3)图中仪器a用不锈钢材质的而不用玻璃的,其主要原因是____________________。
II.产品NaN3纯度测定
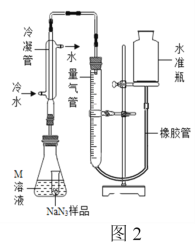
精确称量0.150 g NaN3样品,设计如图2所示装置,连接好装置后使锥形瓶倾斜,使小试管中的NaN3样品与M溶液接触,测量产生的气体体积从而测定其纯度。
已知2 NaN3→ 3N2(NaN3中的N全部转化为N2,其他产物略),反应中放出大量的热。
(4)使用冷水冷凝的目的是______。对量气管读数时,反应前后都需要进行的操作是______。
(5)常温下测得量气管读数为60.0 mL(N2的密度为1.40 g/L)计算NaN3样品的纯度为______。(保留三位有效数字)
【答案】2NH3+2Na![]() 2NaNH2+H2↑ 红色石蕊试纸 碱石灰 A 先产生NH3,排除装置内空气,防止产品不纯 降低NaN3的溶解量或溶解度或促使NaN3析出 D 反应过程生成的NaOH能腐蚀玻璃 冷却生成的气体 调节量气管使两侧的液面保持水平 86.7%
2NaNH2+H2↑ 红色石蕊试纸 碱石灰 A 先产生NH3,排除装置内空气,防止产品不纯 降低NaN3的溶解量或溶解度或促使NaN3析出 D 反应过程生成的NaOH能腐蚀玻璃 冷却生成的气体 调节量气管使两侧的液面保持水平 86.7%
【解析】
Ⅰ.(1)①氨气通入熔融金属钠反应制得氨基钠(NaNH2)和氢气,结合原子守恒即可得发生反应的化学方程式;②根据质量守恒定律和氨水呈碱性回答;(2)①氨气选择碱石灰干燥;②先点燃A产生氨气将装置内空气驱赶除去,防止产品不纯;④根据叠氮化钠(NaN3)固体易溶于水,微溶于乙醇,不溶于乙醚,可知乙醇可降低NaN3的溶解度促使NaN3析出,乙醚洗涤叠氮化钠可减少叠氮化钠的损失;(3)玻璃中的SiO2能于NaOH溶液反应生成硅酸钠;(3)反应过程生成的NaOH能腐蚀玻璃,则仪器a应用不锈钢材质的而不用玻璃的;II.(4)反应可能产生水蒸气,使用冷水冷凝可除去生成的气体中的水蒸气;量气管读数前,需要平衡压强;(5)先根据体积和密谋计算氮气的体积,再利用关系式2NaN3→3N2计算NaN3样品的纯度。
Ⅰ.(1)①氨气通入熔融金属钠反应制得氨基钠(NaNH2)和氢气,则发生反应的化学方程式为2NH3+2Na![]() 2NaNH2+H2↑;②根据质量守恒定律,反应前后原子的种类和数目不变,可确定气体X为氨气,氨水呈碱性,检验时用湿润的红色石蕊试纸,现象是变蓝色;(2)①A中产生的氨气混有水蒸气,干燥氨气选择碱石灰,则在C中盛放的药品是碱石灰;②实验过程中先点燃A产生氨气将装置内空气驱赶除去,防止产品不纯;④C中混合物加水后,根据叠氮化钠(NaN3)固体易溶于水,微溶于乙醇,不溶于乙醚,NaN3溶解在水中,NaNH2与水反应生成NaOH和氨气,可知操作Ⅱ加乙醇可降低NaN3的溶解度促使NaN3析出;乙醚洗涤叠氮化钠可减少叠氮化钠的损失,故操作IV中选用的洗涤试剂最好的是D;II.(4)反应可能产生水蒸气,使用冷水冷凝的目的是除去生成的气体中的水蒸气;量气管读数前,需要调节量气管使两侧的液面保持水平,确保气体压强与外界大气压强相等。(5)生成氮气的质量为
2NaNH2+H2↑;②根据质量守恒定律,反应前后原子的种类和数目不变,可确定气体X为氨气,氨水呈碱性,检验时用湿润的红色石蕊试纸,现象是变蓝色;(2)①A中产生的氨气混有水蒸气,干燥氨气选择碱石灰,则在C中盛放的药品是碱石灰;②实验过程中先点燃A产生氨气将装置内空气驱赶除去,防止产品不纯;④C中混合物加水后,根据叠氮化钠(NaN3)固体易溶于水,微溶于乙醇,不溶于乙醚,NaN3溶解在水中,NaNH2与水反应生成NaOH和氨气,可知操作Ⅱ加乙醇可降低NaN3的溶解度促使NaN3析出;乙醚洗涤叠氮化钠可减少叠氮化钠的损失,故操作IV中选用的洗涤试剂最好的是D;II.(4)反应可能产生水蒸气,使用冷水冷凝的目的是除去生成的气体中的水蒸气;量气管读数前,需要调节量气管使两侧的液面保持水平,确保气体压强与外界大气压强相等。(5)生成氮气的质量为![]() =0.084g,
=0.084g,
设NaN3样品的纯度X
2NaN3 ![]() 2Na+3N2↑
2Na+3N2↑
13084
x0.150g0.084g
![]() 解得:x=86.7%。
解得:x=86.7%。


科目:高中化学 来源: 题型:
【题目】下列关于反应过程中能量变化的说法正确的是

A. 图中a、b曲线可分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g) ΔH<0使用和未使用催化剂时,反应过程中的能量变化
B. 己知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2。则ΔH1>ΔH2
C. 同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同
D. 在一定条件下,某可逆反应的ΔH=+100kJ·mol-1,则该反应正反应活化能比逆反应活化能大100kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷是一种理想的洁净燃料,利用甲烷与水反应制备氢气,因原料廉价,具有推广价值。该反应为CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H>0
CO(g)+3H2(g) △H>0
(1)800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如表。则此时正、逆反应速率的关系是____。
CH4 | H2O | CO | H2 |
3.0molL-1 | 8.5molL-1 | 2.0molL-1 | 2.0molL-1 |
(2)为了探究温度、压强对上述化学反应速率的影响,某同学设计了以下三组对比实验(温度为360℃或480℃、压强为101 kPa或303 kPa,其余实验条件见下表)。
实验序号 | 温度/℃ | 压强/kPa | CH4初始浓度/ molL1 | H2O初始浓度/ molL1 |
1 | 360 | p | 2.00 | 6.80 |
2 | t | 101 | 2.00 | 6.80 |
3 | 360 | 101 | 2.00 | 6.80 |
表中t=____,P=_____;设计实验2、3的目的是________________;
实验l、2、3中反应的化学平衡常数的大小关系是____(用K1、K2、K3表示)。
(3)一定温度下,在容积2L且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容 器 | 甲 | 乙 |
反应物投入量 | 1molCH4、1molH2O | a molCH4、a molH2O、b molCO、c molH2 |
经测定甲容器经过5min达到平衡,平衡后甲中气体的压强为开始的1.2倍,甲容器中该反应在5min内的平均速率υ(H2)=_______,若要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则b的取值范围为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下列装置完成了浓硫酸和SO2性质实验(夹持装置已省略):
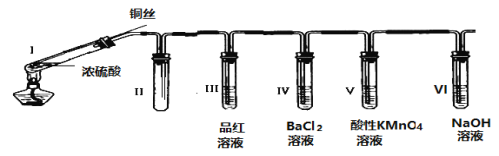
请回答:
(1)连接好装置后,接下来的操作步骤是________________
(2)浓硫酸与铜丝反应的化学方程式为________________
(3)装置II的作用是________________
(4)下列说法正确的是________________
A 反应一段时间后,向试管Ⅰ中的溶液加水,溶液呈蓝色
B 试管III、V中溶液都会褪色,其褪色原理相同
C 取下试管IV并不断振荡,试管中出现浑浊,是因为生成了BaSO4
D 试管VI中NaOH溶液用于吸收尾气,可用Na2CO3溶液代替
(5)某同学根据所学化学知识认为:反应完毕时,不管铜是否过量,硫酸一定有剩余。下列药品能证明反应结束时I试管中确有余酸的是________________
A BaCl2溶液 B 铁粉 C NaHCO3溶液 D 银粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体中可能含有Na+、K+、Mg2+、Ba2+、 SO42-、CO32-、SO32-、SiO32-等离子,将其配成100mL溶液。学生研究性学习小组为了确认其成分,设计并完成了如图所示实验:

请回答下列问题:
(1)实验中最关键的“定容”操作:当液面接近容量瓶刻度线1-2cm处,________再将容量瓶塞盖好,反复上下颠倒,摇匀。
(2)根据以上实验可得出:一定存在的离子是________,一定不存在的离子是________
(3)下列实验结论符合事实的是________________
A.该固体中可能含有Na2SiO3、K2CO3
B.该固体中一定含有Na2SiO3、K2CO3
C.该固体中可能含有Na2SiO3、K2CO3、K2SO4
D.该固体中可能只含有Na2SiO3、Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大。X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子单电子数在同周期元素中最多,W与Z同周期,第一电离能比Z的低,R与Y同一主族,Q的最外层只有一个电子,其他电子层电子均处于饱和状态。请回答下列问题:
(1)Q+核外电子排布式为__________________。
(2)ZX3分子的空间构型为__________________, ZW3-离子的立体构型是__________。
(3)Y、R的最高价氧化物的沸点较高的是_______(填化学式),原因是_____________。
(4)将Q单质的粉末加入到ZX3的浓溶液中,并通入W2,充分反应后溶液呈深蓝色,该反应的离子方程式为:______________________________________________。
(5)W和Na的一种离子化合物的晶胞结构如图,该离子化合物为________(填化学式)。Na+的配位数为________,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为__________。
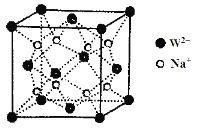
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“即食即热型快餐”适合外出时使用,其内层是用铝箔包裹并已加工好的真包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线使这两种化学物质发生反应,放出的热量便可对食物进行加热,这两包化学物质最适合的选择是
A.浓硫酸和水B.生石灰和水C.熟石灰和水D.氯化钠和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生产生活中,我们会遇到各种各样的化学反应。请按要求完成相应的化学方程式(是离子反应的用离子方程式表示):
(1)金属镁在二氧化碳中燃烧的化学方程式: _____________________________
(2)氯化铵是一种常用化肥,与强碱(NaOH)加热(离子方程式)___________________。
(3)工业上以氯气和石灰乳为原料制造漂白粉____________________________________________。
(4)用FeCl3 溶液与铜反应制作印刷电路板离子方程式__________________________。
(5)碳与二氧化硅在高温条件下反应___________________________________。
(6)工业上电解饱和食盐水制取氯气的离子方程式为_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用双线桥法表示下列反应的电子转移情况并将其改写成离子方程式:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,________________________,离子方程式为________________________。当3.84gCu被氧化时,__________gHNO3被还原,产生标准状况下的气体________L,转移电子数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com