
【题目】火电站是电力的主要来源之一,火电站是利用煤燃烧进行发电,同时产生污染物。下图是火电站的工作示意图:下列叙述不正确的是( )

A.火电站产生的SO2、NO2等气体能形成酸雨
B.加高火电站的烟囱可减少尾气中CO的含量
C.静电沉淀器除尘利用了胶体的性质
D.向煤中加入CaO,可以减少SO2的排放
科目:高中化学 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义。
I.已知某些化学键的键能数据如下
化学键 | C=O | C—O | C—H | H—H | O—H |
键能/kJ·mol-1 | 745 | 351 | 415 | 436 | 462 |
则CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) ΔH = __________ kJ·mol-1
CH3OH(g) + H2O(g) ΔH = __________ kJ·mol-1
II.将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g) + 6H2(g)![]() CH3OCH3(g) + 3H2O(l)
CH3OCH3(g) + 3H2O(l)
(1)该反应化学平衡常数表达式K = __________。
(2)已知在某压强下,该反应在不同温度、不同投料比时,达平衡时CO2的转化率如图所示:

①该反应的ΔH __________ 0(填“>"或“<”)。
②若温度不变,减小反应投料比[n(H2)/n(CO2)],K值将____(填“增大”、“减小”或“不变”)。
(3)某温度下,向体积一定的密闭容器中通入CO2(g)与H2(g)发生上述反应,下列物理量不再发生变化时,能说明反应达到平衡状态的是__________。
A.二氧化碳的浓度 B.容器中的压强
C.气体的密度 D.CH3OCH3与H2O的物质的量之比
(4)某温度下,在体积可变的密闭容器中,改变起始时加入各物质的量,在不同的压强下,平衡时CH3OCH3(g)的物质的量如下表所示:
P1 | P2 | P3 | |
I.2.0 mol CO2 6.0 mol H2 | 0.10 mol | 0.04 mol | 0.02 mol |
II.1.0 mol CO22 | X1 | Y1 | Z1 |
III.1.0 mol CH3OCH3 3.0 mol H2O | X2 | Y2 | Z2 |
①P1 __________ P3(填“>”“<”或“=”);
②P2下,III中CH3OCH3的平衡转化率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,11.2 LHCl气体中含有的分子数为0.5NA
B.50 mL12 mol/L盐酸与足量Fe反应,转移电子数为0.3NA
C.将0.2 mol FeCl3制成胶体,所得胶体粒子数为0.2NA
D.常温常压下,5.6 g N2和CO混合物中所含有的原子数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A. HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
B. CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol
C. 需要加热才能发生的反应一定是吸热反应
D. 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质分离提纯的描述不正确的是

A.分离KCl和MnO2混合物的步骤:加水溶解、过滤,滤渣洗涤后干燥,滤液蒸发结晶
B.蒸馏提纯时温度计的位置如图1所示,收集的产品中混有低沸点杂质
C.NaCl晶体中混有少量KNO3杂质的分离方法为:加水溶解、蒸发结晶、趁热过滤、洗涤、干燥
D.萃取溴水时,加入适量CCl4,转移至分液漏斗中,如图2,用力振摇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等浓度的H2SO4、NaHSO4溶液,分别滴入两份相同的Ba(OH)2溶液中,其电导率与滴入溶液体积变化的曲线如图所示。下列分析正确的是( )
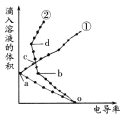
A.b→d反应的离子方程式为:H++OH-=H2O
B.d点溶液中,Na+与SO42-的物质的量之比为1:1
C.c点导电能力相同,所以两溶液中含有相同量的OH-
D.a、b两点Ba2+均沉淀完全,所以对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中分子数相同的是( )
A.2 L CO和2 L CO2B.9 g H2O和标准状况下11.2 L CO2
C.标准状况下1 mol O2和22.4 L H2OD.0.2 mol NH3和4.48 L HCl气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能鉴别 NH4Cl、Na2SO4、(NH4)2SO4、KCl 四瓶无色溶液的试剂是
A. Ba(OH)2溶液 B. AgNO3溶液 C. Ba(NO3)2溶液 D. NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20mL某物质的量浓度的AlCl3溶液中滴加2mol/LNaOH溶液时,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH溶液的体积(mL)和所得沉淀的物质的量(mol)的关系如图所示。则:

(1)写出OA段发生反应的离子方程式:OA段___,图中线段OP:PB=__,
(2)计算原AlCl3溶液的物质的量浓度为__mol/L,
(3)图中A对应的横坐标为__mL,
(4)当加入5mLNaOH溶液时,产生沉淀量为__mol,
(5)当加入的NaOH溶液过量时,使最初生成的沉淀部分溶解,要得到与(4)中相同的沉淀量,加入NaOH溶液的体积为__mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com