
【题目】合成高效、低毒农药杀灭菊酯(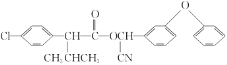 )流程如下:
)流程如下:
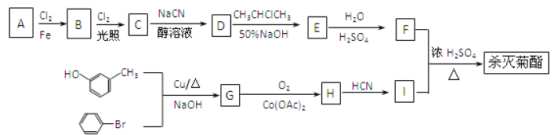
已知:
①R—X![]() RCN
RCN![]() RCOOH
RCOOH
②![]()
![]()
![]()
③![]()
![]()
![]()
④当苯环上连卤原子时,高温高压可以水解。
回答下列问题:
(1)按照系统命名法命名,B的名称是____;合成G的反应类型是________。
(2)有关A的下列说法正确的是________(填字母代号)。
a.A的所有原子可能处在同一平面上
b.A的核磁共振氢谱有5个峰
c.充分燃烧等质量的A和环己烷消耗氧气的量相等
d.A与苯互为同系物
e.A能使酸性KMnO4溶液褪色
(3)写出C在高温高压条件下与足量氢氧化钠水溶液充分反应的化学方程式:__________。
(4)写出反应F+I→杀灭菊酯的化学方程式:_______。
(5)H与银氨溶液水浴加热的离子方程式为:________。
(6)D在硫酸存在下发生水解生成J,符合下列要求的J的同分异构体有______种,并写出J的核磁共振氢谱为2: 2: 2: 1的所有结构简式:________。
①苯环上有两个取代基;②能水解成两种有机物;③可以发生银镜反应
【答案】4-氯甲苯 取代反应 de ![]() +3NaOH
+3NaOH![]() 2NaCl+H2O+
2NaCl+H2O+![]()
![]() +2[Ag(NH3)2]++2OH-
+2[Ag(NH3)2]++2OH-![]()
![]() +NH4++H2O+2Ag↓+3NH3 6
+NH4++H2O+2Ag↓+3NH3 6 ![]() 和
和![]()
【解析】
F与I在浓硫酸、加热条件下发生酯化反应生成杀灭菊酯,H发生信息⑵反应生成I,由杀灭菊酯的结构可知,F为![]() 、I为
、I为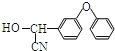 ,结合反应信息⑵可知H为
,结合反应信息⑵可知H为![]() ,G发生信息反应⑶生成H,则G为
,G发生信息反应⑶生成H,则G为![]() ,E发生信息⑴中第2步反应生成F,则E为
,E发生信息⑴中第2步反应生成F,则E为![]() ,C发生信息⑴中第1步反应生成D,D与CH3CHClCH3在氢氧化钠条件下反应生成E,根据E的结构可知,D为
,C发生信息⑴中第1步反应生成D,D与CH3CHClCH3在氢氧化钠条件下反应生成E,根据E的结构可知,D为![]() ,C为
,C为![]() ,A与氯气在Fe作催化剂条件下与氯气发生取代反应生成B,B与氯气在光照条件下生成C,故A为
,A与氯气在Fe作催化剂条件下与氯气发生取代反应生成B,B与氯气在光照条件下生成C,故A为![]() ,B为
,B为![]() ;
;
⑴B为![]() ,其名称是4-氯甲苯,合成G的反应类型是取代反应;故答案为:4-氯甲苯或;取代反应。
,其名称是4-氯甲苯,合成G的反应类型是取代反应;故答案为:4-氯甲苯或;取代反应。
⑵a. 甲苯的苯环上连的甲基,因此所有原子不可能处在同一平面上,故a错误;b. 甲苯有对称轴,核磁共振氢谱有4个峰,故b错误;c.等质量的甲苯和环己烷物质的量分别为![]() 、
、![]() ,C7H8—9O2,C6H12—9O2,物质的量不同,因此消耗氧气的量不相等,故c错误;d. 甲苯与苯互为同系物,故d正确;e. 甲苯能使酸性KMnO4溶液褪色,故e正确;综上所述,答案为de。
,C7H8—9O2,C6H12—9O2,物质的量不同,因此消耗氧气的量不相等,故c错误;d. 甲苯与苯互为同系物,故d正确;e. 甲苯能使酸性KMnO4溶液褪色,故e正确;综上所述,答案为de。
⑶C在高温高压、催化剂条件下与足量氢氧化钠水溶液充分反应的化学方程式为![]() +3NaOH
+3NaOH![]()
![]() +2NaCl+H2O;故答案为:
+2NaCl+H2O;故答案为:![]() +3NaOH
+3NaOH![]()
![]() +2NaCl+H2O。
+2NaCl+H2O。
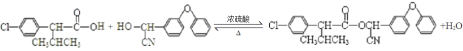
(4)反应F+I→杀灭菊酯的化学方程式: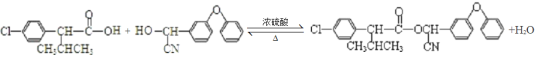 ;故答案为:
;故答案为: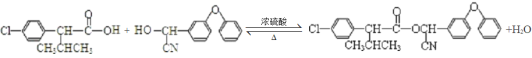 。
。
(5)H与银氨溶液水浴加热的离子方程式为:![]() +2[Ag(NH3)2]++2OH-
+2[Ag(NH3)2]++2OH-![]()
![]() +NH4++H2O+2Ag↓+3NH3;故答案为:
+NH4++H2O+2Ag↓+3NH3;故答案为:![]() +2[Ag(NH3)2]++2OH-
+2[Ag(NH3)2]++2OH-![]()
![]() +NH4++H2O+2Ag↓+3NH3。
+NH4++H2O+2Ag↓+3NH3。
(6)D在硫酸存在下发生水解生成J,则J为![]() ,符合下列要求的J的同分异构体:①苯环上有两个取代基;②能水解成两种有机物,含有酯基,③可以银镜反应,应含有甲酸形成的酯基,故符合条件J的同分异构体有:如果是间位取代基,则有
,符合下列要求的J的同分异构体:①苯环上有两个取代基;②能水解成两种有机物,含有酯基,③可以银镜反应,应含有甲酸形成的酯基,故符合条件J的同分异构体有:如果是间位取代基,则有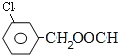 、
、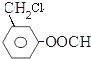 ,还有邻位、对位,共6种,J的核磁共振氢谱为2: 2: 2: 1的结构简式:
,还有邻位、对位,共6种,J的核磁共振氢谱为2: 2: 2: 1的结构简式:![]() 和
和![]() ;故答案为:6;
;故答案为:6;![]() 和
和![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
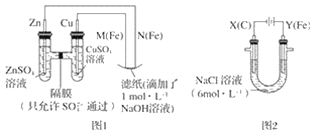
请回答:
Ⅰ.用图 1 所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是__(填字母序号)。
A 铝 B 石墨 C 银 D 铂
(2)N 极发生反应的电极反应式为__。
Ⅱ.用图 2 所示装置进行第二组实验。实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。 查阅资料得知,高铁酸根离子(FeO42-)在溶液中呈紫红色。
(3)电解过程中,X 极区溶液的 pH__(填“增大”“减小”或“不变”)。
(4)电解过程中,Y 极发生的电极反应之一为 Fe﹣6e﹣+8OH﹣= FeO42-+4H2O 若在 X 极收集到672 mL 气体,在 Y 极收集到 168 mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁电极)质量减少____g。
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2K2FeO4+3Z=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度(T℃)时,水的离子积为Kw=1×10-13。若将此温度下pH=11的苛性钠溶液a L与pH=1的稀硫酸b L混合(设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两种溶液的体积比。
(1)若所得混合溶液为中性,则a∶b=__;此溶液中各离子的浓度由大到小的排列顺序是_____。
(2)若所得混合溶液的pH=2,则a∶b=____;此溶液中各种离子的浓度由大到小的排列顺序是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸镍[(CH3COO)2Ni]是一种重要的化工原料。一种以含镍废料(含NiS、 Al2O3、FeO、CaO、SiO2 )为原料,制取醋酸镍的工艺流程图如下:
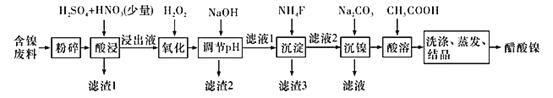
相关离子生成氢氧化物的pH和相关物质的溶解性如表:
金属离子 | 开始沉淀的pH | 沉淀完全的pH | 物质 | 20℃时的溶解性(H2O) |
Fe3+ | 1.1 | 3.2 | CaSO4 | 微溶 |
Fe2+ | 5.8 | 8.8 | NiF2 | 可溶 |
Al3+ | 3.0 | 5.0 | CaF2 | 难溶 |
Ni2+ | 6.7 | 9.5 | NiCO3 | Ksp=9.60×10-6 |
(1)粉碎含镍废料的作用是__________。
(2)酸浸过程中,1molNiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式:_____________。
(3)写出氧化步骤中加入H2O2发生反应的离子方程式:________。
(4)调节pH除铁、铝步骤中,溶液pH的调节范围是________。
(5)滤渣3主要成分的化学式是_________。
(6)沉镍过程中,若c(Ni2+ )=2.0 mol·L-1,欲使100 mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5 mol·L-1],则需要加入Na2CO3固体的质量最少为___________g(保留1位小数)。
(7)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如图。酸浸的最佳温度与时间分别为______℃、_______min。
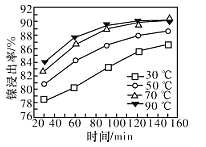
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸或硫酸和NaOH溶液的中和反应没有明显的现象。某学习兴趣小组的同学为了证明NaOH溶液与盐酸或硫酸发生了反应,从中和反应的热效应出发,设计了下面几种实验方案。请回答有关问题:
(1)方案一:如图装好实验装置,图中小试管用细线吊着,细线的上端拴在细铁丝上。开始时使右端U形管两端红墨水相平。实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内NaOH溶液混合,此时观察到的现象是________________________________,原因是______________________________

(2)方案二:该小组借助反应溶液温度的变化来判断反应的发生。如果NaOH溶液与盐酸混合前后有温度的变化,则证明发生了化学反应。该小组同学将不同浓度的NaOH溶液和盐酸各10 mL混合,用温度计测量反应前后温度的变化,测得的部分数据如下表:

则x=______
(3)若HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1;现有:①稀H2SO4与Ba(OH)2(aq) ②浓H2SO4与Ba(OH)2(aq) ③稀HNO3与Ba(OH)2(aq)反应生成1 mol H2O(l)的反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3三者由小到大的关系为______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化铈(CeO2)是一种重要的稀土氧化物。平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2等物质)。某课题小组以此粉末为原料,设计资源回收的工艺流程如图:
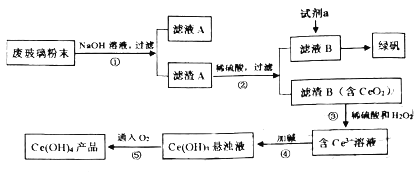
(1)写出第①步反应的离子方程式__。滤液A中的用途是___。
(2)向滤液B中加入过量试剂a可用于制备绿矾(FeSO4·7H2O),试剂a是__(填物质名称)充分反应后,经过滤得到FeSO4溶液。再经蒸发浓缩、冷却结晶、过滤、洗涤等操作步骤得到绿矾。检验所加试剂a已经过量,使用的试剂和判断的依据分别是__、__。
(3)写出第③步反应的化学方程式__。
(4)取上述流程中得到的Ce(OH)4[摩尔质量为208g·mol-1产品0.500g,加硫酸溶解后,用0.1000mol·L-1FeSO4标准溶液滴定(铈被还原为Ce3+)消耗20.00mL标准溶液,该产品中Ce(OH)4的质量分数为__(保留四位有效数字数)。若FeSO4标准溶液部分变质,会使测定结果__。(填“偏高”、“偏低”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚砜(SOCl2)在农药、制药行业中用途广泛,沸点为77℃,遇水剧烈反应,液面上产生白雾,并产生带有刺激性气味的气体。实验室用干燥的Cl2和SO2与SCl2反应合成SOCl2,反应原理是:SO2+Cl2+SCl2=2SOCl2。回答以下问题:
Ⅰ.氯化亚砜的制备
实验室拟用以下装置完成氯化亚砜的制备:
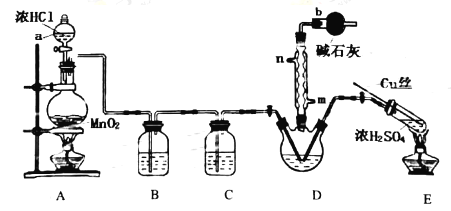
(1)仪器a的名称是__;装置D中冷凝管的冷凝水入口是__。
(2)装置A中反应的离子方程式__;装置E中反应的化学方程式__。
(3)B、C所盛试剂分别是__、__;装置D中干燥管b的作用是__。
(4)本实验的主要副产物是SCl2,已知:SOCl2沸点为77℃,SCl2的沸点为50℃,提纯SOCl2的实验操作是__;
Ⅱ.氯化亚的性质与检测
经分析,某实验小组的同学认为,SOCl2与水反应后的溶液中有盐酸和亚硫酸生成。
(5)欲证明SOCl2与水反应后形成的溶液中有H2SO3生成,可以使用的试剂是__;欲证明纯净SOCl2与水反应后形成的溶液中有Cl-,实验的操作方法是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲萘醌(维生素K)有止血作用,它可通过α-甲基萘的氧化制得,反应中常用乙酸作催化剂,该反应放热,可表示为:
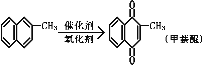
在某次合成反应中,用1.4g(0.01mol)的α-甲基萘,才制得0.17g(0.001mol)甲萘醌,已知该反应的速率是快的。试判断导致其产率低的原因是( )
A.使用了过量的催化剂B.没有用乙酸,而是使用其它催化剂
C.把反应混合物加热D.所生成的甲基醌是沉淀物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g)![]() Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是( )
Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是( )
A.将容器体积变为20L,Z的平衡浓度变为原来的一半
B.若增大压强,则物质Y的转化率减小
C.若升高温度,X的体积分数增大,则该反应的△H>0
D.以X浓度变化表示的反应速率为0.001mol/(L·s)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com