
����Ŀ����ȼ���ֳƷ��������Ҫ�����ӳٻ��ֹ��ȼ���ȼ�ա�������ɣ���ȼ���ɷ�Ϊ±ϵ��ȼ��������ȼ���ȡ�
��1��±ϵ��ȼ����Ϊ�л��Ȼ�����л��廯����Ȼ�ֽ����±���⣨HX��������ȼ���á�±����ĵ���ʽΪ____��HF��HCl��HBr��HI�����Ȼ���ķе��ɸߵ��͵�˳����___��
��2�������ӵ����������Ų�ʽ��___����ԭ�ӵĺ����������___����չ����
��3��������˵���ȵķǽ�����ǿ�������ʵ��___��ѡ���ţ���
a��HClO����ǿ��HBrO
b��HBr�ķֽ��¶ȵ���HCl
c�����廯������Һ�е���������ˮ����Һ��ɫ���
d��BrCl+H2O ��HBrO+HCl�Ƿ�������ԭ��Ӧ
����ȼ���У�����������������þ������ȼ��ռ������Ҫλ�á����ߵ���ȼ���������ڴﵽ�ȷֽ��¶�ʱѸ�ٷֽ�Ϊ��������ˮ�������Ƚ��µ����á�
��4��д������������������Һ�еĵ��뷽��ʽ___��
��5��������ȼ���ķֽ��������Ȼ�������п��ܳ�Ϊԭ�Ӿ������___�����ѧʽ��
��6����ˮ̼��þҲ��һ����������ȼ�������˾��е�λ����������������ص��⣬�����ͷž���������õ����塣д��������Ľṹʽ___��
��7����þ���Ӻ�������Ų���ͬ���������������ӵİ뾶��С��ϵΪ___���������ţ���
���𰸡�![]() HF��HI��HBr��HCl 4s24p6 4 bd Al(OH)3
HF��HI��HBr��HCl 4s24p6 4 bd Al(OH)3![]() Al3++3OH- Al2O3 O=C=O Na+>Al3+
Al3++3OH- Al2O3 O=C=O Na+>Al3+
��������
(1)±��ԭ�ӵ�������������Ϊ7����±�����Ϊ�����ͷ��ӣ���HF���Ӽ���������
(2)��ԭ�Ӻ˵����Ϊ35����ԭ�ӵĺ�������Ų�ʽΪ1s22s22p63s23p5��
(3)Ԫ�صķǽ�����Խǿ���䵥�ʵ�������Խǿ��������������ˮ��������Խǿ�����⻯����ȶ���Խǿ���䵥������������Խ���ס���Լ��ϵ��ʵ�������Խ��
(4)��������������������������ᷴӦ�����κ�ˮ��
(5)����������������þ�ķֽ�����ˮ�⣬����Al2O3��MgO������Mg�Ľ����Ա�Al�Ľ����Ի��ã�
(6)̼��þ���·ֽ�����MgO��CO2������CO2��ֱ���ͷǼ��Է��ӣ�
(7)��þ���Ӻ�������Ų���ͬ����������������ΪNa+��Al3+���˵���������Ӱ뾶С��
(1)±��ԭ�ӵ�������������Ϊ7����±������H��X֮�����һ�����õ��Ӷԣ���HX�ĵ���ʽΪ![]() ��HX��Ϊ�����ͷ��ӣ���Է�������Խ���Ӽ�������Խ�е�Խ�ߣ���HF���Ӽ�����������е������HX�ߣ���HF��HCl��HBr��HI�����Ȼ���ķе��ɸߵ��͵�˳����HF��HI��HBr��HCl��
��HX��Ϊ�����ͷ��ӣ���Է�������Խ���Ӽ�������Խ�е�Խ�ߣ���HF���Ӽ�����������е������HX�ߣ���HF��HCl��HBr��HI�����Ȼ���ķе��ɸߵ��͵�˳����HF��HI��HBr��HCl��
(2)��ԭ�Ӻ˵����Ϊ35���������ӵ����������Ų�ʽΪ4s24p6����ԭ�ӵĺ�������Ų�ʽΪ1s22s22p63s23p5������1s��2s��2p��3s��3p4���ܼ�����s�����1�ֲ�ͬ����չ����p�����3�ֲ�ͬ����չ����������ԭ�ӹ���4�ֲ�ͬ����չ����
(3)a��Ԫ�صķǽ�����Խǿ��������������ˮ��������Խǿ����HClO��HBrO����������������ˮ�����������HClO����ǿ��HBrO�жϷǽ�����Cl��Br����a����
b��HBr�ķֽ��¶ȵ���HCl��˵��HBr�ϲ��ȶ������˵���ȵķǽ�����ǿ���壬��b��ȷ��
c����FeBr2��Һ�еμ�������ˮ����ԭ�ԣ�Fe2+��Br-����������������Fe2+����Fe3+��Fe3+����Һ�г���dz��ɫ������֤���ȵķǽ�����ǿ���壬��c����
d��BrCl+H2O ��HBrO+HCl�Ƿ�������ԭ��Ӧ˵��������Ԫ�ػ��ϼ۵ı仯����BrCl����Ԫ��Ϊ-1�ۣ���֪��ԭ��������������ǿ������Ԫ�صķǽ�����ǿ���壬��d��ȷ��
�ʴ�Ϊbd��
(4)��������������������������ᷴӦ�����κ�ˮ���Լ��ԣ�������������������Һ�еĵ��뷽��ʽΪAl(OH)3![]() Al3++3OH-��
Al3++3OH-��
(5)����������������þ�ķֽ�����ˮ�⣬����Al2O3��MgO����Mg�Ľ����Ա�Al�Ľ�����ǿ��������Ȼ�������п��ܳ�Ϊԭ�Ӿ������Al2O3��
(6)̼��þ���·ֽ�����MgO��CO2������CO2��ֱ���ͷǼ��Է��ӣ���ṹʽΪO=C=O��
(7)��þ���Ӻ�������Ų���ͬ����������������ΪNa+��Al3+���˵���������Ӱ뾶С�����������ӵİ뾶��С��ϵΪNa+>Al3+��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019 ��ŵ������ѧ��������������ӵ����������ͻ��������λ��ѧ�ҡ�һ������ӵ�صĵ���ܷ�ӦΪLix C6 ��Li1-xY![]() C6 (ʯī)+LiY ����֪���ӵ���Ϊ1.6 ��10��19 C �����й��������ص�˵������������
C6 (ʯī)+LiY ����֪���ӵ���Ϊ1.6 ��10��19 C �����й��������ص�˵������������
A.����﮵ļ۵����ܶ�ԼΪ 13760 C/gB.�������Ƕȿ����Ƕ���������
C.�ڷŵ�ʱ�Ԫ�ط����˻�ԭ��ӦD.�ڳ��ʱ����ӽ�Ƕ��ʯī�缫
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijҩ���м���ĺϳ�·�����£�
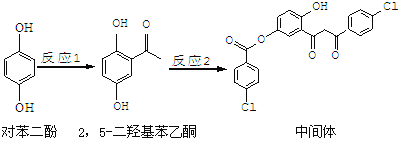
����˵����ȷ����
A.�Ա����Ӻ�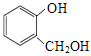 ��Ϊͬϵ��
��Ϊͬϵ��
B.1 mol���м���������7 mol�������Ʒ�Ӧ
C.2��5�����ǻ�����ͪ�ܷ����ӳɡ�ˮ��ȷ�Ӧ
D.���м�����Ӻ����ʻ����ǻ����ֺ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ԭ��Ӧ����( )
A.MgCl2 + Ba(OH)2 == BaCl2 + Mg(OH)2��B.CO2 + 2NaOH == Na2CO3 + H2O
C.CaCO3 ![]() CaO + CO2��D.H2 + CuO ==H2O + Cu
CaO + CO2��D.H2 + CuO ==H2O + Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������BN����һ����Ҫ�Ĺ����մɲ��ϡ�����Ȼ��ɰΪ��ʼ�����һϵ�з�Ӧ���Եõ�BF3��BN����ͼ��ʾ��
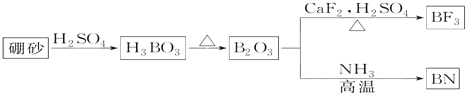
��ش��������⣺
��1����B2O3�Ʊ�BF3��BN�Ļ�ѧ����ʽ��___��___��
��2����̬Bԭ�ӵĵ����Ų�ʽΪ___��B��N��ȣ��ǽ����Խ�ǿ����___��BN��BԪ�صĻ��ϼ�Ϊ___��
��3����BF3�����У�F��B��F�ļ�����___���÷���Ϊ___���ӣ���д�������� �����Ǽ���������BF3����NaF���ÿ�����NaBF4��BF4-�п��ܺ���___������ṹΪ___��
��4������ʯī�ṹ���Ƶ��������������У�����Bԭ����Nԭ��֮��Ļ�ѧ��Ϊ___�����������Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��W��X��Y��Z��Ϊ������Ԫ�أ�X��W���γ�����Һ̬��������ң���ԭ�Ӹ����ȷֱ�Ϊ1��1���ף���2��1���ң����ҷ����е��������ֱ�Ϊ18���ף���10���ң���X��Z���γ�һ�ּ�������ˮ�ļ��������X��Y���γɼ�������ˮ���������嶡���������еĵ�����Ϊ18��X��Y��Z���γ�һ�����ӻ������ˮ��Һ�������ԡ���д����
��1��W��Ԫ�ط���___��������___���˶�״̬��ͬ�ĵ��ӡ�
��2�������ʵĽṹʽΪ___�������ʵĿռ乹��Ϊ___��
��3��ZԪ�غ����___��������ͬ�ĵ��ӣ���������ĵ���ʽΪ___��
��4�������ӷ���ʽ����X��Y��Z�γɵĻ�����ˮ��Һ�������Ե�ԭ����___��
��5����Ԫ�ظ�YԪ�����γɻ����BiY3������ˮ������������ˮ��BiOY��
��BiY3ˮ�ⷴӦ�Ļ�ѧ����ʽΪ___��
�ڰ�������BiY3���ں�����������ˮ�У��ܵõ�������Һ���Է������ܵ�ԭ��___��
��ҽҩ�ϰ�BiOY��������ij���������������ֽз��IJ�����֮����Ϊʲô��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ����(����)
A.����������Һ��ϡ���ᷴӦ:Ba2++S![]() +H++OH-BaSO4��+H2O
+H++OH-BaSO4��+H2O
B.����ӡˢ��·��ķ�Ӧ:Fe3++CuFe2++Cu2+
C.����������������Һ��Ӧ:Cl2+2OH-Cl-+ClO-+H2O
D.ϡ����ε���Ƭ��:2Fe+6H+2Fe3++3H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣��������Ԫ���⣬���е�ÿ����Ŵ���һ��Ԫ�ء������Ҫ��ش����⣺
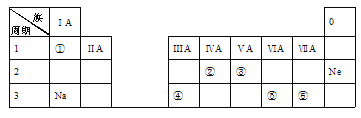
��1���ܵ�ԭ��������________��
��2���ݵ�ԭ�ӽṹʾ��ͼ��____________��
��3���ں͢�����Ԫ�صķǽ�����ǿ����ϵ�ǣ���______�ۣ�����>������<������=������
��4���ٺ͢�����Ԫ����ɵĻ������к��еĻ�ѧ����_____����������������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣��������Ԫ���⣬���е�ÿ����Ŵ���һ��Ԫ�ء������Ҫ��ش����⣺
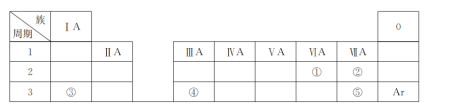
(1)�ٵ�Ԫ�ط�����________��
(2)�ں͢ݵ�ԭ�Ӱ뾶��С��ϵ�Ǣ�________��(����������������������)��
(3)�ۺ͢��γɵĻ����ﺬ�еĻ�ѧ����__________(�������Ӽ����������ۼ���)��
(4)�ۡ��ܵ�����������Ӧ��ˮ�������Ӧ�����ӷ���ʽΪ_________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com