
【题目】某药物中间体的合成路线如下:
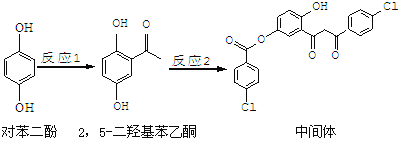
下列说法正确的是
A.对苯二酚和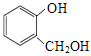 互为同系物
互为同系物
B.1 mol该中间体最多可与7 mol氢氧化钠反应
C.2,5—二羟基苯乙酮能发生加成、水解等反应
D.该中间体分子含有羰基和羟基两种含氧官能团
科目:高中化学 来源: 题型:
【题目】某新型水系钠离子电池工作原理如下图所示。TiO2光电极能使电池在太阳光照下充电,充电时Na2S4还原为Na2S。下列说法错误的是
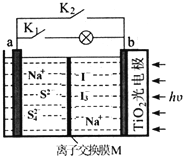
A. 充电时,太阳能转化为电能,又转化为化学能
B. 放电时,a极的电极反应式为:4S2--6e-=S42-
C. 充电时,阳极的电极反应式为:3I--2e-=I3-
D. M是阴离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“嫦娥飞天,玉兔登月”实现了中华民族“九天揽月” 的伟大梦想,“玉兔”号月球车上太阳能电池板使用的半导体材料是( )

A.硫B.硅C.镁D.铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个1L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:

(1)从开始至2min,X的平均反应速率为__________;
(2)该反应的化学方程式为_______________________;
(3)1min时,正逆反应速率的大小关系为:v(正)_____v(逆),2min时,v(正)_____v(逆)。(填“>”或“<”或“=”)
(4)若X、Y、Z均为气体,在2min时,向容器中通入氩气,增大体系压强,X的化学反应速率将______,若加入适合的催化剂,Y的化学反应速率将______。(填“变大”或“不变”或“变小”)
(5)若X、Y、Z均为气体,下列能说明反应已达平衡的是_____________。
a.X、Y、Z三种气体的浓度相等
b.气体混合物物质的量不再改变
c.反应已经停止
d.反应速率v(X)︰v(Y)=2:1
e.(单位时间内消耗X的物质的量):(单位时间内消耗Z的物质的量)=3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中,用下图所示装置(尾气处理装置略去)进行下列实验,将①中液体逐滴滴入到②中。实验结果与预测的现象一致的是
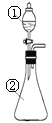
选项 | ①中的物质 | ②中的物质 | 预测②中的现象 |
A. | 氢氧化钠 | 明矾溶液 | 开始时即产生白色沉淀 |
B. | 浓硫酸 | 铜片 | 产生无色气体,溶液变蓝 |
C. | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
D. | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 开始时无明显现象 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳和硅均为元素周期表中第IV A族的元素,其单质和化合物有着重要应用。
(1)石墨烯是只有一个碳原子直径厚度的单层石墨,最早是由科学家用机械剥离的方法从石墨中分离出来,其部分性能优于传统的硅材料,具有广泛的应用前景。
①写出基态碳原子的电子排布式________。石墨烯中C的杂化类型为________。
②下图为单层石墨烯的结构示意图。12 g的石墨烯中由C原子连接成的六元环的物质的量约为________mol。

③石墨烯加氢制得的石墨烷,可用![]() 表示。下列有关叙述正确的是________。
表示。下列有关叙述正确的是________。
a.石墨烷属于烷烃 b.石墨烷难溶于水
c.石墨烷中所有碳原子共平面 d.石墨烷可以发生加成反应
④石墨烯可由加热![]() 晶体脱除
晶体脱除![]() 的方法制得。该过程属于________。
的方法制得。该过程属于________。
a.物理变化 b.分解反应 c.氧化还原反应
(2)![]() 的晶体结构与晶体硅类似。
的晶体结构与晶体硅类似。![]() 的晶体类型为________,晶体中
的晶体类型为________,晶体中![]() 原子与
原子与![]() 键的数目之比为________。
键的数目之比为________。
(3)![]() 与
与![]() 空间构型相似,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式:__________________________。
空间构型相似,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铵明矾(NH4Al(SO4)212H2O)是常见的食品添加剂,用于焙烤食品,可通过硫酸铝溶液和硫酸铵溶液反应制备。用芒硝(Na2SO410H2O)制备纯碱和铵明矾的生产工艺流程图如图1:
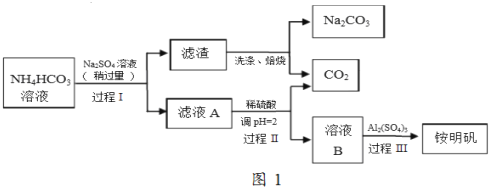
完成下列填空:
(1)铵明矾溶液呈_________性,它可用于净水,原因是_______________;向其溶液中逐滴加入NaOH溶液至过量,可观察到的现象是__________________。
(2)写出过程Ⅰ的化学反应方程式_______________。
(3)若省略过程Ⅱ,直接将硫酸铝溶液加入滤液A中,铵明矾的产率会明显降低,原因是___________。
(4)已知铵明矾的溶解度随温度升高明显增大.加入硫酸铝后,经过程III的系列实验得到铵明矾,该系列的操作是加热浓缩、___________、过滤洗涤、干燥。
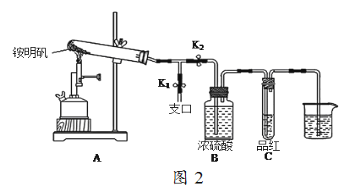
(5)某同学用图2图示的装置探究铵明矾高温分解后气体的组成成份。
①夹住止水夹K1,打开止水夹K2,用酒精喷灯充分灼烧。实验过程中,装置A和导管中未见红棕色气体;试管C中的品红溶液褪色;在支口处可检验到NH3,方法是______________;在装置A与B之间的T型导管中出现白色固体,该白色固体可能是___________(任填一种物质的化学式);另分析得出装置A试管中残留的白色固体是两性氧化物,写出它溶于NaOH溶液的离子方程式_______________。
②该同学通过实验证明铵明矾高温分解后气体的组成成份是NH3、N2、SO3、SO2和H2O,且相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阻燃剂又称防火剂,主要用于延迟或防止可燃物的燃烧。根据组成,阻燃剂可分为卤系阻燃剂、无机阻燃剂等。
(1)卤系阻燃剂多为有机氯化物和有机溴化物,受热会分解产生卤化氢(HX),起到阻燃作用。卤化氢的电子式为____;HF、HCl、HBr、HI四种氯化氢的沸点由高到低的顺序是___。
(2)溴离子的最外层电子排布式是___;氯原子的核外电子云有___种伸展方向。
(3)下列能说明氯的非金属性强于溴的事实是___(选填编号)。
a.HClO酸性强于HBrO
b.HBr的分解温度低于HCl
c.向溴化亚铁溶液中滴入少量氯水,溶液颜色变黄
d.BrCl+H2O →HBrO+HCl是非氧化还原反应
无机阻燃剂中,氢氧化铝和氢氧化镁两种阻燃剂占据着重要位置。两者的阻燃机理都是在达到热分解温度时迅速分解为氧化物与水,起到吸热降温的作用。
(4)写出氢氧化铝在酸性溶液中的电离方程式___。
(5)两种阻燃剂的分解产物在自然界中最有可能成为原子晶体的是___。(填化学式)
(6)无水碳酸镁也是一种新型无机阻燃剂,除了具有单位质量吸热量更大的特点外,还能释放具有灭火作用的气体。写出该气体的结构式___。
(7)与镁离子核外电子排布相同的另外两个阳离子的半径大小关系为___(填微粒符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学学习小组利用如图装置来制取乙酸乙酯。
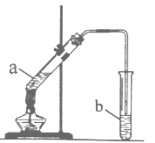
I.实验过程:向试管a中加入碎瓷片,3mL乙醇,然后边振荡试管边慢慢加入2mL浓硫酸,最后加入2mL乙酸,按图连接好装置,用酒精灯缓慢加热,将产生的蒸汽经导管通到b试管中的液面上。
II. 已知化学方程式:CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
III.查阅资料得知:乙酸乙酯不溶于水,密度比水小,且有香味
请回答下列问题:
(1)试管a中加入碎瓷片,其作用是_____(填字母代号)。
A.加快化学反应速率 B.防止溶液暴沸
(2)试管b中的溶液是_____(填字母代号)。
A饱和碳酸钠溶液 B.饱和氢氧化钠溶液
(3)实验完毕后,将b试管中的液体充分振荡,静置后,溶液分为两层。
①乙酸乙酯在________(填“上层”或“下层”)。
②常用________操作将两层液体分离(填“过滤”或“分液”)。
(4)实验中加入乙酸的质量为2.1g,其中60%的乙酸发生酯化反应,则得到乙酸乙酯的质量为______g(计算结果保留两位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com