
【题目】下列说法不正确的是( )
A. HClO、H2CO3、H2SO4、HClO4的酸性依次增强
B. 苹果酸![]() 含有1个手性碳原子
含有1个手性碳原子
C. HF、NH3、CH3OH均易溶于水的原因之一是与H2O分子均形成氢键
D. 以极性键结合的分子一定不是非极性分子
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W原子最外层电子数是其内层电子数的3倍。下列说法错误的是
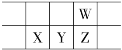
A.原子半径:W<X
B.Y 的最高价氧化物的水化物是强酸
C.气态氢化物热稳定性:Z<W
D.X 的位置为第三周期IVA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有5种短周期元素的原子序数按E、D、B、A、C的顺序依次增大;A、C同周期,B、C同主族;A与B可形成离子化合物A2B,A2B中所有粒子的电子数相同,且电子总数为30;D和E可形成4核10电子的分子。试回答下列问题:
(1)用电子式表示离子化合物A2B的形成过程:______________________。
(2)写出下列物质的电子式: D元素形成的单质__________;E2B________________;A、B、E形成的化合物__________;D、E形成的化合物__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某“绿色试剂”双氧水可作为矿业废液消毒剂,如要消除采矿业废液中的氰化物如KCN,化学方程式为:KCN+H2O2+KOH→K2CO3+NH3↑。
(1)在化学方程式上标出电子转移方向和数目___;
(2)反应中被氧化的元素为___,KOH的电子式为___;
(3)NH3分子中N—H键为__(填极性或非极性)共价键;
(4)H2O2属于___(填共价或离子)化合物;
(5)写出溶液中发生该反应时,生成的化学键类型___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质浓度为c mol/L,则下列关系中不正确的是
A. ![]()
B. ![]()
C. ![]()
D. ![]() =1000Vρ/(17V+22400)
=1000Vρ/(17V+22400)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. Xe元素的所在族的原子的外围电子排布式均为ns2np6,属于非金属元素
B. 在元素周期表中,s区,d区和ds区的元素都是金属(氢元素除外)
C. 某基态原子核外电子排布图为![]() 它违背了泡利原理
它违背了泡利原理
D. 某外围电子排布为4f75d16s2基态原子,该元素位于周期表中第六周期第ⅢB族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两位同学分别设计了如图甲、乙所示的实验。下列叙述中不正确的是( )

A.图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小
B.若图甲所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C.用图乙装置测定反应速率,可测定反应产生的气体体积及反应时间
D.为检查图乙所示装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,下列叙述正确的是
A.1mol ICl与H2O完全反应生成氯化氢和次碘酸,转移的电子数为NA
B.常温常压下,56 g丁烯 (C4H8)中含有的共价单键总数为8 NA
C.电解精炼铜时,阳极质量减少64g,闭合回路转移的电子数一定为2NA
D.质量均为3.2g的S2、S4、S6中所含S原子数相等,都为0.1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某温度时,在一个10L的恒容容器中X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
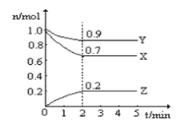
⑴该反应的化学方程式为___________;
⑵反应开始至2min,以气体Z表示的平均反应速率为___________;
⑶平衡时容器内混合气体密度比起始时_________(填“变大”,“变小”或“不变”下同),混合气体的平均相对分子质量比起始时___________;
⑷将amolX与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=__________。
Ⅱ.已知硫代硫酸钠溶液与稀硫酸反应的化学方程式为Na2S2O3+H2SO4= Na2SO4+ SO2↑+S↓+H2O,某学习小组探究一定条件下影响化学反应速率的因素,如下表所示:
⑸对比实验I、III可以得出的结论是______________,实验I、II探究的是___________的浓度越大,该反应速率越快,若实验III、IV也想得出同样结论,X=___________,Y= _________。
实验序号 | 温度 | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
V/mL | c/(molL-1) | V/mL | c/(molL-1) | V/mL | ||
I | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
II | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
III | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
IV | 35 | 5 | 0.2 | X | 0.2 | Y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com