
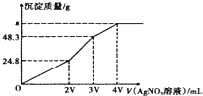
【题目】某混合溶液中含有溶质为NaCl、KI和Na2S各0.1mol,往该溶液在加入一定浓度的AgNO3溶液,产生沉淀的质量随加入AgNO3溶液的体积变化如图所示,则下列说法中不正确的是( )
A.所加AgNO3溶液的物质的量浓度为![]() mol/L
mol/L
B.a的数值为62.65
C.常温下,AgCl,AgI,Ag2S在水中溶解能力依次减小
D.在AgCl饱和溶液中加入NaI固体,有AgI沉淀生成
【答案】A
【解析】
向溶液中加入AgNO3溶液发生的离子反应有Ag++Cl-=AgCl↓、Ag++I-=AgI↓、2Ag++S2-=Ag2S↓,三种阴离子的物质的量相等,根据图中纵坐标数值结合离子方程式知,NaCl、KI消耗硝酸银体积相等且是Na2S消耗硝酸银溶液体积的一半,所以0~2V发生反应2Ag++S2-=Ag2S↓、2V~3V发生反应Ag++I-=AgI↓、3V~4V发生反应Ag++Cl-=AgCl↓。
A.根据图知,0~2V时,发生反应2Ag++S2-=Ag2S↓,n(Ag2S)=![]() =0.1mol,根据Ag原子守恒得n(AgNO3)=2n(Ag2S)=0.2mol,硝酸银物质的量浓度=
=0.1mol,根据Ag原子守恒得n(AgNO3)=2n(Ag2S)=0.2mol,硝酸银物质的量浓度=![]() =
=![]() mol/L,A说法不正确;
mol/L,A说法不正确;
B.a为AgCl、AgI和Ag2S混合物,3V~4V时生成沉淀AgCl,根据Cl原子守恒得n(AgCl) =n(NaCl)=0.1mol,m(AgCl)=0.1mol×143.5g/mol=14.35g,则a=14.35g+48.3g=62.65g,B说法正确;
C.相同温度下,溶解度小的先生成沉淀,根据以上分析知,生成沉淀依次顺序是Ag2S、AgI、AgCl,所以常温下,AgCl、AgI、Ag2S在水中溶解能力依次减小,C说法正确;
D.溶度积常数大的物质容易转化为溶度积常数小的物质,溶解度常数AgI<AgCl,所以在AgCl饱和溶液中加入NaI固体,有AgI沉淀生成,D说法正确;
题目说法不正确的,故选A。


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
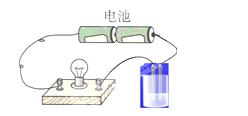
【题目】用如图所示的装置分别进行如下实验,各离子方程式正确及各组物质反应后,溶液的导电性比反应前增强的是( )
A.向硝酸银溶液中通入少量氯化氢:Ag++Cl-=AgCl↓
B.向亚硫酸溶液中通入氯气:H2SO3+C12+H2O=SO42-+4H++2Cl-
C.向FeBr2溶液中通入少量氯气:2Fe2++Cl2=2Fe3++2Cl-
D.向NaOH溶液中通入少量氯气:2OH-+Cl2=Cl-+ClO-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,向10L容积不变的密闭容器中加入1.0molNH2COONH4,发生反应NH2COONH4(s)![]() CO2(g)+2NH3(g) ΔH>0。5min达到平衡时,测得容器中NH2COONH4(s)的物质的量为0.2mol。下列说法正确的是
CO2(g)+2NH3(g) ΔH>0。5min达到平衡时,测得容器中NH2COONH4(s)的物质的量为0.2mol。下列说法正确的是
A. 0~5min内,v(CO2)=0.16mol·L-1·min-1
B. 氨气体积分数不变时,该反应一定达到平衡状态
C. 平衡后,缩小容器容积,重新建立平衡时,c(CO2)增大
D. 其他条件不变,若将原容器改为绝热容器,则达到平衡时,NH2COONH4的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
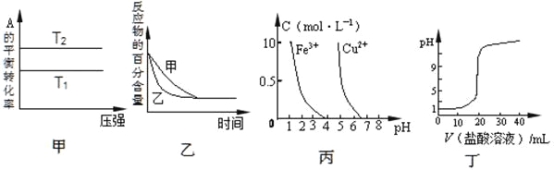
A.由图甲可以判断:若T1>T2,反应A(g)+ B(g)![]() 2C(g)的△H<0
2C(g)的△H<0
B.图乙表示压强对可逆反应2A(g)+2 B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
C.根据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量NaOH溶液,调节pH≈4
D.图丁表示用0.1mol/L的盐酸滴定20mL 0.1mol/LNaOH溶液,溶液pH随加入盐酸体积的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
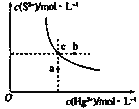
【题目】硫化汞(HgS)难溶于水,在自然界中呈红褐色,常用于油画颜料,印泥及朱红雕刻漆器等。某温度时,HgS在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
A.向硫化汞的浊液中加入硫化钠溶液,硫化汞的Ksp减小
B.图中a点对应的是饱和溶液
C.向c点的溶液中加入Hg(NO3)2,则c(S2-)减小
D.升高温度可以实现c点到b点的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在湿法炼锌的电解循环溶液中,含较高浓度的![]() ,可向溶液中同时加入Cu和
,可向溶液中同时加入Cu和 ![]() ,生成CuCl沉淀从而除去
,生成CuCl沉淀从而除去![]() ,反应原理如下:
,反应原理如下:![]() ;
;![]() ;室温时,实验测得电解液pH对溶液中残留
;室温时,实验测得电解液pH对溶液中残留![]() 的影响和平衡时溶液中相关离子浓度的关系如图所示下列说法正确的是( )
的影响和平衡时溶液中相关离子浓度的关系如图所示下列说法正确的是( )
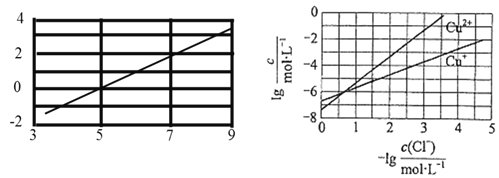
A.已知室温时AgCl的溶度积常数约为![]() ,则:
,则:![]()
B.向电解液中加入稀硫酸,有利于![]() 的除去
的除去
C.![]() 的平衡常数的数量级是
的平衡常数的数量级是![]()
D.除去上述电解循环溶液的产生![]() 的
的![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在密闭容器中发生如下反应:N2O4(g)![]() 2NO2(g) △H>0,反应达到平衡时,下列说法不正确的是 ( )
2NO2(g) △H>0,反应达到平衡时,下列说法不正确的是 ( )
A.若缩小容器的体积,则容器中气体的颜色先变深后又变浅,且比原平衡颜色深
B.若压强不变,向容器中再加入一定量的N2O4,再次达到平衡时各种物质的百分含量不变
C.若体积不变,向容器中再加入一定量的N2O4,平衡向逆反应方向移动,再次平衡时N2O4的体积分数将增大
D.若体积不变,升高温度,再次平衡时体系颜色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,
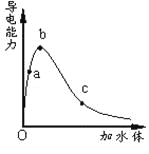
下列说法正确的是
A.a、b、c三点溶液的pH:c<a<b
B.a、b、c三点醋酸的电离程度:a<b<c
C.用湿润的pH试纸测量a处溶液的pH,测量结果偏大
D.a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:c<a<b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述正确的是
A. 苯和氯气生成C6H6Cl6的反应是取代反应
B. 乙烯与溴水发生加成反应的产物是CH2CH2Br2
C. 等物质的量的甲烷与氯气反应的产物是CH3Cl
D. 硫酸作催化剂,CH3CO18OCH2CH3水解所得乙醇分子中有18O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com