
【题目】完全燃烧2mol某有机物,可以收集到标准状况下89.6L的CO2和6mol的H2O,同时消耗6molO2 , 试推断该有机物的分子式是( )
A.C2H4
B.C2H4O
C.C2H6
D.C2H6O
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
【题目】利用如图所示装置,甲中盛有100mL 0.1mol/LCuSO4溶液,乙中盛有100mL 0.2mol/L Na2SO4溶液。
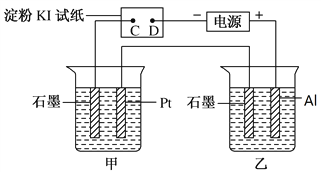
(1)通电一段时间,观察到湿润的淀粉KI试纸的_____(选填“C”或“D”)端变蓝。
(2)装置乙中观察到的现象是_________________________________________。
(3)若电解一段时间后,装置甲、乙中共收集到气体0.168 L(标准状况下),则:
①装置甲中发生反应的离子反应方程式为______________________________。
②若电解前后体积变化忽略不计,则电后装置甲中溶液的c(H+)为________。
(4)若电解一段时间后,装置甲中溶液需加入0.005mol碱式碳酸铜才能恢复原来的浓度和pH,则电解过程中转移的电子数目为__________。
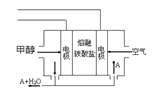
(5)若装置中的电源使用如右图的一种新型燃料电池,以甲醇为燃料,一定比例的Li2CO3和Na2CO3的熔融混合物为电解质,则负极反应式为__________________。
(6)电解一段时间后,拆解装置,将图中甲装置取出后,用导线将石墨和Pt连接构成闭合回路。则此装置中Pt上发生的电极反应式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯水加热至较高温度,下列叙述正确的是( )
A.水的离子积变大,pH变小,呈中性
B.水的离子积变大,pH变大,呈碱性
C.水的离子积变小,pH变大,呈碱性
D.水的离子积变小,pH变大,呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置,完成很多电化学实验.下列有关此装置的叙述中,正确的是( ) 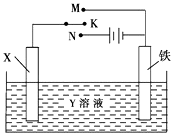
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可加快铁的腐蚀
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,可用于铁表面镀铜,溶液中铜离子浓度将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇既是重要的化工原料,又可作为燃料,还可以作为燃料电池的原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) ![]() CH3OH(g) ΔH1 (已知:CO的结构与N2相似)
CH3OH(g) ΔH1 (已知:CO的结构与N2相似)
②CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)ΔH2
CH3OH(g)+H2O(g)ΔH2
③CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3
回答下列问题:
(1)已知反应①中相关的化学键键能数据如下:
化学键 | H-H | C-O | C=O | H-O | C-H |
E/(KJ/mol) | 436 | 343 | 1076 | 465 | 413 |
由此计算ΔH1=______kJ·mol-1,已知ΔH2=-58kJ·mol-1,则ΔH3=_____kJ·mol-1。
(2)已知:
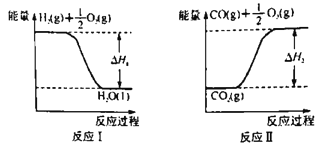
若甲醇的燃烧热为ΔH3,试用ΔH1、ΔH2、ΔH3表示CO(g)+2H2(g) ![]() CH3OH(l)的ΔH=________。若ΔH1=-285.8 kJ·mol-1,ΔH2=+283.0 kJ·mol-1,某H2和CO的混合气体完全燃烧时放出113.74 kJ热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为______。
CH3OH(l)的ΔH=________。若ΔH1=-285.8 kJ·mol-1,ΔH2=+283.0 kJ·mol-1,某H2和CO的混合气体完全燃烧时放出113.74 kJ热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为______。
(3)以CH4和H2O为原料,通过下列反应也可以制备甲醇。
Ⅰ:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206.0 kJ·mol-1
Ⅱ:CO(g)+2H2(g)= =CH3OH (g)ΔH=-129.0 kJ·mol-1
CH4(g)+H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为__________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A,B混合于2L的密闭容器中,发生下列反应:3A(g)+B(g)xC(g)+2D(g),经2min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.25molL﹣1min﹣1 , 下列说法正确的是( )
A.反应速率v(B)=0.25 molL﹣1min﹣1
B.该反应方程式中,x=1
C.2min时,A的物质的量为1.5mol
D.2min时,A的转化率为60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:反应aA(?)+ B(?)=aC(g),下列条件的改变一定能使化学反应速率加快的是( )
A.增加A的物质的量B.升高体系温度
C.减少C的物质的量浓度D.增加体系的压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A、B、C、D、E、F有以下转化关系.A的产量是衡量一个国家石油化工生产水平的标志;D能使石蕊试液变红;E是不溶于水且具有水果香味的无色液体,相对分子质量是C的2倍;F是塑料的主要成分之一,常用于制食品包装袋.结合如图关系回答问题:
(1)按要求回答下列问题:
①写出A、E的结构简式:A、E;
②写出B、C、D、E中官能团的名称:B、C、 DE、;
③写出反应②的反应方程式:
(2)A与苯都是石油化工的重要产品,在一定条件下A可以转化生成苯,按要求回答下列问题:
①苯可以发生取代反应,写出由苯制备溴苯的化学反应方程式:
②纯净的溴苯是无色油状液体,实验室制得的粗溴苯通常因溶解了Br2呈褐色,可以加入试剂除去,反应方程式为 , 该除杂操作所必须的主要玻璃仪器是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种乙醇燃料电池原理如图所示,有关说法正确的是( ) 
A.燃料电池能量转化率比乙醇燃烧发电低
B.电池工作时,电极a上产生淡蓝色火焰
C.电子由电极a经“聚合电解质”流向电极b
D.电池反应为:C2H5OH+3O2→2CO2+3H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com