
����Ŀ����������һ�������(������ˮ���Ҵ����۵�234.5 �棬100 �����Ͽ�ʼ����)�����˷ܴ�������������á���Ҷ�к�������Լ1%��5%��������(KaԼΪ10��6��������ˮ���Ҵ�)Լ3%��10%��������ɫ�ء���ά�صȡ�ʵ���ҴӲ�Ҷ����ȡ�������������ͼ��ʾ��

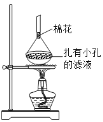
������ȡװ����ͼ��ʾ��ʵ��ʱ��ƿ���ܼ�������������������������2���������������ܣ������������ֽ��Ͳ1�У����Ҷĩ�Ӵ���������ȡ����ȡҺҺ��ﵽ������3����ʱ����������3������ƿ���Ӷ�ʵ�ֶԲ�Ҷĩ��������ȡ���ش��������⣺

(1)ʵ��ʱ�轫��Ҷ��ϸ��������ֽ��Ͳ1�У���ϸ��Ŀ����______________��Բ����ƿ�м���95%�Ҵ�Ϊ�ܼ�������ǰ��Ҫ�Ӽ���______________��
(2)��ȡ���̲���ѡ������ֱ�Ӽ��ȣ�ԭ����__________���볣�����ȡ��ȣ�����������ȡ�����ŵ���_____��
(3)��ȡҺ�辭������Ũ������ȥ���ܼ�����ˮ��ȣ��Ҵ���Ϊ��ȡ�����ŵ���______________��������Ũ������ѡ�õ���������Բ����ƿ������ͷ���¶ȼơ����չ�֮�⣬����______________(����)��
A.ֱ�������� B.����������C.����ƿD.�ձ�
(4)Ũ��Һ����ʯ�ҵ��������к�______________������________��
(5)�ɲ�����ͼ��ʾ�ļ���װ�÷����ᴿ��������״������������в�С����ȣ�������������С����ֽ�����ᣬ�÷����ᴿ������������______________��
���𰸡����ӹ�Һ�Ӵ��������ȡ��� ��ʯ �Ҵ��ӷ�����ȼ ʹ���ܼ��٣���������ȡ �Ҵ��е�ͣ���Ũ�� AC ������ ˮ ����
��������
����Ҷ��ϸ����ֵ����Ҵ��Ӵ����Ҵ���ȡ������͵����ᣬ����������ȡ��������ʹ���Ҵ���ȡ����ȡҺ��������װ�ý�������Ũ����������ʯ���뵥���ᷴӦ������ˮ���õ���״������������ķ����õ�������
(1)ʵ��ʱ�轫��Ҷ��ϸ������Ӵ��������Һ�Ӵ���������ϸ��Ŀ�������ӹ�Һ�Ӵ��������ȡ��֣�Բ����ƿ�м���95%�Ҵ�Ϊ�ܼ���Һ�����ǰ��Ҫ�Ӽ�����ʯ���ʴ�Ϊ�����ӹ�Һ�Ӵ��������ȡ��֣���ʯ��
(2)���������ʹ�Ҵ��ӷ������Ҵ���ȼ�գ���˲������������ԭ�����Ҵ��ӷ�����ȼ���볣�����ȡ��ȣ�����������ȡ�����ŵ���ʹ���ܼ��٣���������ȡ���ʴ�Ϊ���Ҵ��ӷ�����ȼ��ʹ���ܼ��٣���������ȡ��
(3)�Ҵ��ķе�ͣ����������٣�����Ҵ���Ϊ��ȡ�����ŵ����Ҵ��е�ͣ���Ũ����������Ũ������ѡ�õ���������Բ����ƿ������ͷ���¶ȼơ����չ�֮�⣬����ֱ�������������Ҵ������ý���װ���ռ�����˻���AC���ʴ�Ϊ��AC��
(4)Ũ��Һ�к��е����ᡢ�����������ˮ������ʯ�ҵ��������к͵����������ˮ���ʴ�Ϊ�������ˮ��
(5)���ݿ�����100 �����Ͽ�ʼ������������������С����ֽ�����ᣬ�÷����ᴿ�������������������ʴ�Ϊ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ʊ�(NH4)2Fe(SO4)26H2O��ʵ���У���Թ��˳���Ʒ��ĸҺpH<1���д����������£��ֱ�ȡĸҺ�������м���ָ�����ʣ���Ӧ�����Һ����Ҫ���ڵ�һ��������ȷ���ǣ� ��
A.ͨ�����Cl2��Fe2+��H+��NH4+��Cl-��SO42-
B.�������NaClO��Һ��NH4+��Fe2+��H+��SO42-��ClO-
C.�������NaOH��Һ��Na+��Fe2+��NH4+��SO42-��OH-
D.�������NaClO��NaOH�Ļ����Һ��Na+��SO42-��Cl-��ClO-��OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��HCN(aq)�� NaOH(aq) ==NaCN(aq)��H2O(l) ��H����12.1 kJ��mol��1��
HCl(aq)��NaOH(aq) ==NaCl (aq)��H2O(l) ��H����55.6 kJ��mol��1
��HCN��ˮ��Һ�е���Ħ�H����
A����43.5 kJ��mol��1 B ����67.7 kJ��mol��1
C����43.5 kJ��mol��1 D����67.7 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʾ��ͼ���Ӧ�ķ�Ӧ�����ȷ����
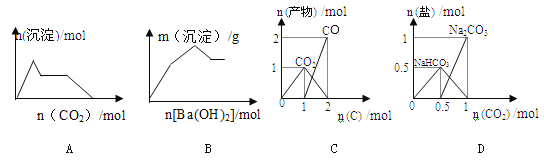
A.��0.01molKOH ��0.01mol Ca��OH��2�Ļ����Һ�л���ͨ��CO2
B.KAl��SO4��2��Һ����μ���Ba��OH��2��Һ
C.n��O2��=1molʱ��������C��O2���ܱ������еķ�Ӧ����
D.n��NaOH��=1molʱ��CO2��NaOH��Һ��Ӧ���ɵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(����)
A.���ݷ�ӦCu��H2SO4![]() CuSO4��H2�����Ƴ�Cu�Ļ�ԭ�Ա�H2��ǿ
CuSO4��H2�����Ƴ�Cu�Ļ�ԭ�Ա�H2��ǿ
B.���û���ӦI2��2NaClO3=2NaIO3��Cl2��֪I2��������ǿ��Cl2��������
C.��⺬Pb(NO3)2��Cu(NO3)2����Һ�������������ӵõ��Ӵ���������Cu2����H����Pb2+
D.��amolNa2S����Һ���������2.5amol�Ķ�����������(������SO2��ˮ�е��ܽ�)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӵ����ڶ��㻨�Ļ����У��Զ����Ϊԭ����ȡ�л��� F ��·�����£�
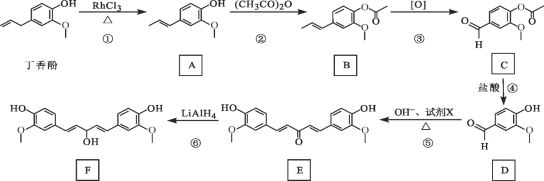
��֪��![]()
��1������ӵķ���ʽΪ_______��
�� 2�� A �еĺ�����������_______�� �����ƣ��� �� �ķ�Ӧ����Ϊ_______��
��3��д���������������� C ������ͬ���칹��Ľṹ��ʽ_______��
�ٺ������һ���ֻ������ȡ������
������������
�ۺ˴Ź��������� 3 ��壬�ҷ����֮��Ϊ 3��1��1��
��4��1 mol D ��������_______molH2 �����ӳɷ�Ӧ��
��5����Ӧ���У��Լ� X �Ľṹ��ʽΪ_______��
��6�������ૼ�ȩ�� ![]() ���ͻ�����Ϊԭ����
���ͻ�����Ϊԭ���� ![]() �ĺϳ�·��_______�����Լ���ѡ����
�ĺϳ�·��_______�����Լ���ѡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ������Ӧ�����ӷ���ʽ��ȷ����
A. �����£��ⶨ��������Һ��pH > 7��CH3COONa === CH3COO-��Na+
B. ʵ�������Ȼ�����Һ�Ͱ�ˮ�Ʊ�����������Al3+ +3OH- === Al(OH)3��
C. ��ϡ�����ȥ��������Һ����������������ƣ�Na2S2O3 + 2H+ === SO2 �� + S��+ 2Na+ + H2O
D. ��̼������Һ������¯ˮ���е�����ƣ�CaSO4(s) + CO32-(aq) === CaCO3(s) + SO42-(aq)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��·��������ҵ��ˮ����������������ŷŵ���ˮ�����±���ʾ��Ϊ�о���ˮ��Cu2+���������pH��ȡ5�ݵ����ķ�ˮ���ֱ���30%��NaOH��Һ����pH��8.5��9��9.5��10��11�����ú����ϲ���Һ��ͭԪ�صĺ�����ʵ��������ͼ��ʾ��

�������ϣ�ƽ��I��Cu(OH)2 + 4NH3 ![]() [Cu(NH3)4]2+ + 2OH-��
[Cu(NH3)4]2+ + 2OH-��
ƽ��II��Cu(OH)2 + 2OH- ![]() [Cu(OH-)4]2-
[Cu(OH-)4]2-
��Ŀ | ��ˮˮ�� | �ŷű� |
pH | 1.0 | 6~9 |
Cu2+/ mg��L-1 | 72 | ��0.5 |
NH4+/ mg��L-1 | 2632 | ��15 |
����˵������ȷ����
A. ��ˮ��Cu2+���������pHԼΪ9
B. b~c�Σ���pH���ߣ�Cu(OH)2�������ӣ�ƽ��I�����ƶ���ͭԪ�غ�������
C. c~d�Σ���pH���ߣ�c(OH-)���ӣ�ƽ��I�����ƶ���ͭԪ�غ����½�
D. d���Ժ���c(OH-)���ӣ�ͭԪ�غ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������þͭ�Ͻ���뵽ϡ�����У�����ǡ����ȫ��Ӧ�����跴Ӧ�����л�ԭ����ȫ��NO����������Һ�м������ʵ���Ũ��Ϊ3 mol��L��1 NaOH��Һ��������ȫ��������ɳ�����������ԭ�Ͻ����������5.1 g���������й���������ȷ���ǣ� ��
A. ����Ͻ������������Ϊ6.4 g
B. �μӷ�Ӧ����������ʵ���Ϊ0.1 mol
C. ������ȫʱ����NaOH��Һ�����Ϊ150 mL
D. �ܽ�Ͻ�ʱ�ռ���NO���������ڱ�״����Ϊ2.24 L
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com