
【题目】W、X、Y、Z、N是短周期元素,它们的核电荷数依次增大。
元素 | 元素性质或原子结构 |
W | 单质在氯气中燃烧,产生苍白色火焰 |
X | 在Y的上一周期,原子核外s能级上的电子总数与p能级上的电子总数相等 |
Y | 元素的离子半径在该周期中最小 |
Z | 原子核外p能级上的电子总数比s能级上的电子总数多2 |
N | 最外层电子数比次外层电子数少1 |
(1)W单质的化学式为_______,Z元素原子核外有_________个原子轨道填充了电子。
(2)Y、Z和N三种元素第一电离能由大到小的顺序为____________(填元素符号),写出Y3+在过量氨水中反应的离子方程式 ____________。
(3)用电子式表示X与W构成的化合物的形成过程________。
(4)Z元素原子共有________种不同运动状态的电子。
【答案】H2 8 Cl>Si>Al Al3++3NH3. H2O=Al(OH)3 ↓+3NH4+ ![]() 14
14
【解析】
W元素的单质在氯气中燃烧,产生苍白色火焰可知W是H元素,X在Y的上一周期,原子核外s能级上的电子总数与p能级上的电子总数相等,则X核外电子排布是1s22s22p4,X是O元素;Y元素的离子半径在该周期中最小,则Y是Al元素;Z原子原子核外p能级上的电子总数比s能级上的电子总数多2,则Z核外电子排布式是1s22s22p63s23p2,Z是Si元素,N最外层电子数比次外层电子数少1,则N核外电子排布是2、8、7,N是Cl元素,然后根据物质的元素组成及物质结构分析解答。
根据上述分析可知:W是H,X是O,Y是Al,Z是Si,N是Cl元素。
(1)W单质的化学式为H2,Z是Si,是14号元素,核外电子排布式是1s22s22p63s23p2,s轨道数是1,p轨道数目是3,在Si原子最外层的2p轨道上有2个轨道上有电子,而且成单排列,自旋方向相同,所以Si元素原子核外有1+1+3+1+2=8个原子轨道填充了电子。
(2)Y、Z和N三种元素分别是Al、Si、Cl,元素的非金属性越强,原子半径越小,第一电离能就越大,元素的非金属性Cl>Si>Al,所以这三种元素第一电离能由大到小的顺序为Cl>Si>Al。Al3+与过量氨水反应产生Al(OH)3沉淀和NH4+,反应的离子方程式为:Al3++3NH3. H2O=Al(OH)3 ↓+3NH4+。
(3)H原子核外有1个电子,O元素的原子最外层有6个电子,O原子与2个H原子形成2个共价键,使分子中每个原子都达到稳定结合,用电子式表示H2O的形成过程为:![]() 。
。
(4)原子核外有多少电子,则元素原子核外就有多少不同运动状态的电子,Si是14号元素,所以Si元素原子共有14种不同运动状态的电子。


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】为了纪念元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。回答下列问题:
(1)Ag与Cu在同一族,则Ag在周期表中_____(填“s”、“p”、“d”或“ds”)区。[Ag(NH3)2]+中Ag+空的5s轨道和5p轨道以sp杂化成键,则该配离子的空间构型是_____。
(2)表中是Fe和Cu的部分电离能数据:请解释I2(Cu)大于I2(Fe)的主要原因:______。
元素 | Fe | Cu |
第一电离能I1/kJ·mol-1 | 759 | 746 |
第二电离能I2/kJ·mol-1 | 1561 | 1958 |
(3)亚铁氰化钾是食盐中常用的抗结剂,其化学式为K4[Fe(CN)6]。
①CN-的电子式是______;1mol该配离子中含σ键数目为______。
②该配合物中存在的作用力类型有______(填字母)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
(4)MnO的熔点(1660℃)比MnS的熔点(1610℃)高,其主要原因是________。
(5)第三代太阳能电池利用有机金属卤化物碘化铅甲胺(CH3NH3PbI3)半导体作为吸光材料,CH3NH3PbI3具有钙钛矿(AMX3)的立方结构,其晶胞如图所示。

①AMX3晶胞中与金属阳离子(M)距离最近的卤素阴离子(X)形成正八面体结构,则M处于_______位置,X处于______位置(限选“体心”、“顶点”、“面心”或“棱心”进行填空)。
③CH3NH3PbI3晶体的晶胞参数为a nm,其晶体密度为dg·cm-3,则阿伏加德罗常数的值NA的计算表达式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色) ![]() 2CrO42-(黄色)+2H+ 。用K2Cr2O7溶液进行下列实验,结合实验,下列说法不正确的是( )
2CrO42-(黄色)+2H+ 。用K2Cr2O7溶液进行下列实验,结合实验,下列说法不正确的是( )
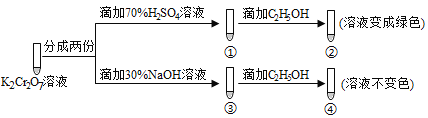
A. ①中溶液橙色加深,③中溶液变黄 B. ②中Cr2O72-被C2H5OH还原
C. 若向④中加入70%H2SO4溶液至过量,溶液变为橙色 D. 对比②和④可知K2Cr2O7酸性溶液氧化性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.实验室将少量Na保存在乙醇中
B.可用激光笔鉴别FeCl3溶液和Fe(OH)3胶体
C.32 g O3中含有的氧原子数约是3×6.02×1023
D.常温下,可以用铝制容器来储运浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
A. 2.0 mol·L-1 B. 1.5 mol·L-1 C. 0.18 mol·L-1 D. 0.24 mol·L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及少量杂质铁,利用电解法回收WC和制备Co2O3的工艺流程简图如下:
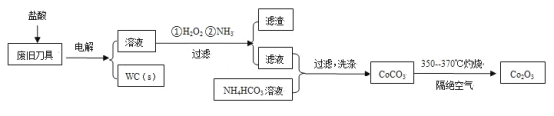
已知:在上述流程中,各种金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Fe2+ | Co2+ |
开始沉淀的pH | 1.9 | 7.0 | 6.5 |
沉淀完全的pH | 3.2 | 9.0 | 9.4 |
回答下列问题:
(1)以废旧刀具作阳极,不锈钢作阴极,盐酸为电解质溶液。电解时阳极的电极反应有:Co-2e-=Co2+和______。
(2)通入氨气的目的是调节溶液的pH,除去铁元素。由表中的数据可知,理论上可选择的pH的范围是_______。
(3)生成CoCO3的离子方程式是________。
(4)实验测得NH4HCO3溶液显碱性。制备CoCO3时,不能将滤液加入NH4HCO3溶液中,原因是_______。
(5)已知:Ksp(CoCO3)=1.4×10-13,Ksp(CoC2O4)=6.3×10-8。若仅从沉淀转化角度考虑,在0.01mol/L Na2C2O4溶液中加入CoCO3固体能否转化为CoC2O4沉淀?通过计算说明:_________。
(6)洗涤CoCO3不充分对最终产品纯度并无影响,但在焙烧时会造成环境污染,主要原因是____。
(7)CoCO3生成Co2O3的化学方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式见下图,取足量的Na、NaOH溶液和NaHCO3溶液分别和等物质的量的该物质在一定的条件下反应(必要时可以加热),完全反应后消耗Na、NaOH和NaHCO3三物质的物质的量之比

A.3∶4∶2B.3∶5∶2
C.3∶5∶1D.3∶4∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物粉末样品,可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的一种或几种,某同学试图通过实验确定该样品的成分,操作如下:
中的一种或几种,某同学试图通过实验确定该样品的成分,操作如下:
![]() 取一定量样品于烧杯中,加足量NaOH溶液,过滤得到固体A和无色溶液B;
取一定量样品于烧杯中,加足量NaOH溶液,过滤得到固体A和无色溶液B;
![]() 向B中加入足量
向B中加入足量![]() 溶液,出现白色沉淀,再加入足量稀硫酸,白色沉淀未消失,并有气体生成;
溶液,出现白色沉淀,再加入足量稀硫酸,白色沉淀未消失,并有气体生成;
![]() 向A中加入足量稀硫酸,固体完全溶解,得溶液C;
向A中加入足量稀硫酸,固体完全溶解,得溶液C;
![]() 向C中加入足量NaClO溶液,并调节pH至
向C中加入足量NaClO溶液,并调节pH至![]() ,产生红褐色沉淀,过滤后得到蓝绿色溶液D;
,产生红褐色沉淀,过滤后得到蓝绿色溶液D;
下列说法正确的是
A.通过操作![]() 所得的现象可以确定样品中含有
所得的现象可以确定样品中含有![]()
B.通过操作![]() 所得的现象可以确定样品中肯定不含
所得的现象可以确定样品中肯定不含![]()
C.通过实验可以确定样品中一定含有![]() 、
、![]()
D.将C滴入少量紫色![]() 溶液,若观察到紫色褪去,则可以确定样品中含有
溶液,若观察到紫色褪去,则可以确定样品中含有![]() 4
4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分析正确的是
A. 异丁烷的二氯代物有4种
B. 区别蛋白质和淀粉可用浓硝酸做颜色反应
C. 石蜡油分解产物均能使酸性KMnO4溶液褪色
D. 甲苯的硝化反应方程式为: ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com