
【题目】下列实验现象及相关的离子方程式均正确的是( )
A.Cl2与FeI2溶液反应,当n(Cl2):n(FeI2)=1:1时:2Fe2++2I﹣+2Cl2=2Fe3++I2+4Cl﹣
B.向Ba(NO3)2溶液中通人SO2气体,出现白色沉淀:Ba2++SO2+H2O=BaSO3↓+2H+
C.向H2O2溶液中滴加酸化的KMnO4溶液,KMnO4溶液褪色:2 MnO4+7 H2O2+6 H+=2Mn2++6O2↑+10 H2O
D.将等物质的量浓度、等体积的Ba(OH)2溶液和NaHSO4溶液混合:Ba2++SO ![]() +H++OH﹣=BaSO4↓+H2O
+H++OH﹣=BaSO4↓+H2O
【答案】D
【解析】解:A.n(Cl2):n(FeI2)=1:1时,氯气恰好氧化碘离子,亚铁离子不参与反应,正确的离子方程式为:2I﹣+Cl2=I2+2Cl﹣ , 故A错误;
B.向Ba(NO3)2溶液中通人SO2气体,发生氧化还原反应生成硫酸钡沉淀,正确的离子方程式为:3SO2+2NO ![]() +3Ba2++2H2O═3BaSO4↓+2NO↑+4H+ , 故B错误;
+3Ba2++2H2O═3BaSO4↓+2NO↑+4H+ , 故B错误;
C.向H2O2溶液中滴加酸化的KMnO4溶液,双氧水被氧化,KMnO4溶液褪色,正确的离子方程式为:2MnO4﹣+5H2O2+6H+=2Mn2++5O2↑+8H2O,故C错误;
D.等物质的量浓度、等体积的Ba(OH)2溶液和NaHSO4溶液混合,发生反应的离子方程式为:Ba2++SO ![]() +H++OH﹣=BaSO4↓+H2O,故D正确;
+H++OH﹣=BaSO4↓+H2O,故D正确;
故选D.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种原子序数依次增大的短周期元素.A与其余五种元素既不同周期,也不同主族;B、C、D、E、F五种元素分别位于五个相邻的主族,原子序数之和为54,其中B的单质为空气中的主要成分之一.
(1)A、B形成的化合物液态时可发生微弱电离,电离产生的阴离子的电子式为 .
(2)某含F的盐矿石的组成可以看作其氧化物中有 ![]() 的F被E替换,再由D平衡其电荷形成的.该矿石的化学式为 . (用氧化物形式表示)
的F被E替换,再由D平衡其电荷形成的.该矿石的化学式为 . (用氧化物形式表示)
(3)工业中制备单质E的阳极电极反应式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中,书写错误的是( )
A.Ca(OH)2=Ca2++2OH﹣
B.NaOH=Na++O2﹣+H+
C.HCl=H++Cl﹣
D.K2SO4=2K++SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知拆开1mol氢气中的化学键需要436.4kJ能量,拆开1mol氧气中的化学键需要消耗498kJ能量,形成水分子中的1molH﹣O键能够释放462.8kJ能量,则下列热化学方程式中正确的是( )
A.2H2(g)+O2(g)═2H2O(g)△H=﹣480.4kJ/mol
B.H2(g)+ ![]() O2(g)═H2O(l)△H=﹣240.2kJ/mol
O2(g)═H2O(l)△H=﹣240.2kJ/mol
C.2H2(g)+O2(g)═2H2O(g)△H=+480.4kJ/mol
D.H2(g)+ ![]() O2(g)═H2O(l)△H=﹣480.4kJ/mol
O2(g)═H2O(l)△H=﹣480.4kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.在离子化合物中,可能含共价键
B.含离子键的化合物不一定是离子化合物
C.在共价化合物中,可能含离子键
D.含共价键的化合物一定是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人类较早使用的金属之一。运用所学知识,回答下列问题。
(1)将FeCl3溶液滴入沸水可以制得Fe(OH)3胶体。鉴别Fe(OH)3胶体和FeCl3溶液的方法是____________________________________。
(2)胶体区别于其他分散系的本质特征是__________________________________。
(3)人体不易吸收三价铁,所以常用硫酸亚铁治疗缺铁性贫血。解释补铁的同时服用维生素C的原因__________________________________________________。
(4)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式__________________________________________。
工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案:
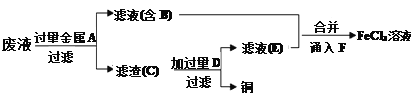
根据上述设计方案并结合所学知识回答以下问题。
(5)检验滤液E中金属阳离子的方法是___________________________________。
(6)通入F发生反应的离子方程式为_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z、W四种短周期元素,原子序数依次增大。X的阳离子就是一个质子。Z、W在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体。Y原子的最外层电子数是次外层电子数的2倍。请回答:
(1)Z2的电子式为_________,Y的原子结构示意图为________,YW2的结构式为________。
(2)将X2、W2 按下图所示通入某燃料电池中,其中,b电极的电极反应式为________。若有16gW2参加反应,转移的电子数是_______NA。
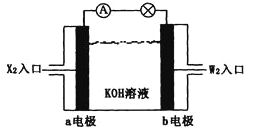
(3)由X、Y、Z、W四种元素组成的无机酸酸式盐,与足量的NaOH溶液在加热条件下反应的离子方程式为______________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 同温同压下,相同体积的两物质,它们的物质的量必相等
B. 任何条件下,等物质的量的氮气和一氧化碳所含的分子数必相等
C. 1L一氧化碳气体的质量一定比1L氧气的质量要小
D. 等体积、等物质的量浓度的强酸中所含的H+数一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然碳元素的相对原子质量为 12.01,若在自然界碳元素有12C、13C两种同位素,则 12C与13C的质量比为:
A. 等于 1:99 B. 大于 99:1 C. 等于 99:1 D. 小于 99:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com