
【题目】化合物X(只含两种短周期元素)是一种重要的还原剂。某同学取X做了如下实验
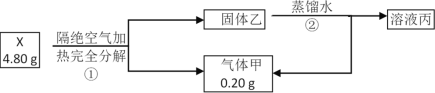
请回答:
(1)X的电子式是____________
(2)固体乙所含元素在元素周期表中的位置____________。
(3)写出X与水反应的化学方程式____________。
(4)X在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式____________。
【答案】![]() 第三周期,IA族 NaH+H2O=NaOH+H2↑ 3NaH+Fe2O3=2Fe+3NaOH
第三周期,IA族 NaH+H2O=NaOH+H2↑ 3NaH+Fe2O3=2Fe+3NaOH
【解析】
化合物X(只含两种短周期元素)是一种重要的还原剂,含两种元素的质量比为(4.80g-0.20g):0.20g=23:1,两种短周期元素分别为Na、H,化合物X为NaH,固体乙为Na,气体甲为H2,Na与水反应生成NaOH和H2,溶液丙含NaOH。
(1)X为NaH,X的电子式是![]() ,故答案为:
,故答案为:![]() ;
;
(2)固体乙为钠单质,所含元素钠在元素周期表中的位置第三周期,IA族。故答案为:第三周期,IA族;
(3)X与水反应的化学方程式为NaH+H2O=NaOH+H2↑,故答案为:NaH+H2O=NaOH+H2↑;
(4)X在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式3NaH+Fe2O3=2Fe+3NaOH。故答案为:3NaH+Fe2O3=2Fe+3NaOH;


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】已知由短周期元素构成的三种粒子:甲a(单核带一个单位正电荷)、乙I(四核不带电荷)、丙e(双核带一个单位负电荷),它们都有10个电子。物质A由甲、丙构成,B、C、D、K都是单质,反应①~⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如下图所示:
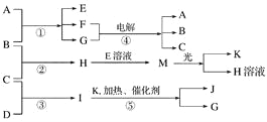
请填写下列空白:
(1)写出下列物质的化学式:B________,I________,J________。
(2) A的化学式是__________________。
(3)写出下列反应的离子方程式:
①H+E(溶液)→M_________________________________________________________。
②I溶于G________________________________________________________________。
(4)写出反应①的化学方程式_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
①三氯化铁溶液中加入铁粉:Fe3++Fe=2Fe2+
②碳酸镁与稀硫酸:MgCO3+2H+=H2O+CO2↑+Mg2+
③醋酸与大理石:2CH3COOH+CaCO3=Ca2++2CH3COO-+H2O+CO2↑
④Fe2+与H2O2(酸性):2Fe2++H2O2+2H+=2Fe3++2H2O
⑤钠与CuSO4溶液:2Na+Cu2+=2Na++Cu
⑥碳酸氢钙溶液与过量烧碱溶液混合:Ca2++HCO3-+OH-=CaCO3↓+H2O
A.①③④⑥B.②③④C.②③④⑥D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液X中可能含有下列离子中的若干种:Iˉ、![]() 、
、![]() 、
、![]() 、Na+、Mg2+、Fe3+,所含离子的物质的量浓度均相同。为了确定该溶液的组成,某同学取100mL上述溶液X,进行了如下实验:
、Na+、Mg2+、Fe3+,所含离子的物质的量浓度均相同。为了确定该溶液的组成,某同学取100mL上述溶液X,进行了如下实验:
(1)向溶液X中加入足量的Ba(OH)2溶液,得到白色沉淀;
(2)将(1)的反应混合液过滤,将足量盐酸加入沉淀中,沉淀部分溶解且产生气体。
下列说法正确的是
A.(2)中产生的气体可能含有SO2
B.溶液X中一定存在![]() 、
、![]() 、Mg2+
、Mg2+
C.溶液X中一定不存在Fe3+,可能存在Iˉ
D.无法确定溶液中是否含有Na+,需要做焰色反应才能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300mL某溶液中可能含有Na+、NH4+、Mg2+、Ba2+、CO32-、SO42-、Cl-中的若干种,现将此溶液分成三等份,进行如下实验:
①向第一份中加入AgNO3溶液,有白色沉淀产生;
②向第二份中加足量KOH溶液并加热,收集到气体0.04 mol;(铵盐与碱共热可产生氨气)
③向第三份中加足量BaCl2溶液,得到沉淀6.27g,加入足量盐酸充分反应后,剩余沉淀2.33g。根据上述实验,回答下列问题:
(1)实验③中生成沉淀的离子方程式为________,沉淀溶解的离子方程式为__________。
(2)溶液中一定不存在的离子有_________。
(3)实验①中加入AgNO3溶液,有沉淀产生,能否说明原溶液中含有Cl-?________(填“能”或“否”)理由是______________。
(4)推断钠离子是否存在并说明理由_________。若存在,计算其物质的量的浓度____________(若不存在,此问不作答)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种有机合成中间体,某研究小组采用如下路线合成X和一种常见的高分子化合物D。首先合成D和乙醇,线路如下:
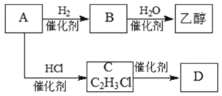
(1)已知A是一种常见的气态烃。写出A分子的结构式________________。
![]() 的化学方程式________________,该反应的类型是:________________。
的化学方程式________________,该反应的类型是:________________。
(2)写出化合物B的结构简式________________,实验室制取B反应的化学方程式:________________。乙醇中官能团的名称是:________。
进一步合成X线路如下:
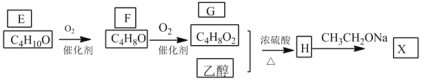
已知:①化合物E的结构中有2个甲基
②![]()

(3)若G中混有F,可以用来检验的试剂是________________,反应的化学方程式为________________。
(4)写出![]() 的化学方程式是________________;反应类型是________。
的化学方程式是________________;反应类型是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的二氧化硫和含0.7 mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应2SO2+O2![]() 2SO3。反应达到平衡后,将容器中的混合气体通过过量氢氧化钠溶液,气体体积减小了21.28 L;再将剩余气体通过一种碱性溶液吸收氧气,气体的体积又减少了5.6 L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)请回答下列问题:
2SO3。反应达到平衡后,将容器中的混合气体通过过量氢氧化钠溶液,气体体积减小了21.28 L;再将剩余气体通过一种碱性溶液吸收氧气,气体的体积又减少了5.6 L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)请回答下列问题:
(1)判断该反应达到平衡状态的标志是(填字母)__________________。
a.二氧化硫和三氧化硫浓度相等
b.三氧化硫百分含量保持不变
c.容器中气体的压强不变
d.三氧化硫的生成速率与二氧化硫的消耗速率相等
e.容器中混合气体的密度保持不变
(2)求该反应达到平衡时,消耗二氧化硫的物质的量占原二氧化硫的物质的量的百分比____。
(3)若将平衡混合气体的5%通入过量的氯化钡溶液中,生成沉淀的质量是多少?______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设X、Y、Z代表三种元素。已知:
①X+和Y-两种离子具有相同的电子层结构。
②Z元素原子核内质子数比Y元素原子核内质子数少9个。
③Y和Z两种元素可以形成四核42个电子的-1价阴离子。
据此,请填空:
(1)写出X、Y、Z三种元素的元素符号:X________,Y________,Z________。
(2)X、Y两种元素最高价氧化物对应水化物相互反应的离子方程式为___________。
(3)Y-的电子式____________。
(4)用电子式表示X、Z形成化合物的过程____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期主族元素,它们的原子序数依次增大,其中A元素原子核外电子仅有一种原子轨道,也是宇宙中最丰富的元素,B元素原子的核外p电子数比s电子数少1,C为金属元素且原子核外p电子数和s电子数相等,D元素的原子核外所有p轨道全满或半满。
(1)写出下列四种元素的元素名称:
A:___,B:____,C:____,D:____。
(2)写出C、D两种元素基态原子核外电子排布的电子排布图。C:___,D:___。
(3)写出A、B两种元素单质在一定条件下反应的化学方程式:____。
(4)写出B2A4的电子式:____。
(5)写出C3B2化合物与水反应的方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com