
| A、地壳中含量最多的金属元素是Al |
| B、金属一般是热和电的良导体 |
| C、自然界中绝大多数金属元素以游离态的形式存在 |
| D、金属一般呈银白色具有金属光泽 |
科目:高中化学 来源: 题型:
| A、铁和盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、足量碳酸氢钠溶液中滴加少量的石灰水:2HCO3-+Ca2++2 OH-═CaCO3↓+CO32-+2H2O |
| C、碳酸钙溶于稀醋酸:CO32-+2H+=H2O+CO2↑ |
| D、氯化钙溶液与CO2的反应:CO2+Ca2++H2O═CaCO3↓+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
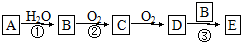
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
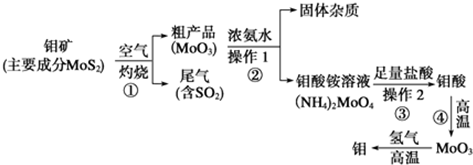
| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | - | - | - |
| 完全沉淀时的pH | 3.7 | 11.1 | 8(>9溶解) | 9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
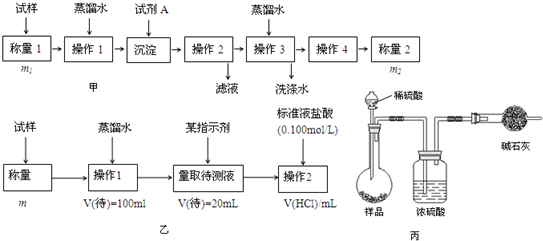
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com