
【题目】在容积一定的密闭容器中,反应A2(g)+B2(g)![]() xC(g),符合图Ⅰ所示关系。对图Ⅱ的说法正确的是(T为温度、P为压强、t为时间) ( )
xC(g),符合图Ⅰ所示关系。对图Ⅱ的说法正确的是(T为温度、P为压强、t为时间) ( )
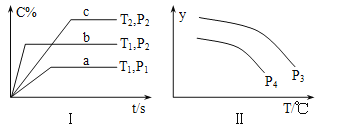
A. P3<P4,y为A2转化率
B. P3<P4,y为A2浓度
C. P3>P4,y为混合气密度
D. P3>P4,y为C的体积分数
【答案】D
【解析】由图Ⅰ,a、b曲线温度相等,则先达到平衡的b曲线对应的压强p2更大,曲线b的C物质的含量比压强小的P1大,所以反应后气体系数更小,即1+1>x,x只能等于1。b、c曲线压强相等,则先达到平衡的b曲线对应的温度T1更高,曲线b的C物质含量比温度低的T2的小,说明升高温度,平衡逆向移动,正反应为放热反应。
对于图Ⅱ,等温时p3的y值更大。如果P3<P4,压强由P3变化到P4,压强增大时平衡向气体体积减小的正反应方向移动,反应物A2的转化率增大,因此,当y表示A2的转化率时,温度相同时压强为P4的曲线应当位于压强为P3的曲线上方,所以A错误;而温度升高时,上述放热反应平衡向逆反应方向移动,A2的浓度增大,因此,当y表示A2浓度时,曲线的走向应当是逐渐增大,所以B错误。C、由于容器体积一定、混合气体总质量不变,所以混合气体的密度始终不变,当y表示混合气体密度时,每条图线均为平行与横坐标的直线,因此C错误。D、P3>P4,压强由P3变化到P4,压强减小时平衡向逆反应方向移动,产物C不断消耗,当温度相同时,压强更小的P4对应的产物C体积分数更小,曲线位于下方,图Ⅱ符合;而温度升高时,平衡向逆反应方向移动,产物C不断消耗,y表示C的体积分数时,曲线走向逐渐向下,图Ⅱ也符合,所以D正确。正确答案D。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】下列有关概念的叙述正确的是
A. 水玻璃、王水、液氨均为混合物
B. Na2O2、CaH2均含有离子键和共价键
C. 非金属氧化物一定是酸性氧化物
D. 生成盐和水的反应不一定是中和反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图所示。
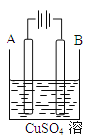
请回答:
①A电极对应的金属是 (写元素名称),B电极的电极反应式是 。
②镀层破损后,镀铜铁和镀锌铁更容易被腐蚀的是 。
(2)下列哪个装置可防止铁棒被腐蚀
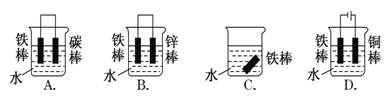
(3)利用右图装置可以模拟铁的电化学防护。
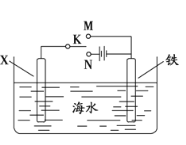
①若X为碳棒,为减缓铁的腐蚀,开关K应置于 处。假设海水中只有NaCl溶质,写出此时总离子反应方程式:
②若X为锌,开关K置于M处,该电化学防护法称为 ,写出铁电极处的电极反应式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在25℃、101kPa下,1g甲醇(CH3OH,常温为液体)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为____________________
(2)氨可用作碱性燃料电池的燃料,电池反应为 4NH3+3O2=2N2+6H2O,则氨燃料电池的负极电极反应为 ____________________.
(3)现有25℃、pH=13的Ba(OH)2溶液,
①该Ba(OH)2溶液的物质的量浓度为___________________
②加水稀释100倍,所得溶液中由水电离出c(OH-)=_____________________
③与某浓度盐酸溶液按体积比(碱与酸之比)1 : 9混合后,所得溶液pH=11,该盐酸溶液的pH=________。
(4)盐类水解在实际生产生活中有重要的用途.常用的泡沫灭火器就是利用了小苏打和硫酸铝溶液的反应原理来灭火,写出该反应的离子方程式:_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是( )
A. NH4+、SO42-、NO3- B. Ba2+、SO42-、NO3-
C. Na+、H+、HCO3- D. NH4+、OH-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com