
【题目】周期表前四周期的元素 a、b、c、d、e,原子序数依次增大。a 的核外电子总数与其周期数相同,b 的价电子层中的未成对电子有 3 个,c 的最外层电子数为其内层电子数的 3 倍,d 与 c 同族;e 的基态原子的价电子数是其 N 层电子数的4 倍。回答下列问题:
(1)a 的基态原子核外电子运动的轨道呈_____形。
(2)b 的基态原子的核外电子占据_____个原子轨道。
(3)c 的价电子轨道表示式为_____。
(4)b 与 c 的第一电离能相比,较大的是_________(填元素符号),理由是_____。
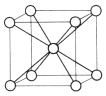
(5)e 的晶体在一定温度下的晶胞结构如图,其一个晶胞的质量为_________g(用含 NA 的式子表示),晶体中空间利用率为_______(用 含 π 的式子表示)。
【答案】球 5 ![]() N N的外围电子排布为2s22p3,p轨道处于半充满状态,比较稳定,较难失电子,故第一电离能较大
N N的外围电子排布为2s22p3,p轨道处于半充满状态,比较稳定,较难失电子,故第一电离能较大 ![]() (或
(或![]() )
) ![]()
【解析】
周期表前四周期的元素 a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,a为H元素;b 的价电子层中的未成对电子有3个,b为N元素;c的最外层电子数为其内层电子数的3倍,d与c同族,c是O元素,d是S元素;e的基态原子的价电子数是其N层电子数的4倍,e是Fe元素。
(1)a为H元素,电子去呈球形,H的基态原子核外电子运动的轨道呈球形。
(2)b为N元素,N的基态原子的核外电子排布式为1s22s22p3,N的基态原子的核外电子占据1+1+3=5个原子轨道。
(3)c为O元素,c的价电子轨道表示式为![]() 。
。
(4)N与O的第一电离能相比,较大的是N(填元素符号),理由是N的外围电子排布为2s22p3,p轨道处于半充满状态,比较稳定,较难失电子,故第一电离能较大。
(5)根据晶胞结构,每个晶胞中含Fe原子个数为8×1/8+1=2,其一个晶胞的质量为![]() (或
(或![]() );设Fe的原子半径为r,Fe晶胞中处于体对角线上的原子相邻,体对角线长度为晶胞棱长的
);设Fe的原子半径为r,Fe晶胞中处于体对角线上的原子相邻,体对角线长度为晶胞棱长的![]() 倍,则晶胞边长=
倍,则晶胞边长=![]() ,空间利用率为
,空间利用率为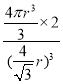 =
=![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】恒温恒容时,在体积为0.5L的密闭容器中,进行NO2和N2O4之间发生反应N2O4(g)![]() 2NO2(g),如图所示。
2NO2(g),如图所示。
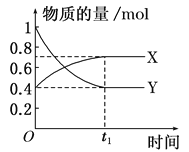
(1)曲线________(填“X”或“Y”)表示NO2的物质的量随时间变化的曲线。
(2)若升高温度,则υ(正)________(填“加快”或“减慢”,下同),υ(逆)________。
(3)若t1=10s,则用υ(NO2)=________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】抗丙肝新药的中间体 合成路线图如下:
合成路线图如下:

已知:-Et为乙基。
(1)![]() 的名称是____,
的名称是____,![]() 所含官能团的名称是____。
所含官能团的名称是____。
(2) 的分子式为____。
的分子式为____。
(3)反应②化学方程式为________,反应③的反应类型是____。
(4)写出与 互为同分异构体的芳香类化合物的结构简式(核磁共振氢谱为四组峰,峰面积比为1:2:2:6,且不含-NH2)____
互为同分异构体的芳香类化合物的结构简式(核磁共振氢谱为四组峰,峰面积比为1:2:2:6,且不含-NH2)____
(5)设计由乙醇、1,3-丁二烯和甲氨( CH3NH2)合成![]() 路线(其他试剂任选)。__________
路线(其他试剂任选)。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 是具有相同电子层结构的短周期元素形成的简单离子。下列叙述正确的是
是具有相同电子层结构的短周期元素形成的简单离子。下列叙述正确的是
A.原子半径: C>D>A>BB.原子序数: b>a>d>c
C.离子半径: D>C>A>BD.单质还原性: A>B>C>D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示一些晶体中的某些结构,请回答下列问题:
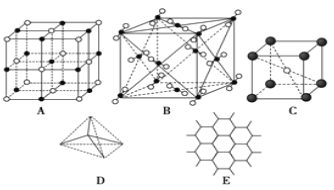
(1)代表金刚石的是(填编号字母,下同)_____,其中每个碳原子与_____个碳原子最近且距离相等。
(2)代表石墨的是_____,每个正六边形占有的碳原子数平均为_____个。
(3)代表 NaCl 的是_________,每个Na+周围与它最近且距离相等的Cl-有_____个。
(4)代表 CsCl 的是_____,每个Cs+与_____个Cl-紧邻。
(5)代表干冰的是_____,每个 CO2 分子与_____个 CO2 分子紧邻。
(6)已知石墨中碳碳键的键长比金刚石中碳碳键的键长短,则上述五种物质熔点由高到低的排列顺序为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取少量乙酸乙酯的装置图.下列关于该实验的叙述中,不正确的是
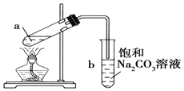
A. 向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸
B. 试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象
C. 实验时加热试管a的目的是及时将乙酸乙酯蒸出并加快反应速率
D. 采用长玻璃导管有导气兼冷凝的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中正确的是

A. ①②中Mg作负极、③④中Fe作负极
B. ②中A1作负极,电极反应式为2A1-6e-=2Al3+
C. ③中Fe作负极,电极反应式为Fe-2e-=Fe2+
D. ④中Cu作正极,电极反应式为O2+4e-+2H2O=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里研究不同价态硫元素之间的转化
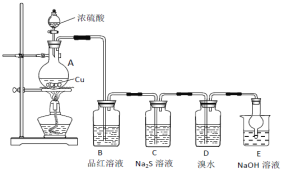
(1)A中发生反应的化学方程式为________________。
(2)B中的现象是__________________。
(3)C中出现淡黄色沉淀,反应中Na2S做 ____________(填“氧化剂”或“还原剂”)。
(4)D溴水褪色,该反应S元素的价态变化是由+4价变为________________价。
(5)某同学认为D中换成H2O2溶液也可以实现上述硫元素的价态转化,并通过实验进一步证明了他的观点。实验方案和现象为:取D中反应后的溶液于试管中,_________。
(6) E的作用是_____________,离子方程式为_________________________。
(7)上述实验体现SO2 的性质有__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来分枝酸称为某些生化研究的热点,其结构如图所示。下列关于分枝酸的说法,正确的是( )
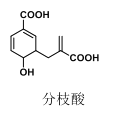
A.该化合物的分子式为C11H12O5,且含有两种官能团
B.能使酸性高锰酸钾溶液褪色,也能使溴的四氯化碳溶液褪色,且原理相同
C.1mol 分枝酸最多能与 3mol NaOH 发生中和反应
D.1mol 分枝酸与1mol Br2发生加成反应,可能得到4 种产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com