
【题目】I.下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
第二周期 | ① | ② | ③ | |||||
第三周期 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
第四周期 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是:________(填元素符号),
(2)在最高价氧化物对应的水化物中,碱性最强的化合物是________(填化学式),在常温下该化合物和元素⑦的单质反应的离子方程式__________。
(3)用电子式表示元素④与⑥的化合物的形成过程:__________。
(4)表示①与⑦的化合物的电子式_______,该化合物是由______(填“极性”或“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是____________(用化学式表示)。
II.①CBr2;②H2O;③NH4Cl;④H2O2;⑤Na2O2;⑥Ca(OH)2;⑦HClO;⑧I2;⑨He
只含有离子键的是(用序号回答)_____,即含离子键又含共价键是(用序号回答)_____,其中含有非极性共价键的共价化合物是(用序号回答)_____,常温时为固体,当其熔化时,不破坏化学键的是(用序号回答)_____。
【答案】Ar KOH Cl2+2OH-=Cl-+ClO-+H2O ![]()
 极性 S2->Cl->O2- ① ③⑤⑥ ④ ⑧
极性 S2->Cl->O2- ① ③⑤⑥ ④ ⑧
【解析】
I.根据元素在周期表的位置可知:①是C元素,②是N元素,③是O元素,④是Na元素,⑤是Al元素,⑥是S元素,⑦是Cl元素,⑧是Ar元素,⑨是K元素,⑩是Br元素,然后根据元素周期律分析解答;
II.根据构成物质元素的金属性、非金属性强弱判断物质含有的化学键类型,结合各物质的构成微粒及微粒间的作用力判断物质熔化时破坏的作用力。
I.根据上述分析可知:①是C,②是N,③是O,④是Na,⑤ 是Al,⑥是S,⑦是Cl,⑧是Ar,⑨是K,⑩是Br元素。
(1)同一周期中惰性气体元素的原子核外电子排布达到最外层2个或8个电子的稳定结构,化学性质不活泼,在上述元素中,化学性质最不活泼的是Ar元素;
(2)元素的金属性越强,其最高价氧化物对应的水化物的碱性就越强,在上述元素中金属性最强的元素是K元素,所以最高价氧化物对应的水化物中,碱性最强的化合物是KOH;⑦是Cl元素,Cl2与KOH反应产生KCl、KClO、H2O,该反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O;
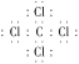
(3)元素④与⑥形成的化合物是Na2S,该化合物为离子化合物,Na+与S2-之间通过离子键结合,用电子式表示其形成过程为:![]()
(4)①与⑦的化合物的化学式是CCl4,由于C、Cl都是非金属元素,两种元素的原子间以共价键形成共价化合物,其电子式为: ;C、Cl是不同的元素,C-Cl键为极性共价键;
;C、Cl是不同的元素,C-Cl键为极性共价键;
(5)③、⑥、⑦三种元素形成的离子分别是O2-、S2-、Cl-,O2-核外有2个电子层,而S2-、Cl-的核外有3个电子层,由于离子核外电子层数越多,离子半径越大;对于电子层结构相同的离子,核电荷数越大,离子半径越小,因此这三种离子半径由大到小的顺序是:S2->Cl->O2-;
II. ①CaBr2是离子化合物,只含有离子键,常温呈固态,熔化时破坏离子键;②H2O是共价化合物,只含极性共价键,常温呈液态;③NH4Cl是离子化合物,含有离子键、极性共价键,常温呈固态,熔化时破坏离子键;④H2O2是共价化合物,含极性共价键、非极性共价键,常温呈液态;⑤Na2O2是离子化合物,含离子键、非极性共价键,常温呈固态,熔化时破坏离子键;⑥Ca(OH)2是离子化合物,含离子键、极性共价键,常温呈固态,熔化时破坏离子键;⑦HClO是共价化合物,含极性共价键,熔化时破坏分子间作用力;⑧I2是非金属单质,含有非极性共价键,在室温下呈固态,熔化时破坏分子间作用力;⑨He是单原子分子,无化学键,常温呈气态;
综上所述可知:只含有离子键的是①,既含有离子键又含有共价键的是③⑤⑥,含有非极性共价键的共价化合物是④;常温时为固体,当其熔化时,不破坏化学键的物质是⑧。


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.SO2的水溶液能导电,故SO2为电解质
B.阳离子在反应中只能得电子被还原作氧化剂
C.标准状况下,6.72L的NH3的物质的量为0.3mol
D.氯水、液氨、空气、盐酸都是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室回收废水中苯酚的过程如图所示。下列分析错误的是( )
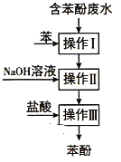
A. 操作Ⅰ中苯作萃取剂,多次萃取后检验是否萃取干净可选择三氯化铁溶液
B. 苯酚钠是离子化合物,在苯中的溶解度比在水中的小
C. 通过操作Ⅱ苯可循环使用, 三步操作均需要分液漏斗,
D. 操作中苯酚碰到皮肤,需用NaOH溶液清洗后,再用大量水不断冲洗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在含CH3COOH和CH3COO-的溶液中, CH3COOH、CH3COO-二者中各自所占的物质的量分数(a)随溶液pH变化的关系如图所示。

下列说法不正确的是
A. 在pH<4.76的溶液中,c(CH3COO-)<c(CH3COOH)
B. 在pH=7的溶液中,a(CH3COOH)=0,a(CH3COO-)=1.0
C. 在pH>4.76的溶液中,c(CH3COO-)与c(OH-)之和可大于c(H+)
D. 在pH=4.76的溶液中加盐酸,a(CH3COOH)与a(CH3COO-)之和保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是某同学设计的用于鉴别苯和苯的同系物的几种方法或试剂,其中最适合的是( )
A. 液溴和铁粉B. 浓溴水
C. 酸性KMnO4溶液D. 在空气中点燃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的化学式为C8H10,能使酸性KMnO4溶液褪色。
(1)若分子中含有一个苯环,则该烃属于_____,是_____的同系物。该烃具有_____种同分异构体。
(2)若为链烃且有两个甲基取代基,写出一种分子中只含叁键的同分异构体的结构简式:________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于烷烃的表述正确的是( )
A.乙烷的结构式为CH3CH3
B.C5H12分子的某种结构为CH3CH2(CH3)CH2CH3
C.CH3CH2CH(C2H5)CH2CH2CH3与CH3CH2CH2CH(C2H5)CH2CH3互为同分异构体
D.C4H10的一氯代物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表所列各组物质中,物质之间通过一步反应不能实砚如下图所示转化的是
选项 | X | Y | Z |
A | Na | NaOH | NaCl |
B | Si | SiO2 | Na2SiO3 |
C | Cl2 | HClO | NaClO |
D | NO | NO2 | HNO3 |

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大。X是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,R与X同主族;Y、R、Q最外层电子数之和为8,M的单质为黄绿色有毒气体。请回答下列问题:
(1)Q的离子结构示意图是__________________。
(2)六种元素中,原子半径最大的是___________。(写元素符号)
(3)Z、Q、M简单离子半径由大到小的顺序为(写元素离子符号)____________。
(4)Y和Z的气态氢化物中,热稳定性强的是________(用物质化学式表示)。
(5)Y的气态氢化物与X和M形成的化合物反应,产物的化学式为________,其中存在的化学键类型为____________________。
(6)X与Z可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:_______________________________________________________________。
(7)单质M与水反应的离子方程式为____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com