
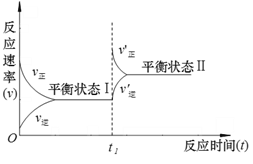
【题目】下图是恒温下H2(g)+I2(g)![]() 2HI(g)+Q(Q>0)的化学反应速率随反应时间变化的示意图,t1时刻改变的外界条件是
2HI(g)+Q(Q>0)的化学反应速率随反应时间变化的示意图,t1时刻改变的外界条件是
A. 升高温度
B. 增大压强
C. 增大反应物浓度
D. 加入催化剂
【答案】C
【解析】从题干给的图示得出0-t1时间内是建立化学平衡状态的过程,t1以后改变条件,原平衡被破坏,在新的条件下重新建立平衡,升高温度,正逆反应速率同时增大(增加的起点与原平衡不重复),且H2(g)+I2(g) ![]() 2HI(g)+Q(Q>0)是放热反应,逆反应增大的倍数大于正反应,即逆反应的曲线在上方,A选项错误;增大压强,对H2(g)+I2(g)
2HI(g)+Q(Q>0)是放热反应,逆反应增大的倍数大于正反应,即逆反应的曲线在上方,A选项错误;增大压强,对H2(g)+I2(g) ![]() 2HI(g)+Q(Q>0)平衡不移动,但浓度增大,正逆反应速率同等程度增大,即应该新平衡曲线是高于原平衡的一条直线,B选项错误;增加反应物浓度,正反应速率应该瞬间提高,而生成物浓度瞬间不变,其逆反应速率与原平衡相同,增加反应物浓度,平衡正向移动,正反应曲线在上方,C正确;加入催化剂能够同等程度改变正逆反应速率,即是高于原平衡的一条直线,D错误;正确答案C。
2HI(g)+Q(Q>0)平衡不移动,但浓度增大,正逆反应速率同等程度增大,即应该新平衡曲线是高于原平衡的一条直线,B选项错误;增加反应物浓度,正反应速率应该瞬间提高,而生成物浓度瞬间不变,其逆反应速率与原平衡相同,增加反应物浓度,平衡正向移动,正反应曲线在上方,C正确;加入催化剂能够同等程度改变正逆反应速率,即是高于原平衡的一条直线,D错误;正确答案C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式:___________。
(2)H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银.
①(H3PO2)中,磷元素的化合价为___________。
②利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为:___________(填化学式);
③NaH2PO2是 正盐还是酸式盐?___________,其溶液显___________性(填“弱酸性”、“中性”、或者“弱碱性”)。
(3)H3PO2的工业制法是:将白磷(P4)与氢氧化钡溶液反应生成PH3气体和Ba(H2PO2)2,后者再与硫酸反应,写出白磷与氢氧化钡溶液反应的化学方程式___________。
(4)(H3PO2)也可以通过电解的方法制备.工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):

①写出阳极的电极反应式___________;
②分析产品室可得到H3PO2的原因___________;
③早期采用“三室电渗析法”制备H3PO2,将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室,其缺点是___________杂质。该杂质产生的原因是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
金属铁及其化合物在材料、航空工业上有重要用途。回答下列相关问题:
(1)基态钛原子中有__________个状态不同的电子,最高能层电子的电子云轮廓图形状为__________,写出其价电子的轨道表达式__________。
(2)化合物TiO2不仅是常用的白色颜料,也是一些反应的良好催化剂,如:

有机物X中C原子的杂化轨道类型为__________,1mol Y中所含σ键的数目是__________。
(3)已知TiCl4在常温下是无色液体,TiCl4的晶体类型是__________晶体,其空间构型是__________。
(4)自然界中有丰富的钛矿资源,如右图表示的是钡钛矿晶体的晶胞结构,经X射线分析,该晶胞为正方体,晶胞参数为apm。
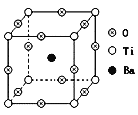
写出钡钛矿晶体的化学式__________,其密度是__________g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列情况中,会对人体健康造成较大危害的是 ( )
A.用SO2漂白食品B.用小苏打发酵面团制作馒头
C.用食醋清洗热水瓶胆内壁附着的水垢D.用ClO2对自来水进行杀菌消毒。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝氢化钠(NaAlH4) 是有机合成的重要还原剂。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质) 为原料制备铝氢化钠的一种工艺流程如下:
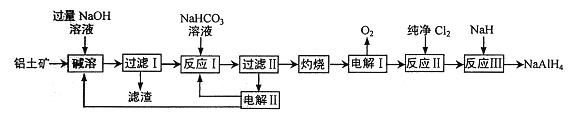
注: SiO2在“碱溶”时转化为铝硅酸钠(Na2Al2SixO8) 沉淀。
(1)铝硅酸钠(Na2Al2SixO8) 可以用氧化物的形式表示其组成,形式为________。
(2) “过滤I”中滤渣主要成分有________(写名称)。向“过滤I”所得滤液中加入NaHCO3溶液,反应的离子方程式为_______________、______________。
(3) “电解I”的另一产物在1000℃时可与N2反应制备AlN,在这种产物中添加少量NH4Cl固体并充分混合,有利于AlN 的制备,其主要原因是__________________。
(4)“电解II”是电解Na2CO3溶液,原理如图所示。
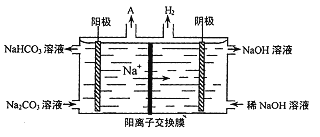
阳极的电极反应式为_________________。
(5)铝氢化钠遇水发生剧烈反应产生大量气泡,其反应的化学方程式为_____________,每产生1mol 气体转移电子数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为原子序数依次增大的短周期元素,已知A、B、D三种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4。
(1)写出下列元素符号: B________,D________。
(2)A与D两元素可形成化合物,用电子式表示其化合物的形成过程:________。
(3)A在空气中燃烧生成原子个数比为1:1的化合物,写出其电子式为________。
(4)元素C的最高价氧化物与元素A的最高价氧化物的水化物反应的离子方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《新科学家》杂志发表的一份研究报告指出,西伯利亚西部永久冻土层开始融化,会释放出大量的温室气体,从而加剧全球变暖,形成可怕的恶性循环。下列不属于温室气体的是( )
A.二氧化硫
B.氟氯代烷
C.二氧化碳
D.甲烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com