
【题目】中国是最早发现并使用青铜器的国家。司母戊鼎是迄今为止出土的世界上最大、最重的青铜礼器,享有“镇国之宝”的美誉(如图1)。
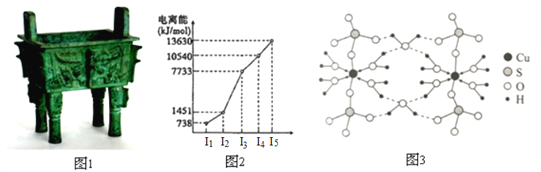
(1)Cu原子的外围电子排布式为_______。
(2)图2所示为第四周期某主族元素的第一至五电离能数据,该元素是_______,I3远大于I2的原因是_______。
(3)图3是某含铜配合物的晶体结构示意图。
①晶体中H2O和SO42-的中心原子的杂化类型为_______,试判断H2O和SO42-的键角大小关系并说明原因_______。
②图3中的氢键有(H2O)O—H···O(H2O)和_______。
③写出该配合物的化学式_______。
(4)一种铜的氯化物晶胞结构如下图所示。
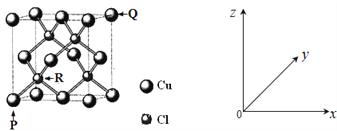
该化合物的化学式为_______,已知P、Q、R的原子坐标分别(0,0,0)、(1,1,1)、 (![]() ,
,![]() ,
,![]() ),若Cu原子与最近的Cl原子的核间距为a pm,则该晶体的密度计算表达式为_______。
),若Cu原子与最近的Cl原子的核间距为a pm,则该晶体的密度计算表达式为_______。
【答案】 3d104s1 Ca(或钙) Ca原子失去2个电子以后达到稳定结构,再失去1个电子很困难 sp3、sp3 H2O分子键角小于的SO42-键角,因为H2O中O存在2对孤电子对而SO42-中的S不存在,孤电子对成键电子的斥力大于成键电子对成键电子的斥力 (H2O)O—H···O(SO42-) [Cu(H2O)4]SO4·H2O CuCl ![]()
![]() g/cm3
g/cm3
【解析】(1)Cu为第29号元素,原子的外围电子排布式为:3d104s1 ;
(2)根据图示第四周期某主族元素的第一至五电离能数据,电离能突变在第三电离能,故该元素为第四周期第IIA族元素,该元素是Ca;I3远大于I2的原因是Ca原子失去2个电子以后达到稳定结构,再失去1个电子很困难;
(3)①晶体中H2O和SO42-的价层电子对数均为4对,故中心原子的杂化类型均为sp3;H2O的键角小于SO42-的键角,因为H2O中O存在2对孤电子对而SO42-中的S没有孤对电子,孤电子对成键电子的斥力大于成键电子对成键电子的斥力,故键角更小;
②图3中的氢键有(H2O)O—H···O(H2O)和(H2O)O—H···O(SO42-);
③该配合物中,中心离子是Cu2+,配体是水,配位数是4,阴离子是硫酸根,还有一个结晶水,故其化学式为:[Cu(H2O)4]SO4·H2O;
(4)铜的氯化物晶胞结构中Cu占据了顶点和面心,Cl占据了体内4个位置,故该化合物的化学式为CuCl,已知P、Q、R的原子坐标分别(0,0,0)、(1,1,1)、 (![]() ,
,![]() ,
,![]() ),若Cu原子与最近的Cl原子的核间距为a pm,即为体对角线的四分之一,故则该晶体的边长为:
),若Cu原子与最近的Cl原子的核间距为a pm,即为体对角线的四分之一,故则该晶体的边长为:![]() ×10-10cm,该晶胞的体积为:
×10-10cm,该晶胞的体积为:![]() ×10-30cm3,一个晶胞的质量为:
×10-30cm3,一个晶胞的质量为:![]() g,故晶胞的密度计算表达式为:
g,故晶胞的密度计算表达式为: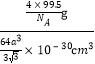 =
= ![]()
![]() g/cm3。
g/cm3。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】化合物G是一种药物合成中间体,其合成路线如下:
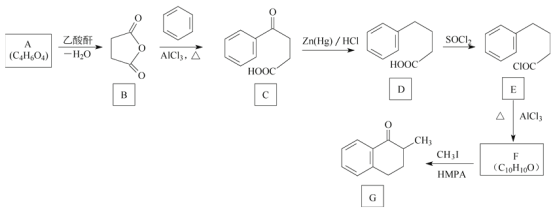
已知A分子中只含有一种官能团且能与NaHCO3反应生成CO2。回答下列问题:
(1)A的化学名称是___________。
(2)C中的官能团名称是___________。
(3)D生成E的反应类型是___________。
(4)F的结构简式是___________。
(5)A与乙二醇在催化剂作用下反应生成可生物降解型聚酯PES,该反应的化学方程式为____________。
(6)X是G的同分异构体,满足下列条件的X共有___________种(不考虑立体异构),其中核磁共振氢谱有5组峰且面积比为6:2:2:1:1的是___________(写结构简式)。
①含苯环且苯环上只有两个取代基;②含醛基且与苯环直接相连;③除苯环外不含其他环状结构。
(7)设计由苯和甲苯制备![]() 的合成路线:_________(无机试剂任选)。
的合成路线:_________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莫尔盐是硫酸盐的一种复盐,是一种重要的化学试剂,它的水溶液中加入KSCN不显红色,并有如图所示的反应:
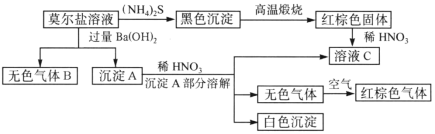
根据以上关系,按要求填空:
(1)可用检验气体B__________________。
(2)莫尔盐的化学式为____________________。
(3)部分沉淀A与稀HNO3反应的离子方程式是_____________________。
(4)古代硫酸的制法是隔绝空气锻烧绿矾(FeSO4·7H2O),将蒸气冷却可制得一种无色粘稠的液体“绿矾油”,剩余的固体为红棕色。(已知SO3的熔点是16.8°C,沸点是44.8°C,再加矾受热分解的产物)

①装置的连接顺序为______________。
②B的作用是验证该反应有水生成,其中的试剂为_________,实验过程中发现F中溶液褪色,D中出现无色粘稠液体,则煅烧绿矾的反应方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是镁元素和硫元素的相关信息,由此不能得到的信息是( )

A.镁属于金属元素
B.镁原子核内有12个质子
C.镁离子与硫离子的电子层数相等
D.在化学反应中,1个硫原子容易得到2个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L恒温密闭容器中通入气体X并发生反应:2X(g)![]() Y(g)(正反应放热),X的物质的量n(X)随时间t变化的曲线如图所示(图中的两条曲线分别代表有、无催化剂的情形),下列叙述正确的是( )
Y(g)(正反应放热),X的物质的量n(X)随时间t变化的曲线如图所示(图中的两条曲线分别代表有、无催化剂的情形),下列叙述正确的是( )
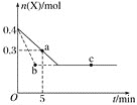
A.实线表示使用催化剂的情形
B.b、c两点表明反应在相应的条件下达到了最大限度
C.反应进行到a点时放出的热量多于反应进行到b点时放出的热量
D.反应从开始到a点的平均反应速率可表示为v(Y)=0.01mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫—空气质子交换膜燃料电池将化学能转变成电能的同时,实现了制硫酸、发电、环保三位一体的结合,降低了成本提高了效益,其原理如图所示。下列说法错误的是( )

A. Pt1电极附近发生的反应为:SO2+2H2O-2e-===SO![]() +4H+
+4H+
B. Pt2电极附近发生的反应为O2+4e-===2O2-
C. 该电池放电时电子从Pt1电极经过外电路流到Pt2电极
D. 相同条件下,放电过程中消耗的SO2和O2的体积比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种常见的单质,B、C为中学化学常见的化合物,A、B、C均含有元素X。它们有如下的转化关系(部分产物及反应条件已略去),下列判断正确的是
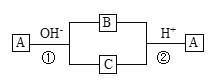
A.X元素可能为Al
B.X元素不一定为非金属元素
C.反应①和②互为可逆反应
D.反应①和②一定为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图结构的说法不正确的是( )
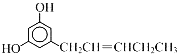
A. 分子中既有![]() 键又有π键
键又有π键
B. 碳原子有sp、sp2、sp3三种杂化方式
C. O—H键的极性强于C-H键的极性
D. 羟基中氧原子采取sp3杂化,VSEPR模型为四面体形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ |
(1)在这些元素中,化学性质最不活泼的是:___(填具体元素符号或化学式,下同)。⑥元素的原子结构示意图是___。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是__,碱性最强的化合物的化学式是___。
(3)最高价氧化物是两性氧化物的元素是_;写出它最高价氧化物对应水化物与氢氧化钠反应的化学方程式__。
(4)元素③与④形成淡黄色化合物的电子式:___,该化合物属于___(填“共价”或“离子”)化合物。
(5)用电子式表示③与①最高价态形成的化合物的形成过程___,将标准状况下4.48L该化合物通入足量的③和④形成的淡黄色固体化合物中,充分反应后,固体的质量增加___g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com