
【题目】(1)一定条件下的密闭容器中,反应3H2(g)+3CO(g)![]() CH3OCH3(二甲醚)(g)+CO2(g) ΔH<0达到平衡,要提高CO的转化率,可以采取的措施是 (填字母代号)。
CH3OCH3(二甲醚)(g)+CO2(g) ΔH<0达到平衡,要提高CO的转化率,可以采取的措施是 (填字母代号)。
a.升高温度b.加入催化剂 c.减小CO2的浓度d.增加CO的浓度 e.分离出二甲醚
(2)已知反应②2CH3OH(g)![]() CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
①比较此时正、逆反应速率的大小:v(正) v(逆)(填“>”“<”或“=”)。
②若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH)= ;该时间内反应速率v(CH3OH)= 。
【答案】 (1)c、e (2)①> ②0.04 mol·L-1 0.16 mol·(L·min)-1
【解析】
试题 (1)正反应是放热反应,升高温度平衡左移,CO转化率减小;加入催化剂,平衡不移动,转化率不变;减少CO2的浓度、分离出二甲醚,平衡右移,CO转化率增大;增大CO浓度,平衡右移,但CO转化率降低,故选c、e。
(2)此时的浓度商Qc==1.86<400,反应未达到平衡状态,向正反应方向移动,故v(正)>v(逆);设平衡时生成物的浓度为(0.6 mol·L-1+x),则甲醇的浓度为(0.44 mol·L-1-2x),根据平衡常数表达式400=,解得x=0.2 mol·L-1,故0.44 mol·L-1-2x=0.04 mol·L-1。
由表可知,甲醇的起始浓度为(0.44+1.2) mol·L-1=1.64 mol·L-1,其平衡浓度为0.04 mol·L-1,10 min内变化的浓度为1.6 mol·L-1,故v(CH3OH)=0.16 mol·(L·min)-1。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。该燃料电池以氢气为燃料,空气为氧化剂,铂作催化剂,导电离子是H+。下列对该燃料电池的描述中正确的是( )
①正极反应为:O2+4H++4e-2H2O
②负极反应为:2H2-4e-4H+
③总的化学反应为:2H2+O2![]() 2H2O
2H2O
④氢离子通过电解质向负极移动
A. ①② B. ②③④ C. ①② ③ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中有如下反应:2SO2(g)+O2 (g)![]() 2 SO3(g);△H<0。某研究小组进行了当其他条件不变时,改变某一条件对上述反应影响的研究,下列分析正确的是
2 SO3(g);△H<0。某研究小组进行了当其他条件不变时,改变某一条件对上述反应影响的研究,下列分析正确的是
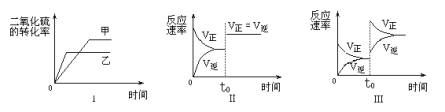
①图Ⅰ研究的是温度对化学平衡的影响,且乙的温度较高
②图Ⅱ研究的是催化剂对反应速率的影响,化学平衡不移动
③图Ⅱ研究的是t0时刻通入氦气增大体系压强对反应速率的影响
④图Ⅲ研究的是t0时刻增大O2的浓度对反应速率的影响
A. ①②B. ②③C. ②④D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z在周期表中的位置如图所示,下列说法错误的是( )
![]()
A. 简单氢化物沸点:X>Z
B. 用pH试纸可测得YZX和YZX4溶液分别显碱性和中性
C. W的单质可用于工业冶炼铁、硅
D. 原子半径:Y>W>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某澄清透明溶液可能含有Na+、Cl-、CO32-、SO42-、Mg2+、NH4+中的几种,进行如下实验:将上述溶液分为两等份,其中一份滴加足量的BaCl2溶液,得到白色沉淀4.66g;另一份溶液中滴加足量的NaOH溶液,得到0.58g白色沉淀,加热后产生标准状况下的气体0.224L,该气体能使湿润的红色石蕊试纸变蓝色。下列说法正确的是( )
A.溶液中可能有Na+、Cl-
B.溶液中一定没有Cl-、CO32-
C.溶液中一定有Na+、SO42-、Mg2+、NH4+
D.溶液中是否存在Na+只能用焰色反应确认
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理解释的是
A. 向K2Cr2O4溶液中滴入浓的NaOH溶液后,溶液黄色加深
B. 高压比常压更有利于合成SO3
C. 反应2SO2+O2![]() 2SO3 ΔH<0,工业上采取高温的措施有利于提高SO2的转化率
2SO3 ΔH<0,工业上采取高温的措施有利于提高SO2的转化率
D. 合成氨反应:N2+3H2![]() 2NH3 ΔH<0,为使氨的产率提高,理论上应采取低温高压的措施
2NH3 ΔH<0,为使氨的产率提高,理论上应采取低温高压的措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利多卡因盐酸盐(F)是一种酰胺类局麻药,对中枢神经系统有明显的兴奋和抑制双相作用,其合成路线如下图所示,请回答相关问题。
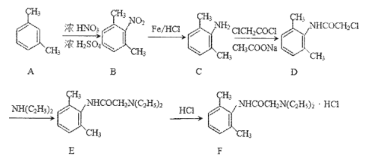
(1)A的系统名称是_____,D中的官能团名称是___。
(2)F的化学式是_____。
(3)B—C、D—E的反应类型依次是_____、_____。
(4)D与足量NaOH溶液加热充分反应的方程式是_____。
(5)G物质是比B多一个碳原子的同系物,符合下列要求的G的同系物有___种(不考虑立体异构),其中核磁共振氢谱有六组峰且面积比为3:2:2:2:1:1的结构简式是____(任写一种)。______
I.苯环上有两个取代基且其中一个不含碳原子 II.含有一COO—结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以苯酚为主要原料,经下列转化可合成高分子材料C和重要的有机合成中间体H(部分反应条件和产物已略去)

已知:R1CH2COOCH3+R2COOCH3 +CH3OH
+CH3OH
请回答下列问题:
(1)A→B的反应类型是___________。
(2)B→C的化学方程式为_________。
(3)D的官能团名称是_________。
(4)E→F的化学方程式为_______。
(5)G的结构简式是_________。
(6)F→G为两步反应,中间产物的结构简式是_______。
(7)芳香化合物M(C8H10O2)与E的水解产物互为同分异构体,1molM可与2 mol NaOH反应,其核磁共振氢谱中有3组峰且峰面积之比为3:1:1,则M的结构简式是_________(写出一种即可)。
(8)以CH3Cl、CH3ONa、NaCN为原料(其它无机试剂任选),结合题目已知信息,写出制备CH3COCH2 COOCH3的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、体积为2 L的密闭容器中进行反应:2A(g) ![]() 3B(g)+C(g),若反应物在前20 s由3 mol降为1.8 mol,则前20 s的平均反应速率为
3B(g)+C(g),若反应物在前20 s由3 mol降为1.8 mol,则前20 s的平均反应速率为
A. v(B)=0.03 mol·L-1·s-1 B. v(B)=0.045 mol·L-1·s-1
C. v(C)=0.03 mol·L-1·s-1 D. v(C)=0.06 mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com