
����Ŀ�������ȣ�SO2Cl2���������л��ϳɺ�ҩ������ȡ�ʵ��������SO2��Cl2�ڻ���̿��������ȡSO2Cl2[SO2(g)+Cl2(g)![]() SO2Cl2(l) ��H=-97.3kJ/mol]��װ����ͼ��ʾ������װ��ʡ�ԣ�����֪SO2Cl2���۵�Ϊ��54.1�棬�е�Ϊ69.1�棬��ǿ��ʴ�ԣ����˽Ӵ��������ά�ص�����������л����ˮ�ܷ������ҷ�Ӧ�������������ش��������⣺
SO2Cl2(l) ��H=-97.3kJ/mol]��װ����ͼ��ʾ������װ��ʡ�ԣ�����֪SO2Cl2���۵�Ϊ��54.1�棬�е�Ϊ69.1�棬��ǿ��ʴ�ԣ����˽Ӵ��������ά�ص�����������л����ˮ�ܷ������ҷ�Ӧ�������������ش��������⣺
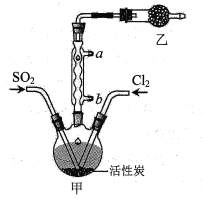
I��SO2Cl2���Ʊ�
��1��ˮӦ��___��ѡ�a����b�����ڽ��롣
��2����ȡSO2����������___�����ţ���
��Fe+18.4mol/LH2SO4
��Na2SO3+70%H2SO4
��Na2SO3+3mo/LHNO3
��3����װ����ʢ�ŵ��Լ���___��
��4���Ʊ���������Ҫ��װ�ü����ڱ�ˮԡ�У�ԭ����___��
��5����Ӧ����������л��������ʵ�������___��
II���ⶨ��Ʒ��SO2Cl2�ĺ�����ʵ�鲽�����£�
��ȡ1.5g��Ʒ��������Ba(OH)2��Һ����������ˡ�ϴ�ӣ���������Һ��������ƿ�У�
������ƿ�м��������ữ���ټ���0.2000mol��L��1��AgNO3��Һl00.00mL��
�������м���2mL������������ҡ����ʹ�������汻�л��︲�ǣ�
�ܼ���NH4Fe(SO4)2ָʾ������0.1000mol��L-1NH4SCN��Һ�ζ�����Ag+���յ��������Ϊ10.00mL��
��֪��Ksp(AgCl)=3.2��10-10Ksp(AgSCN)=2��10-12
��6���ζ��յ������Ϊ___��
��7����Ʒ��SO2Cl2����������Ϊ___%��������۲�����������������SO2Cl2������___���ƫ�ߡ�����ƫ�͡�����Ӱ�족����
���𰸡�b �� ��ʯ�� ��ȡ�����ȵķ�Ӧʱ���ȷ�Ӧ�������¶�ʹƽ�������ƶ������������SO2Cl2���� ���� ��Һ��Ϊ��ɫ�����Ұ�����ڲ���ɫ 85.5% ƫС
��������
��1��������ȴ��ˮӦ�ô��¿��룬�Ͽڳ���
��2���Ʊ�SO2������Ũ���ᷴӦ��Ҫ���ȣ�����������SO2��������70% H2SO4+Na2SO3���Ʊ�SO2��
��3�������ܵ�������������������Ӧ��û�м��ȣ���SO2��������ķ�ӦΪ���ȷ�Ӧ�����ڻ���һ����Cl2��SO2ͨ���������ݳ���������Ӧʹ�ü����Լ�������SO2Cl2��ˮ��ˮ�⣬���ü�ʯ�ң�
��4����ȡ�����ȵķ�Ӧʱ���ȷ�Ӧ�������¶�ʹƽ�������ƶ������������SO2Cl2���ʣ�
��5������е㲻ͬ��Һ�����������ķ��������Լ��л������뿪��ʵ�����������
��6����0.1000mol��L-1NH4SCN��Һ�ζ�����Ag+���յ㣬���ζ��ﵽ�յ�ʱNH4SCN��������NH4Fe(SO4)2��ָʾ����Fe3+��SCN��Ӧ��Һ����ɫ��������ڲ���ɫ������ȷ���ζ��յ㣻
��7����cmol��L-1NH4SCN��Һ�ζ�����Ag+���յ㣬�����������V�������Ag+�����ʵ���ΪVcmol����Cl��Ӧ��Ag+�����ʵ���Ϊ0.1000mol/L��0.1LVc��103mol����������SO2Cl2�����ʵ����� AgSCN�������ܽ�ȱ�AgClС���ɼ�������������ҡ����ʹAgCl�������汻�л��︲�ǣ������ڵμ�NH4SCNʱ����AgCl����ת��ΪAgSCN���������˲�����NH4SCN��AgCl��Ӧ����AgSCN��������ζ�ʱ���ĵ�NH4SCN��Һ�����ƫ�࣬�������ӵ����ʵ���ƫ�����������ӷ�Ӧ�������ӵ����ʵ���ƫС��
��1��������ȴ��ˮӦ�ô��¿��룬�Ͽڳ�����ˮӦ�ô�b�ڽ��룻
��2���Ʊ�SO2������Ũ���ᷴӦ��Ҫ���ȣ�����������SO2�������â�70% H2SO4+Na2SO3���Ʊ�SO2����ѡ�ڣ�
��3������װ��ͼ��֪�������ܵ�������������������Ӧ��û�м��ȣ���SO2��������ķ�ӦΪ���ȷ�Ӧ�����ڻ���һ����Cl2��SO2ͨ���������ݳ���������Ӧʹ�ü����Լ�������SO2Cl2��ˮ��ˮ�⣬���ü�ʯ�ң���������������SO2����ֹ�����е�ˮ���������������У�����װ����ʢ�ŵ��Լ��Ǽ�ʯ�ң�
��4����ȡ�����ȵķ�Ӧʱ���ȷ�Ӧ�������¶�ʹƽ�������ƶ������������SO2Cl2���ʣ�
��5������е㲻ͬ��Һ�����������ķ��������Լ��л������뿪��ʵ�����������
��6����0.1000mol��L-1NH4SCN��Һ�ζ�����Ag+���յ㣬���ζ��ﵽ�յ�ʱNH4SCN��������NH4Fe(SO4)2��ָʾ����Fe3+��SCN��Ӧ��Һ����ɫ��������ڲ���ɫ������ȷ���ζ��յ㣻�ʴ�Ϊ����Һ��Ϊ��ɫ�����Ұ�����ڲ���ɫ��
��7����0.1000mol��L-1NH4SCN��Һ�ζ�����Ag+���յ㣬�����������10.00mL�������Ag+�����ʵ���ΪVcmol=0.01��0.1000mol��L-1=1��10-3mol����Cl��Ӧ��Ag+�����ʵ���Ϊ0.2000mol/L��0. 1LVc��103mol��1.9��10-2mol����SO2Cl2�����ʵ���Ϊ1.9��10-2mol ��0.5=9.5��10-3mol ����Ʒ��SO2Cl2����������Ϊ![]() ��100%=85.5%�� ��֪��Ksp(AgCl)=3.2��1010��Ksp(AgSCN)=2��1012����AgSCN�������ܽ�ȱ�AgClС���ɼ�������������ҡ����ʹAgCl�������汻�л��︲�ǣ������ڵμ�NH4SCNʱ����AgCl����ת��ΪAgSCN���������˲�����NH4SCN��AgCl��Ӧ����AgSCN��������ζ�ʱ���ĵ�NH4SCN��Һ�����ƫ�࣬�������ӵ����ʵ���ƫ�����������ӷ�Ӧ�������ӵ����ʵ���ƫС�����Բ�õ������ӵ����ʵ���ƫС���ʴ�Ϊ��85.5%��ƫС��
��100%=85.5%�� ��֪��Ksp(AgCl)=3.2��1010��Ksp(AgSCN)=2��1012����AgSCN�������ܽ�ȱ�AgClС���ɼ�������������ҡ����ʹAgCl�������汻�л��︲�ǣ������ڵμ�NH4SCNʱ����AgCl����ת��ΪAgSCN���������˲�����NH4SCN��AgCl��Ӧ����AgSCN��������ζ�ʱ���ĵ�NH4SCN��Һ�����ƫ�࣬�������ӵ����ʵ���ƫ�����������ӷ�Ӧ�������ӵ����ʵ���ƫС�����Բ�õ������ӵ����ʵ���ƫС���ʴ�Ϊ��85.5%��ƫС��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�ǰ�߸պ��Ǻ����������ǣ�������
A.2molˮ��Ħ��������1molˮ��Ħ������
B.20%NaOH��Һ��NaOH�����ʵ���Ũ�Ⱥ�10%NaOH��Һ��NaOH�����ʵ���Ũ��
C.64g������������ԭ�����ͱ�״����22.4Lһ����̼����ԭ����g
D.200mL1mol/L�Ȼ�����Һ��c(Cl-)��200mL1mol/L�Ȼ�����Һ��c(Cl-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ྦྷ�������������صĹؼ����ϡ��������ɴֹ��Ʊ��ྦྷ��ļ����̡�
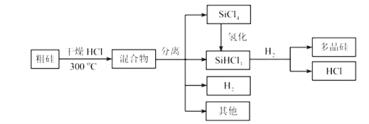
�ش��������⣺
(I)�����HCl��300��ʱ��Ӧ����1mol SiHCl3�����![]() ���ų�225kJ�������÷�Ӧ���Ȼ�ѧ����ʽΪ________________________��
���ų�225kJ�������÷�Ӧ���Ȼ�ѧ����ʽΪ________________________��![]() �ĵ���ʽΪ__________________��
�ĵ���ʽΪ__________________��
(II)��![]() �⻯Ϊ
�⻯Ϊ![]() �����ַ�������Ӧ�ķ�Ӧ����Ϊ��
�����ַ�������Ӧ�ķ�Ӧ����Ϊ��
��SiCl4(g)+H2(g)![]() SiHCl3(g)+HCl(g)��H1>0
SiHCl3(g)+HCl(g)��H1>0
��3SiCl4(g)+2H2(g)+Si(s)![]() 4SiHCl3(g) ��H2>0
4SiHCl3(g) ��H2>0
��3SiCl4(g)+H2(g)+Si(s)+HCl(g)![]() 3SiHCl3��H3
3SiHCl3��H3
��Ӧ�۵�![]() ______������H1����H2��ʾ�����¶����ߣ���Ӧ�۵�ƽ�ⳣ��K______������������������С����������������
______������H1����H2��ʾ�����¶����ߣ���Ӧ�۵�ƽ�ⳣ��K______������������������С����������������
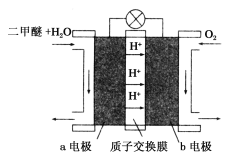
(III)��ͼΪ��ɫ��Դ��������(CH3OCH3)ȼ�ϵ�����Ĺ���ԭ��ʾ��ͼ��b�缫��________������д�������ĵ缫��Ӧ����ʽ��__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������dz�����ˮ����������ҵ���Ʊ���������ж��ַ�����ij��ȤС������мΪԭ��ģ���Ʊ�������ص��������£�
���������ϣ�������س��Ϻ�ɫ�������Ի�������Һ�п��ٲ���O2��
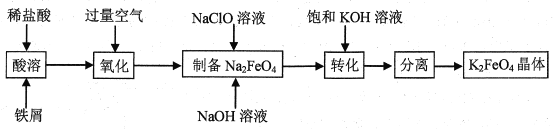
�ش��������⣺
��1������������ͨ����������������������������е��ŵ���___��
��2��Ϊ�˼��顰����������������FeCl3��Һ���Ƿ���Fe2+����ѵļ����Լ���___�����ţ���
a.K3[Fe(CN)6]��Һ b.NaOH��Һ c.����KI��ֽ
��3����д�����Ʊ�����Ӧ�����ӷ���ʽ___��
��4����ת��������ʹ�ù�������KOH��Һ��ԭ����___��
��5�������롱���̻��K2FeO4�����ϵ�в������������ᾧ�����ˡ�ϴ�ӡ��������ϴ��ʹ�õ����ϴ�Ӽ���___�����ţ���
a.��ˮ b.���ϡNaOH��Һ c.���ŨKOH��Һ
��6����ⷨ�Ʊ�K2FeO4������������ʵ�����Ʊ�ԭ����ͼ��ʾ�����������ĵ缫��Ӧʽ��___��

��7��̽��K2FeO4�����ʡ�ȡ������Ϻ�ɫ��Һ������ϡ���ᣬ�۲쵽��Һ���Ϻ�ɫ��Ϊ��ɫ�����ռ�������ɫ���塣��ͬѧ��Ϊ��������һ������Cl2����ͬѧ��Ϊ�������л����ܺ���___�������ʵ��֤����ͬѧ�IJ²�___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���谢���ӵ�����ֵ��NA��ʾ������˵����ȷ���ǣ� ��
A.������1LpH��3����������Һ�У���H+��ĿΪ0.3NA
B.A1��NaOH��Һ��Ӧ����11.2L���壬ת�Ƶĵ�����Ϊ0.5NA
C.NO2��N2O4��������������ag�����к�������Ϊ0.5aNA
D.1mo1KHCO3�����У�����������֮��Ϊ3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������ʽṹ�������У������������
��CH3COOH������̼ԭ�ӵ��ӻ�������sp2��sp3����
��Ԫ��Geλ�����ڱ���������IVA�壬��������Ų�ʽΪ [Ar]4s24p2������P��
�۷Ǽ��Է����������и߶ȶԳ��ԣ���BF3��PCl5��H2O2��CO2�����ķ���
�ܱ��д��ڼ��Թ��ۼ���������ֻ�ѧ��������
��Cu(OH)2��һ����ɫ��״���������������ᡢ��ˮ��Ҳ����������������Һ��
������̬��HgCl2�����磬HgCl2ϡ��Һ�����ĵ�������˵����̬HgCl2�Ƿ��Ӿ��壬Ϊ�ǵ����
�߰�ˮ�д�NH3��H2O��������á�����������ʾ����ϳ�NH3��H2O���ӣ����ݰ�ˮ�����ʿ�֪NH3��H2O�Ľṹʽ�ɼ�Ϊ��
A. 4�� B. 5�� C. 6�� D. 7��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ,�����й�������ȷ���ǣ� ��
A.��״���£�22.4L���麬�еĹ��ۼ�����Ϊ19NA
B.1L 0.1 mol��L-1 Na2CO3��Һ������������֮��Ϊ0.3NA
C.16g O2��14C2H4�Ļ����������������Ϊ8NA
D.�ܱ�������l.5mol H2��0.5mol N2��ַ�Ӧ���õ�NH3�ķ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж��ֻ������H2S��COS���ʻ���SO2�ȣ����ǶԻ�������һ����Ӱ�졣
��1��H2S�� K2CO3��Һ���պ�����������ʽ������������һ����ʽ���Ļ�ѧʽ��____��
��2��COS���ʻ���ȼ��ʱ��SO2���ɣ���ԭ��Ϊ��2COS+3O2![]() 2CO2+2SO2����ת��3.612��1024�����ӣ���μӷ�ӦCOS���ʻ������ʵ�����____mol��
2CO2+2SO2����ת��3.612��1024�����ӣ���μӷ�ӦCOS���ʻ������ʵ�����____mol��
��3���糧�ų��������к���CO��SO2�ȡ�SO2����H2S��Ӧ����S��H2O��˵��SO2����____�ԡ�CO�ڴ�������ʱ����SO2��Ӧ��ת��Ϊһ�ֹ����һ�������塣�÷�Ӧ�Ļ�ѧ����ʽ��___��
��4��ʯ��ʯ��Ϊ�����������Ч���շ����е�SO2����������IJ�����
����ú̿�м���ʯ��ʯ�ɼ���ȼ��ʱSO2���ŷ�����������CaSO4���÷�Ӧ�Ļ�ѧ����ʽ��____��
������Ϊ�������������;���ɲ�ȡ�Ĵ�ʩ��____������ţ���
a������ֱ���ø���ú��ȼ�ϡ� b���ѹ������̴���ߡ�
c��ȼ������ d����������Դ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��S2Cl2�dzȻ�ɫҺ�壬����й©�������Ϣ�����壬��ˮ���ɼ�����ӷ�����������������Һ������ӽṹ��ͼ��ʾ�����й���S2Cl2��˵���д������( )

A.S2Cl2Ϊ�Ǽ��Է���
B.�����мȺ��м��Լ��ֺ��зǼ��Լ�
C.��S2Br2�ṹ���ƣ��ۡ��е�S2Br2>S2Cl2
D.��ˮ��Ӧ�Ļ�ѧ����ʽ����Ϊ2S2Cl2��2H2O===SO2����3S����4HCl
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com