
【题目】根据学过的化学知识填空:
(1)金刚石和石墨物理性质差异较大的原因是____________________;一氧化碳和二氧化碳性质不同的原因是_____________________。
(2)天然气的主要成分燃烧的化学方程式是_________________________。
(3)煤在空气中燃烧需要满足的条件是__________;吹灭蜡烛的原理是____________。
(4)生铁和钢都是铁的合金,由于________不同,二者性能不同。
【答案】碳原子的排列方式不同分子构成不同CH4+2O2![]() CO2+2H2O温度达到着火点,降低温度到着火点以下含碳量
CO2+2H2O温度达到着火点,降低温度到着火点以下含碳量
【解析】
(1)因为金刚石、石墨的内部碳原子的排列方式不同,导致两种物质物理性质的差异很大;一氧化碳是一氧化碳分子构成的,而二氧化碳是二氧化碳分子构成,两者一个分子中相差一个氧原子,而分子是保持物质化学性质的最小微粒,分子不同,化学性质也就不同.所以一氧化碳和二氧化碳的化学性质不同,故答案为:碳原子的排列方式不同;分子构成不同;
(2)天然气的主要成分是甲烷,甲烷在点燃条件下燃烧生成二氧化碳和水,反应的化学方程式为CH4+2O2![]() CO2+2H2O,故答案为:CH4+2O2
CO2+2H2O,故答案为:CH4+2O2![]() CO2+2H2O;
CO2+2H2O;
(3)煤是可燃物,空气中有氧气,因此煤在空气中燃烧需要满足的条件是温度达到其着火点;吹灭蜡烛的原理是降低温度到着火点以下,故答案为:温度达到着火点;降低温度到着火点以下;
(4)生铁和钢都是铁的合金,二者性能不同是因为含碳量不同,故答案为:含碳量。


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】某化学小组欲进行如下的实验探究金属与浓硫酸反应。试回答下列问题:
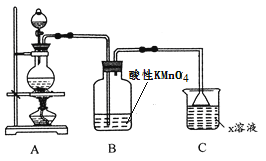
(1)利用上图装置研究铜与浓硫酸反应,反应的化学方程式为____________。C装置的作用_____________。
(2)将上述实验中的铜改为铁,在常温下进行,无明显现象,其原因是__________。在加热条件下,实验的后阶段可观察到倒立的漏斗边沿有气体冒出,该气体可能为_______。
验证该气体的实验方案如下:
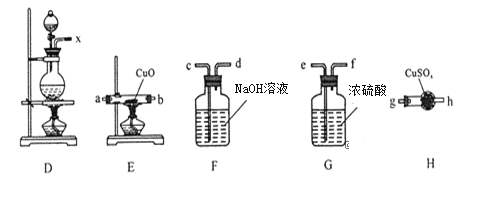
①装置连接顺序:X→ ___→___→___→___→a→b→_____;
②能证明上述假设成立的实验现象是_____________。
③某学习小组经过讨论认为该实验方案还不够严谨,你认为是否合理,若合理,则不作答,若不合理,请指出不严谨之处__________________________。
④若把D中的反应液倾倒入盛水的烧杯中,为氧化其中的某离子,可供选用的试剂: a、Cl2;b、Br2;c、稀硫酸和H2O2,从无污染角度考虑,你认为合适试剂是______(填字母),反应的离子反应方程式为_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.需要加热才能发生的反应一定是吸热反应
B.放热反应在常温条件下一定能进行
C.NaOH固体溶于水是放热反应
D.A+B=C+D是放热反应,说明A和B物质的总能量高于C和D的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用有机物C3H8为原料制取乙酸乙酯。它们之间的转化关系如图:

已知:CH2=CH2+CH3COOH![]() CH3COOCH2CH3,下列说法正确的是( )
CH3COOCH2CH3,下列说法正确的是( )
A. 反应过程①在石油工业上称作分馏,属于化学变化
B. 用新制碱性氢氧化铜悬浊液可区分有机物B、C 和D
C. 通过直接蒸馏乙酸乙酯和有机物C 的混合物,可分离得到纯的乙酸乙酯
D. 相同条件下乙酸乙酯在氢氧化钠溶液中水解不如在稀硫酸中完全
查看答案和解析>>
科目:高中化学 来源: 题型:
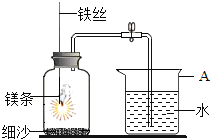
【题目】某学习小组用右图做镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%。
(1)瓶底铺细沙的原因是__________________________________________;
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的________%。现进入集气瓶中水的体积约为其容积的70%,根据空气的组成推测原因可能是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g)△H=-192.9kJ/mol
下列说法正确的是( )
A. CH3OH的标准燃烧热为△H=192.9kJ·mol-1
B. 反应①中的能量变化如图所示

C. 根据②推知反应:CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ/mol
D. CH3OH转变成H2的过程一定要吸收能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据热化学方程式2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1,下列说法或表达正确的是( )
A. 2 mol水蒸气分解生成2 mol氢气与1 mol氧气需吸收483.6 kJ的热量
B. 2H2(g)+O2(g)===2H2O(l) ΔH>-483.6 kJ·mol-1
C. H2(g)+![]() O2(g)===H2O(g) ΔH=241.8 kJ·mol-1
O2(g)===H2O(g) ΔH=241.8 kJ·mol-1
D. 1 mol氢气与0.5 mol 氧气总能量小于1 mol水蒸气的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)纯水在T℃时,pH=6,该温度下0.1 molL-1 的NaOH 溶液中,由水电离出的c(OH-)=__________ molL-1。
(2)在25℃下;将amol·L-1的NaX溶液与0.01mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,则a__________0.01(填“>”、“<”或“=”);用含a的代数式表示HX 的电离常数 Ka=________。
(3)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
①CO(g)+NO2(g)=NO(g)+CO2(g) △H=-aKJ·mol-1 (a>0)
②2CO(g)+2NO(g)=N2(g)+2CO2(g) △H=-bKJ·mol-1 (b>0)
若用标准状况下5. 6LCO将NO2还原至N2(CO完全反应),则整个过程中转移电子的物质的量为_____ mol,放出的热量为_________ kJ(用含有a和b的代数式表示)。
(4)已知AgCl、Ag2CrO4 (砖红色) 的Ksp分别为2×10-10和2.0×10-12。分析化学中,测定含氯的中性溶液中Cl- 的含量,以K2CrO4作指示剂,用AgNO3溶液滴定。滴定过程中首先析出沉淀_________,当溶液中Cl- 恰好完全沉淀(浓度等于1.0×10-5 mol·L-1) 时,此时溶液中c(CrO42-)等于__________ molL-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com