
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
| IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)元素②的原子结构示意图为_____。
(2)元素③、④、⑤、⑥原子半径由大到小为_____。
(3)上述 8 种元素中,非金属性最强的是_____。
(4)元素②、③形成的气态氢化物稳定性:_____>_____;元素①、③、⑤可形成既含离子键又含极性共价键的化合物,写出其电子式:_____。
(5)元素⑦的最高价氧化物对应的水化物与元素⑤最高价氧化物对应的水化物溶液反应的离子方程式为_____。
(6)写出金属铜与②最高价氧化物对应的水化物稀溶液反应的离子方程式_____。
(7)从原子结构的角度解释元素③和⑦的非金属性强弱:_____
【答案】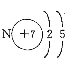 Na>Al>O>F F H2O NH3
Na>Al>O>F F H2O NH3 ![]() H++OH-=H2O 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O O与S相比,电子层数少,原子核对最外层电子的吸引能力强,故易得到电子,故O的非金属性比S强
H++OH-=H2O 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O O与S相比,电子层数少,原子核对最外层电子的吸引能力强,故易得到电子,故O的非金属性比S强
【解析】
根据各元素在周期表中的位置可以知道,①为H元素,②为N元素,③为O元素,④为F元素,⑤为Na元素,⑥为Al元素,⑦为S元素,⑧为Cl元素,据此回答。
(1)N元素的原子结构示意图为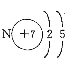 ;
;
(2)同一周期从左向右原子半径依次减小,同一主族原子半径从上到下依次增大,故N、O、Na、Al的原子半径从大到小依次是Na>Al>O>F;
(3)同一周期从左向右非金属性依次增强,同一主族从上到下非金属性依次减小,故8种元素中非金属性最强的是F元素;
(4)两种气态氢化物分别为NH3和H2O,因O的非金属性强,故H2O的稳定性强;H、O、Na三种元素形成的离子化合物为NaOH,电子式为![]() ;
;
(5)元素⑦的最高价氧化物对应的水化物为H2SO4,元素⑤最高价氧化物对应的水化物为NaOH,二者发生反应的离子方程式为H++OH-=H2O;
(6)②最高价氧化物对应的水化物为HNO3,其稀溶液与Cu反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(7)O与S相比,电子层数少,原子核对最外层电子的吸引能力强,故易得到电子,故O的非金属性比S强。


科目:高中化学 来源: 题型:
【题目】已知反应 A+B===C+D 的能量变化如图所示,下列叙述正确的是( )

A.A 的能量一定低于 C 的能量,B 的能量一定低于 D 的能量
B.因为该反应为吸热反应,故一定要加热,反应才能进行
C.破坏反应物中的化学键所吸收的能量一定小于形成生成物中化学键所放出的能量
D.A 和 B 的总能量一定低于 C 和 D 的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾可做净水剂的原因:_______________________________________________(请用相关的化学用语和文字描述),若向明矾的水溶液中加入饱和的小苏打溶液,则观察到的现象是_________________________,有关的离子方程式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)性能优越,钛被称为“第三金属”(铁、铝分为第一、二金属),工业以TiO2冶炼Ti的主要反应有:①TiO2+2C+2Cl2![]() TiCl4+2CO ②TiCl4+2Mg
TiCl4+2CO ②TiCl4+2Mg![]() 2MgCl2+Ti下列叙述正确的是( )
2MgCl2+Ti下列叙述正确的是( )
A. 反应①是置换反应 B. 反应②是复分解反应
C. 反应①中TiO2是氧化剂 D. 反应②中金属镁是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂制备净水剂硫酸铁铵晶体[NH4Fe(SO4)2·6H2O]的一种方案如下:

下列说法不正确的是
A. 滤渣A的主要成分是CaSO4
B. 相同条件下,NH4Fe(SO4)2·6H2O净水能力比FeCl3强
C. “合成”反应要控制温,温度过高,产率会降低
D. “系列操作”包括蒸发浓缩、降温结晶、过滤、干燥等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表中短周期的一部分,四种元素均不是稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是( )

A. 原子半径:W>Z
B. 气态氢化物的稳定性:W>X
C. W的最高正化合价与负化合价的绝对值可能相等
D. Z的最高价氧化物的水化物可能为强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由芳香烃M合成某有机物N的一种流程如下:

已知部分信息如下:
①![]()
![]()
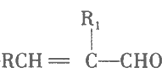 +H2O
+H2O
② 
![]()
③ ![]()
![]()
![]()
请回答下列问题:
(1)M分子最多有_______________个原子共平面。
(2)C中含有的官能团名称是__________;能测定C中含官能团种类的仪器名称是____________________________。
(3)E的结构简式为______________________
(4)F和G反应生成N的化学方程式为_________________________________________。
(5)T是F的同分异构体,T同时具备下列条件的结构有________________________种。
①能与新制氢氧化铜浊液共热产生红色固体;
②含碳碳三键;
③遇氯化铁溶液发生显色反应。
(6)以丙烯为原料合成![]() ,设计合成路线:_______________(溶剂和无机试剂任选)。
,设计合成路线:_______________(溶剂和无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中Mg2+、NH4+、Al3+三种离子的物质的量之比为( )

A. 1∶1∶2B. 2∶2∶1
C. 1∶2∶2D. 9∶2∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,可逆反应X(g)+3Y(g)![]() 2Z(g)达到平衡时,测得Y转化了37.5%,X转化了25%,下列叙述正确的是
2Z(g)达到平衡时,测得Y转化了37.5%,X转化了25%,下列叙述正确的是
A.升高温度,正逆反应速率增大,平衡不移动
B.开始充入容器中的X、Y物质的量之比为1∶2
C.若Y的反应速率为0.2mol·L-1·s-1,则Z的反应速率为0.3 mol·L-1·s-1
D.若容器体积不变,向容器中充入氦气,压强增大,反应速率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com